懡曽岦偐偮抜奒揑偵恑峴偡傞嵶朎暘壔偵偍偗傞塣柦寛掕儊僇僯僘儉偺夝柧媶椞堟棯徧丗嵶朎塣柦惂屼
尋媶壽戣柤
RUNX1偲僄僺僕僃僱僥傿僢僋惂屼婡峔攋抅偺嫤挷嶌梡偵傛傞MDS敪徢婡峔偺夝柧
尋媶撪梕
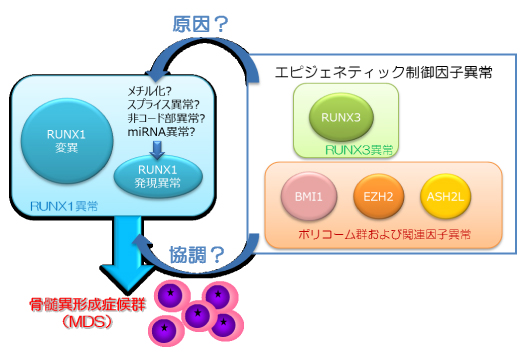
丂杮尋媶偱偼丄RUNX1偲僄僺僕僃僱僥傿僢僋惂屼婡峔攋抅偺嫤挷嶌梡偵傛偭偰敪徢偡傞憿寣婍庮釃丆摿偵崪悜堎宍惉徢岓孮乮MDS乯偺暘巕敪徢婡峔偺夝柧偡傞丅
丂尋媶戙昞幰偺僌儖乕僾偼丄RUNX1堚揱巕偺僎僲儉堎忢偑姴嵶朎暘壔忈奞丒庮釃尨惈傪桳偟丆憿寣婍庮釃敪徢偺拞怱揑栶妱傪扴偭偰偄傞偙偲傪夝愅丒曬崘偟偰偒偨乮Blood 2003, 2004, 2009, 2010乯丅偦偺摿挿偼丄姵幰偱堚揱巕堎忢傪尒弌偟丄昦懺偵婎偯偄偰堚揱巕堎忢偐傜偺敪徢儊僇僯僘儉傪悇應偟偰婡擻夝愅傪峴偆丄偲偄偆椪彴偲婎慴偺嫶搉偟揑側尋媶丄偲偄偆揰偱偁傞丅摉尋媶椞堟挿乮杒懞攷巑乯偲嫟偵丄偙傟傑偱偵RUNX1傗CEBPA曄堎偑MDS昦懺傪婯掕偡傞堚揱巕堎忢偱偁傞偙偲傪帵偟偨乮Blood 2008, 2011, 2013乯丅偟偐偟RUNX1堚揱巕堎忢扨撈偱偼vivo偱偺憿寣婍庮釃敪徢偵偼帄傜側偄丅偟偨偑偭偰丆偝傜側傞堚揱巕偺堎忢偑娭傢偭偰偄傞偲峫偊傜傟丆MDS敪徢傊偺娭梌偑嫮偔帵嵈偝傟傞僄僺僕僃僱僥傿僢僋惂屼場巕偵拝栚偟偨丅帺尡徢椺偱偼丆RUNX1曄堎丆RUNX3崅敪尰丆BMI1崅敪尰丆EZH2掅敪尰丒崅敪尰側偳偑條乆側慻傒崌傢偣偱擣傔傜傟丆傑偨HBO1堎忢偑娭梌偡傞敀寣昦徢椺傪摨掕偟偨偙偲偐傜丆僄僺僕僃僱僥傿僢僋惂屼場巕堎忢偑RUNX1偲嫤挷偟偰MDS敪徢偵娭傢偭偰偄傞偙偲偑嫮偔帵嵈偝傟偨丅偦偙偱杮尋媶偱偼丆姵幰偵偍偗傞RUNX1偲僄僺僕僃僱僥傿僢僋惂屼場巕偺曄堎丒敪尰堎忢傪専嶕偟丆偙傟傜偺in vitro偍傛傃in vivo偱偺婡擻傪夝愅偡傞偙偲偵傛傝丆惓忢丒堎忢RUNX1偲僄僺僕僃僱僥傿僢僋惂屼場巕偺憡屳嶌梡偵傛傞MDS偺暘巕敪徢婡彉夝柧傪帋傒傞丅
庡側榑暥
- 尨揷丂峗摽
-
Harada Y, Inoue D, Ding Y, Imagawa J, Doki N, Matsui H, Yahata T, Matsushita H, Ando K, Sashida G, Iwama A, Kitamura T, and *Harada H.
RUNX1/AML1 mutant collaborates with BMI1 overexpression in the development of human and murine myelodysplastic syndromes.
Blood. 121: 3434-46, 2013.Imagawa J, Harada Y, Shimomura T, Tanaka H, Okikawa Y, Hyodo H, Kimura A, and *Harada H.
Clinical and genetic features of therapy-related myeloid neoplasms after chemotherapy for acute promyelocytic leukemia.
Blood. 116: 6018-6022, 2010.Ding Y, Harada Y, Imagawa J, Kimura A, and *Harada H.
AML1/RUNX1 point mutation possibly promotes leukemic transformation in myeloproliferative neoplasms.
Blood. 114: 5201-5205, 2009.