ポイント
- ミオクロニー発作など、てんかん患者類似症状をモデルマウスで確認
- 脳室壁の上衣細胞繊毛の運動機能の低下など特異的な異常を発見
- てんかんの発症メカニズムの理解や治療法の開発・改良に大きく寄与
要旨
独立行政法人理化学研究所(野依良治理事長)は、最も発症数の多いてんかんとして知られている「若年性ミオクロニーてんかん」で変異が見られる遺伝子「EFHC1」のノックアウトマウスを初めて作製し、このマウスがてんかん患者と類似の症状とともに、発症機序の理解につながりうる特異的な複数の異常を示すことを見いだしました。脳科学総合研究センター(田中啓治センター長代行)神経遺伝研究チームの山川和弘チームリーダー、鈴木俊光基礎科学特別研究員、および同センター神経回路発達研究チーム、津本研究ユニット、神経蛋白制御研究チーム、行動遺伝学技術開発チーム、大阪医科大学、名古屋市立大学などによる共同研究の成果です。
若年性ミオクロニーてんかんは、思春期に発症し、起床時に頻発するミオクロニー発作※1、強直間代発作※2などを特徴とする、最も発症頻度の高いてんかんの1つです。神経遺伝研究チームはこれまでに、多くの若年性ミオクロニーてんかん患者家系の遺伝的連鎖解析※3を行い、第6染色体の一部領域に原因遺伝子の存在部位を絞り込み、この領域から、てんかん患者に特異的な変異がみられる新規遺伝子「EFHC1」を発見しました(2004年、Nature Genetics)。今回、この遺伝子のノックアウトマウスを初めて作製し、このマウスがミオクロニー発作やけいれん誘発剤に対する高い感受性など、てんかん患者と類似の症状を示すことに加え、脳室壁の上衣細胞繊毛の運動機能の低下などいくつかの特異的な異常症状を示すことを見いだしました。これらの成果は、EFHC1遺伝子の異常が確かにてんかんの発症につながることを明らかにするとともに、今後、さらなるてんかんの発症メカニズムの理解、治療法の開発・改良に大きく寄与するものと期待されます。
本研究成果は、英国の科学雑誌『Human Molecular Genetics』(ヒューマン・モレキュラー・ジェネティクス)オンライン版(1月15日付け:日本時間1月16日)に掲載されます。
背景
てんかんは、反復するてんかん発作(強直間代発作(きょうちょくかんたいほっさ))、欠神発作(けつしんほっさ)※4など)を特徴とし、世界の全人口のおよそ3%が一生を通じて一度は発症する頻度の高い神経疾患です。てんかんには、多数の種類があり、大きくは特発性てんかん、症候性てんかん、もしくは潜因性てんかんに分類されます※5。中でも特発性てんかんは、てんかん全体の約7割を占めるとされています。その発症のほとんどに遺伝的背景が想定され、原因となる遺伝子も100個を大きく上回ると予想されています。現在までに明らかにされた特発性てんかんの原因遺伝子は、およそ17個の遺伝子を数え、うち14個の遺伝子がイオンチャネル※6をコード(暗号化)しています(表1)。
特発性てんかんの1つ「若年性ミオクロニーてんかん」は、8歳から20歳程度の間(思春期)で発症し、起床時に頻発するミオクロニー発作、全身性強直間代発作を特徴とする最も発症頻度の高い優性遺伝形式をとるてんかんで、少なく見積もっても全てんかん患者の7~9%を占め、特発性てんかんの20~25%に及ぶとされています。若年性ミオクロニーてんかんの主要な原因遺伝子(患者の半数の発症に関与する)と考えられるものが、遺伝的連鎖解析により第6染色体短腕部にあるとされていました。神経遺伝研究チームはこれまでに、この領域に若年性ミオクロニーてんかん患者で複数の変異を示す「EFHC1」遺伝子を同定しています(Suzuki et al., Nature Genetics, 36: 842-849, 2004)。このEFHC1遺伝子がコードしているタンパク質「ミオクロニン1」は、胎生期には脈絡叢、出生後には脳室壁を覆う上衣細胞の繊毛に強く発現するもので(Suzuki et al., Biochemical and Biophysical Research Communications 367: 226-233, 2008)、イオンチャネルではありませんでした。その後、ほかの研究グループからも新たな複数のEFHC1遺伝子変異が報告され、EFHC1遺伝子は若年性ミオクロニーてんかんだけでなく、ほかの種類の特発性てんかんの原因遺伝子でもあることが見いだされてきています。このEFHC1遺伝子の変異が引き起こすてんかんの発症機序を明らかにするためには、この遺伝子に変異を導入したモデル動物を対象とした解析が望まれますが、これまでそのような報告はありませんでした。
研究手法と成果
研究グループは、相同組み換え法※7によってマウスEfhc1遺伝子をノックアウトし、ヘテロ接合体※8(+/-)を作製しました。変異を導入したヘテロ接合体(+/-)マウス同士を掛け合わせたところ、野生型(+/+)、ヘテロ接合体(+/-)、ホモ接合体※8(-/-)のマウスがほぼ通常の割合(1:2:1)で生まれました。
これらのマウスの脳で発現するタンパク質のウェスタンブロット解析※9では、ヘテロ接合体(+/-)マウスではEfhc1遺伝子がコードするミオクロニン1タンパク質が半減し、ホモ接合体(-/-)マウスでは消失していることを確認しています(図1)。
ヘテロ接合体(+/-)、ホモ接合体(-/-)マウスはともに、外見はほぼ正常に育ちました。しかし、出生7~8カ月頃から、ミオクロニー発作を起こし始め、その頻度はヘテロ接合体(+/-)、ホモ接合体(-/-)マウスでほとんど同じでした(図2)。ミオクロニー発作は野生型(+/+)マウスではほとんど見られません。
けいれん誘発剤であるペンチレンテトラゾールを投与し、けいれんを生じるまでの時間を測定したところ、4~5月齢、9~12月齢ともにヘテロ接合体(+/-)およびホモ接合体(-/-)マウスで、野生型に比べてけいれんを生じるまでの時間が大きく短縮されることが分かりました(図3)。
免疫組織化学解析※10では、野生型(+/+)マウスで見られるミオクロニン1タンパク質の胎生期脈絡叢や出生後の上衣細胞繊毛における発現が、ホモ接合体(-/-)マウスでは消失していることを確認しています(図4)。ホモ接合体(-/-)マウスでは、上衣細胞繊毛の構造そのものには異常はみられませんが、運動率に大きな低下が認められました(図5)。さらに、脳室の拡大などの異常も見いだしました。
これらの成果は、EFHC1遺伝子異常が確かにてんかんの発症につながることを確認するとともに、上衣細胞繊毛運動機能低下などの特異的な異常がてんかん発症の背景に存在する可能性を示唆するものとなりました。
今後の期待
若年性ミオクロニーてんかんは、てんかんの中でも最も発症頻度の高いものの1つであることから、このてんかんで複数の変異がみられるEFHC1遺伝子は、これまでに報告されてきた数あるてんかん原因遺伝子の中でも特に重要なものであるといえます。また、てんかん全体の7割を占める特発性てんかんの原因遺伝子のほとんどがイオンチャネルをコードする中、EFHC1遺伝子がコードするミオクロニン1タンパク質は、イオンチャネルではないことから、今までに提示されたことがないまったく新しいてんかんの発症機構の存在をも示唆するものです。これらのことから、EFHC1遺伝子変異により引き起こされるてんかんの発症機構を理解することは、若年性ミオクロニーてんかんばかりではなく、てんかん全体の発症メカニズムの理解にもつながると予想できます。今回の知見と作製したモデルマウスは、今後、治療法の開発・改良にも大きく寄与することが期待されます。
発表者
理化学研究所
脳科学総合研究センター 神経遺伝研究チーム
チームリーダー 山川 和弘
お問い合わせ先
脳科学研究推進部 鈴木 一郎(すずき いちろう)
Tel : 048-467-9596 / Fax : 048-462-4914
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ミオクロニー発作
短時間のぴくぴくとした骨格筋の攣縮発作。全身の場合もあれば顔面、体幹、四肢の一部に限局する場合もある。 - 2.強直間代発作
てんかん発作のなかでも最もよく見られるもので、大発作として知られる。固く激しい筋の収縮により四肢がこわばった姿勢に固定される。呼吸抑制のためにチアノーゼを呈し、しばしば眼球および頭部が側方へ偏位し、転倒を伴う。間代発作時には、筋の間欠的な攣縮によるガクガクとした動きを示す。 - 3.遺伝的連鎖解析
特定の遺伝疾患を有する多数の家系において、症状が染色体のどの領域と一緒に親から子へと伝わっているかを統計的に解析することにより、染色体上のどこに疾患原因遺伝子が存在するのかを予想する方法。 - 4.欠神発作
行動が突然中断し、眼球の短い上転を伴って、うつろな凝視が見られる発作。発作は数秒から30秒ほど続く。 - 5.てんかんの分類(特発性/症候性/潜因性)
てんかんは大きく、①脳内病変を認めず原因のはっきりしない、主にてんかん発作だけを症状とし一般に予後のよい特発性てんかんと、②背景となる脳内病変・脳損傷や代謝疾患など原因が明らかで、一般に難治/重篤な症候性てんかんの2つに分けられる。また、③脳内病変や代謝疾患など確定できる原因は見られないが、症状の重篤さやほかの精神神経症状の合併などから、特発性てんかんに分類し難いものを潜因性てんかんと呼んで区別する場合もある。 - 6.イオンチャネル
細胞膜を貫通するように存在し、カリウム、カルシウム、ナトリウムなどのイオンを通す穴を形成するタンパク質。電位差や情報伝達物質の結合により穴が開き、イオンが通過する。神経細胞膜にあるイオンチャネル群は情報伝達に重要な働きをしている。 - 7.相同組み換え法
当該遺伝子に変異を導入したDNAをマウス細胞に導入して相同組み換えを起こさせることにより、変異をゲノムDNAに導入する方法。この方法により、マウスES細胞(胚性幹細胞)に変異や欠失を導入し、ノックアウトマウスやノックインマウスなどが作製できる。 - 8.ヘテロ接合体、ホモ接合体
遺伝子は一個体当たり、父親由来と母親由来の2コピー存在する。ヘテロ接合体の場合では、正常遺伝子1コピーと変異遺伝子1コピー、ホモ接合体の場合では、変異遺伝子2コピーを有する。 - 9.ウェスタンブロット解析
組織などからのタンパク質抽出物を電気泳動し、膜に移した後、標的タンパク質に対する抗体で染色する解析法。 - 10.免疫組織化学解析
組織切片を標的タンパク質に対する抗体で染色し、その組織内での局在を解析する手法。

表1 特発性てんかん原因遺伝子がコードするタンパク質と染色体座
1~14がイオンチャネルをコードするタンパク質。今回ノックアウトした遺伝子EFHC1がコードするタンパク質ミオクロニン1は、イオンチャネルではない。
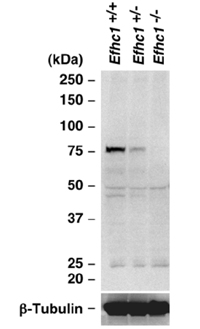
図1 野生型マウス、Efhc1変異ヘテロ接合体(+/-)、ホモ接合体(-/-)に、抗ミオクロニン1抗体を用いたウェスタンブロット解析
ミオクロニン1タンパク質(75kDa)は、ヘテロ接合体(+/-)では半減し、ホモ接合体(-/-)マウスでは消失していた。
注: Suzuki et al., Biochemical and Biophysical Research Communications 367:226-233, 2008より引用。今回の結果ではないが重要参考資料として示した。
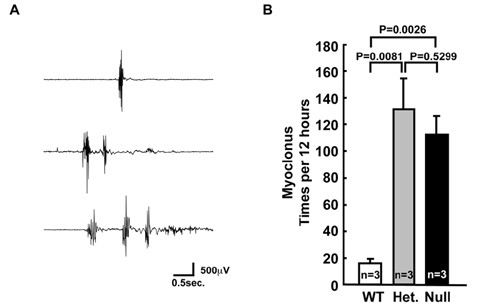
図2 (A)ホモ接合体で見られたミオクロニー発作時筋電図の3例
(B)12時間の観察でみられたミオクロニー発作の頻度
WT:野生型(+/+)、Het:ヘテロ接合体(+/-)、Null:ホモ接合体(-/-)
野生型に比べて、ヘテロ接合体およびホモ接合体において、ミオクロニー発作頻度が大きく増えた。
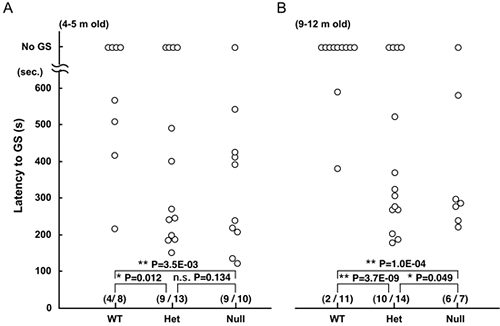
図3 けいれん誘発剤であるペンチレンテトラゾールを投与し強直間代発作(GS)を生じたマウスの個体数、および発作までの時間
(A)4~5月齢(B)9~12月齢
WT:野生型(+/+)、Het:ヘテロ接合体(+/-)、Null:ホモ接合体(-/-)
No GS:発作を生じなかったマウス、Latency to GS:発作を生じるまでの時間
野生型に比べて、ヘテロ接合体およびホモ接合体では、強直間代発作(GS)を示すマウスの割合が多くなり、また、発作までの時間に大きな短縮がみられた。具体的には、4~5月齢の場合、野生型8匹中4匹で発作が見られたのに対し、ヘテロ接合体13匹中9匹、ホモ接合体10匹中9匹で、発作が見られた。9~12月齢の場合、野生型11匹中2匹に対し、ヘテロ接合体14匹中10匹、ホモ接合体7匹中6匹で、発作が見られた。
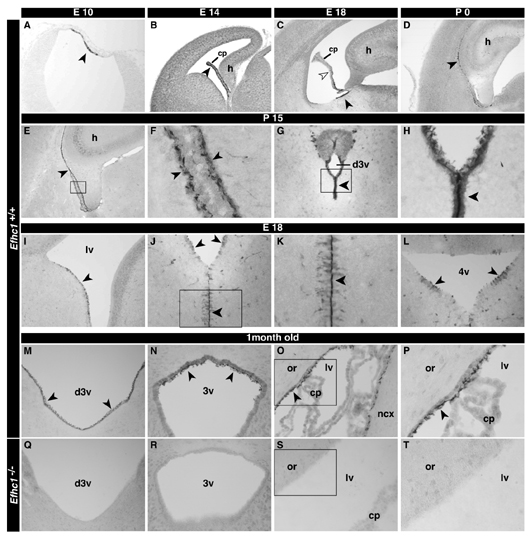
図4 抗ミオクロニン1抗体を用いた免疫組織化学解析
E:胎生日数、P:出生後日数、1 month old:出生後1カ月
cp:脈絡叢、h:海馬、d3v:第3脳室、lv:側脳室、4v:第4脳室、or:海馬上昇層、ncx:大脳皮質
野生型(+/+)マウスで見られたミオクロニン1タンパク質の胎生期脈絡叢(cp)および出生後の上衣細胞繊毛における発現(A-P)が、ホモ接合体(-/-)マウスでは消失していた(Q-T)。濃淡の濃い部分がミオクロニン1タンパク質の発現を示す(黒い矢印)。ミオクロニン1の発現は胎生期から出生後にかけて脈絡叢から脳室壁、上衣細胞繊毛へと移動していく(A-P)。E14(胎生14日)で脈絡叢(cp)に発現していたミオクロニン1はE18ではcpから消失している(白い矢印)。
注: Suzuki et al., Biochemical and Biophysical Research Communications 367:226-233, 2008より引用。今回の結果ではないが重要参考資料として示した。
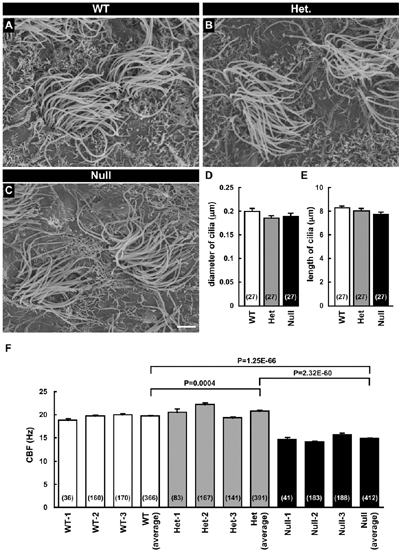
図5 上衣細胞繊毛の形態と運動速度
(A-C)上衣細胞繊毛の電子顕微鏡写真 (D)上衣細胞繊毛の直径
(E) 上衣細胞繊毛の長さ
(F) 上衣細胞繊毛の運動(振動)速度
WT:野生型(+/+)、Het:ヘテロ接合体(+/-)、Null:ホモ接合体(-/-)
ヘテロ接合体とホモ接合体の構造そのものには異常は見られなかったが、ホモ接合体では上衣細胞繊毛の運動速度の低下が見られた。
