2009年9月15日
独立行政法人 理化学研究所
独立行政法人 科学技術振興機構
国立大学法人 奈良先端科学技術大学院大学
妊娠中の胎盤に影響大の小胞体ストレス応答機能を発見
-小胞体ストレス応答分子のIRE1αは胎盤の発達に必須な役割を持つ-
ポイント
- 小胞体ストレスとIRE1機能解明のため、3種類の遺伝子改変マウスを作製
- 正常な発生過程で生じる胎盤の小胞体ストレスをマウス生体レベルで可視化
- 小胞体ストレス応答分子IRE1αの機能に、マウス生体レベルでアプローチ
要旨
独立行政法人理化学研究所(野依良治理事長)と独立行政法人科学技術振興機構(以下JST、北澤宏一理事長)、国立大学法人奈良先端科学技術大学院大学(磯貝彰学長)は、難病との関連性が指摘されている、小胞体ストレスの軽減にかかわる分子の1つである「IRE1α」が、妊娠中の胎盤で胎児の生死を左右する重要な機能を持つことを世界で初めて発見しました。理研基幹研究所(玉尾皓平所長)岩脇独立主幹研究ユニットの岩脇隆夫独立主幹研究員(JST さきがけ研究員兼任)、赤井良子テクニカルスタッフ、奈良先端科学技術大学院大学バイオサイエンス研究科の河野憲二教授、山中伸弥教授(現・京都大学物質-細胞総合システム拠点 iPS細胞研究センター長)らによる成果です。
ストレスは精神的なものを連想しがちですが、実は小さな細胞の世界にもストレスは存在します。小胞体ストレスは、細胞小器官の1つである小胞体への機能的な負担や障害により生じます。そもそも小胞体は、分泌タンパク質や膜タンパク質の加工工場として機能しています。それらタンパク質には生物が生きていくのに重要なものが数多く含まれるため、小胞体がうまく機能しない場合には、生命活動に大きな支障が生じます。これまでにアルツハイマー病やパーキンソン病などの神経変性疾患や糖尿病といった難病と、小胞体ストレスとの関連性が報告されてきました。しかしその一方、健康な生物で小胞体ストレスがどのような生命現象に関与するのかはよく分かっていませんでした。今回の研究では、小胞体ストレスをマウス生体レベルで可視化する技術と、遺伝子欠損技術を利用して、妊娠中の胎盤が軽度な小胞体ストレス状態にあること、そして小胞体ストレスを軽減するために働くとされているIRE1αが、胎盤の発達や機能に必須であることを明らかにしました。これは健全な繁殖・成長過程でのほ乳動物体内における小胞体ストレスの実態や、それを解消するための反応「小胞体ストレス応答」にかかわる分子の存在意義に迫る発見です。さらに、妊娠中の過度な小胞体ストレスと流産の危険性との関連性を解明する研究へ発展する可能性を持ち、医学的な立場から人間社会への貢献が期待できます。同時に、家畜動物の繁殖が重要な畜産などの産業にも影響を及ぼすと注目されます。
本研究成果は、JST戦略的創造研究推進事業 個人型研究(さきがけ)の研究領域「情報と細胞機能」(研究総括:三菱化学生命科学研究所 関谷剛男取締役所長)における研究課題「生理・病態環境下で生じる小胞体ストレスの実態とその応答の動物個体レベルでの解明」および研究領域「代謝と機能制御」(研究総括:国立医薬品食品衛生研究所 西島正弘所長)における研究課題「細胞内の蛋白質代謝を管理するストレス応答機構の解明」の一環として得られ、米国科学アカデミー紀要『Proceedings of the National Academy of Sciences of the United States of America』オンライン版に9月14日の週に掲載されます。
背景
生き物の体を構成する細胞は、さまざまなタンパク質を作り出しています。その中には、細胞外へ分泌される分泌タンパク質や細胞の膜上で働く膜タンパク質があり、ホルモンやその受容体は、分泌および膜タンパク質として作り出されています。細胞内のすべてのタンパク質は、リボゾーム※1によって合成されますが、その後、分泌および膜タンパク質になるべきタンパク質は、大抵の場合、小胞体と呼ばれる細胞小器官へと運ばれていきます。そこでタンパク質は、適切な立体構造へと形を整えられ、必要な(糖鎖などの)修飾が施されます。いわば、小胞体は分泌および膜タンパク質の加工工場としての機能を担っています。また、製品として完成したタンパク質をほかの細胞小器官へ輸送したり、未加工品や不良品タンパク質などの品質管理を行うことも小胞体の役割です。そのため大量のタンパク質や異常なタンパク質が小胞体内に蓄積すると、小胞体内ではタンパク質の品質管理上の負担が大きくなり、小胞体はストレスにさらされる状態になります。小胞体ストレスは、これまで主に培養細胞を用いて、人工的なストレス環境下で研究が進められてきた結果、生体内でも細胞が特殊な分泌細胞へと分化したときや、病的環境下にさらされると起こり得ると考えられていました。しかし、実際に生体レベルの研究、特にほ乳動物を用いた研究は、あまり進んでいませんでした。
小胞体ストレスにさらされている細胞は、それを解消するための反応「小胞体ストレス応答」を示すことが知られています。その代表的な例として、IRE1と呼ばれるタンパク質が小胞体に存在し、小胞体ストレスを感知すると、小胞体ストレスの解消に働く遺伝子の発現を活性化させます。IRE1の存在や機能は、酵母菌からヒトに至る広い範囲で進化的に保存されていて、小胞体ストレス応答で中心的な役割を担っているものと考えられています。酵母菌では、小胞体ストレスの感知から応答反応までを担う分子として、唯一IRE1しか知られていません。しかし、ほ乳動物での小胞体ストレス応答はより複雑で、IRE1のほかにPERKやATF6といったタンパク質も、小胞体でのストレス感知からストレス解消までの応答反応を担っています。また、ほ乳動物のIRE1は、少なくともα型とβ型の2種類があることも知られています。
これまでにいくつかの生物種で、小胞体ストレス応答分子(IRE1やPERK、ATF6)を欠損した変異体の解析が進められてきました。これらの研究は、小胞体ストレス応答分子や小胞体ストレス自体の、生体レベルにおける機能や実態を調べるために有効です。これまでにIRE1αを欠損したマウスは、ほかの小胞体ストレス応答分子を持っているにもかかわらず、胎児期に死んでしまうことが示されており、IRE1αがほ乳動物の発生過程で必須のものであることが分かってきました。一方、IRE1を欠損した酵母菌や線虫が、通常の(実験的に過度なストレスを与えたりしない)環境では生育できることが示され、それら生物にとって外因性のストレスがない限りIRE1が不要であることも分かってきました。研究グループはこれらの知見から、ほ乳動物特有の生命現象と、小胞体ストレスやIRE1の機能との重要な結びつきに着目し、マウス胎児期の小胞体ストレスとIRE1の機能を研究することにしました。
研究手法と成果
本研究では、マウス胎児期の小胞体ストレスとIRE1の機能の解明のために、3種類の遺伝子改変マウスの作製とその表現型解析に取り組みました。
(1)小胞体ストレス可視化マウスの作製と解析
研究グループは、生体内で生じる小胞体ストレス(狭義ではIRE1αの活性)を、ホタルの発光メカニズムの中心的な役割を担う酵素(ホタルルシフェラーゼ※2)を用いて検出することができるマウス、「小胞体ストレス可視化マウス」を作製しました。小胞体ストレスの可視化原理には、小胞体ストレスで活性化されたIRE1αが、XBP1メッセンジャーRNA(XBP1mRNA)※3を特異的にスプライシング※4することを利用しています。このマウスには、人工的に作製したXBP1とホタルルシフェラーゼの融合遺伝子を組み込み、IRE1αがこの人工遺伝子から作られるmRNAを通常のXBP1mRNAと同様にスプライシングすると、ホタルルシフェラーゼが発現し発光するように設計しました(図1)。研究グループは、この小胞体ストレス可視化マウスを使い、マウス胎児の小胞体ストレス発生(IRE1α活性化)部位を調査しました。その結果、妊娠中の胎盤が小胞体ストレス状態にあるとともに、IRE1αが活性化状態にあることを突き止めました(図2)。研究グループは、2002年にGFPの蛍光を利用した小胞体ストレス可視化マウスを作製しています。そのときは、成体マウスの膵臓(すいぞう)の小胞体ストレス状態を検出することができましたが、胎児期の小胞体ストレスやIRE1αの活性化は発見できませんでした。つまり、本研究で新たに作製したホタルルシフェラーゼ型の小胞体ストレス可視化マウスによって、初めて胎盤での小胞体ストレスを明らかにできました。
(2)IRE1αの遺伝子欠損マウスの作製と解析
研究グループは、2007年のノーベル医学生理学賞の対象となったジーンターゲティング技術※5を用いて、IRE1αの遺伝子を全身で欠損させたマウス、「IRE1αの遺伝子欠損マウス」を作製しました。このマウスは、これまでの研究から胎児期に死んでしまうことが分かっていたので、胎児がまだ生きている妊娠11~13日目の時期に胎児を母体から取り出し、IRE1αの遺伝子を欠損した影響を、遺伝子発現解析やタンパク質発現解析、組織学的解析などにより調査しました。その結果、胎盤サイズは小さくなり(図3)、血管系の発達はやや乏しく(図4)、母体から胎児への栄養輸送能は低下していることを見いだしました。胎盤は、ほ乳動物特有の器官で、妊娠中に母体と胎児の間での栄養や老廃物および酸素や二酸化炭素の交換を行っており、高度に血管系を発達させています。血管系への影響から、研究グループは血管内皮成長因子の発現も調査し、IRE1αの遺伝子欠損マウスの胎盤で、発現レベルが半減していることも明らかにしました。これらの結果から「胎盤の発達にはIRE1αが必要である」ということが分かりました。
(3)IRE1αの遺伝子条件的欠損マウスの作製と解析
IRE1αの遺伝子を、全身ではなく体の特定部位で欠損させたマウス、「IRE1αの遺伝子条件的欠損マウス」を作製しました。このマウスは、先のIRE1αの遺伝子欠損マウスを作製した技術の改良によって得ることができます。ほ乳動物の胎児は、胎盤や臍帯(さいたい;へその緒)を通じて母体とつながっており、それら胎盤や臍帯は胎児と同じように受精卵に由来するため、普通は遺伝学的に胎児と同じ特徴を持ちます。本研究では、遺伝子の条件的欠損技術を使い、胎児部分だけIRE1αの遺伝子を欠損させ、胎盤部分はIRE1αの遺伝子を維持するようにしたマウス胎児の生存率調査を行いました。その結果、このマウスは胎児期に亡くならず、通常通り妊娠から20日で誕生しました。また、このマウスの胎盤の発達状況や機能は正常でした。つまり、胎盤でのIRE1αの発現が、胎盤自体の発達とマウス胎児の生存に必要であることが明らかになりました。
今後の期待
本研究では、ほ乳動物(マウス)では妊娠時に胎盤が軽度の小胞体ストレス状態に陥り、そこではIRE1αが活性化されるということや、胎盤でのIRE1αの発現が胎盤自体の発達とマウス胎児の生存に必要であることが明らかとなりました。この結果は、生体内における小胞体ストレスの実態や、小胞体ストレス応答分子の存在意義に迫る重要な知見です。また、今回の発見がほ乳動物特有の器官である胎盤に関与しているということを踏まえると、進化学的な見地で非常に興味深い研究成果であると考えています。
現時点での研究成果はマウスの段階であり、まだヒトの治療に直結するものではありません。ただ、将来的には、妊娠中の小胞体ストレスと、流産の危険性との関連性を解明するような研究へと発展する可能性を持っており、医学的な立場から人間社会への貢献が期待できます。妊娠しても流産に至ってしまうケースは医療の発達した日本でも意外に多く10~15%(出典:厚生省心身障害研究報告)にも達するようです。また高齢出産が増え、少子化の進行などが深刻な社会において、妊娠や出産に関する研究は重要であるにもかかわらず、流産の原因はあまり分かっていません。多くの場合は胎児側の染色体異常か子宮の異常(子宮筋腫や子宮奇形)だと考えられていますが、小胞体ストレスも1つの原因かもしれません。少なくとも研究グループの予備的調査では、マウスに一定濃度の薬剤を投与し、人工的に全身へ小胞体ストレスを加えた場合、非妊娠マウスでは大きな健康被害はなく、妊娠マウスでは流産するという結果を得ています。小胞体ストレスの研究が、流産の原因を1つでも解明し、予防につなげることで、社会に大きく貢献することができると期待されます。
発表者
理化学研究所
基幹研究所 岩脇独立主幹研究ユニット
独立主幹研究員 岩脇 隆夫(いわわき たかお)
Tel: 048-467-9477 / Fax: 048-467-8503
お問い合わせ先
(JSTの事業に関すること)独立行政法人科学技術振興機構
イノベーション推進本部 研究推進部(さきがけ担当)
原口 亮治(はらぐち りょうじ)
Tel: 03-3512-3525 / Fax: 03-3222-2067
報道担当
独立行政法人理化学研究所 広報室 報道担当Tel:048-467-9272 / Fax:048-462-4715
独立行政法人科学技術振興機構 広報ポータル部
Tel: 03-5214-8404 / Fax: 03-5214-8432
補足説明
- 1.リボゾーム
細胞内にあるRNAとタンパク質からなる複合体。mRNAのコードを基にアミノ酸を連結してタンパク質を合成する場となる。 - 2.ホタルルシフェラーゼ
ホタルの発光反応を触媒する酵素。最近では、遺伝子やタンパク質の発現や活性化レベルを測定するための指標として、いろいろな生命現象の研究の場で利用されている。 - 3.XBP1メッセンジャーRNA(XBP1mRNA)
IRE1αの内在性の特異的基質の1つで、小胞体ストレス時にIRE1αによりスプライシングを受ける。細胞では、スプライシングされたXBP1メッセンジャーRNAをもとに、活性のあるXBP1タンパク質がつくられ、小胞体ストレスを軽減するための遺伝子の発現を上昇させる。 - 4.スプライシング
DNAから転写されたRNAのうち、不必要な部分が切り取られる過程のこと。この反応を経て活性のあるメッセンジャーRNAが完成する。スプライシングによって切断除去される部分をイントロン、メッセンジャーRNAになる部分をエキソンと呼ぶ。 - 5.ジーンターゲティング技術
細胞核内の標的とする遺伝子を、細胞外から導入した遺伝子と置き換える技術。
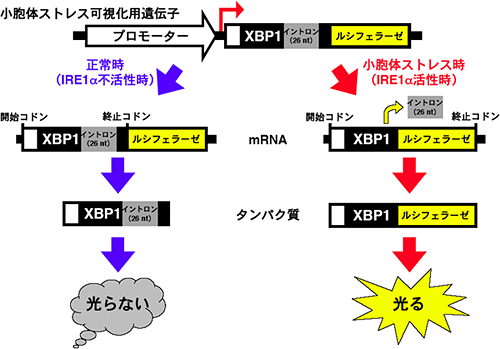
図1 小胞体ストレス可視化マウスに導入された遺伝子と作用機序の模式図
小胞体ストレス可視化用遺伝子は、XBP1とホタルルシフェラーゼの融合遺伝子、その発現を活性化するプロモーター遺伝子から成り立つ。プロモーターの働きにより、XBP1とホタルルシフェラーゼの融合遺伝子からmRNAへの合成(転写)が進む。IRE1α不活性時のmRNAから生じるタンパク質は、XBP1部分だけとなり光を発することはない。IRE1α活性時のmRNAから生じるタンパク質は、XBP1とホタルルシフェラーゼの融合型となり光を発するようになる。
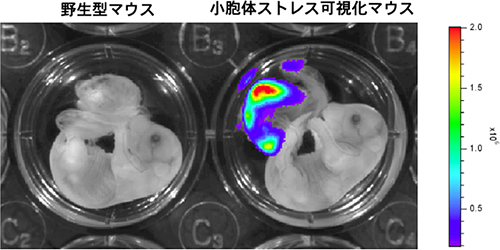
図2 小胞体ストレス可視化マウスの胎児におけるシグナル解析の結果
写真は臍帯(さいたい)および胎盤がついたままの、2匹のマウス胎児(妊娠14日目)。発光シグナルをカラーで表現している。
(左)野生型マウス。どこからも発光シグナルは検出できない。
(右)小胞体ストレス可視化用遺伝子を導入したマウス。小胞体ストレスに応答した発光シグナルを検出。胎盤から強い発光シグナルを検出した。
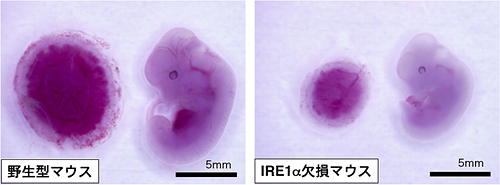
図3 野生型マウスとIRE1αを欠損させたマウスの胎盤(左側)と胎児(右側)
それぞれのマウス胎児は共に妊娠11日目の段階で、母マウスから取り出したもの。野生型マウスに比べ、IRE1αを欠損させたマウスでは胎児のサイズだけでなく、胎盤のサイズも小さくなっている。
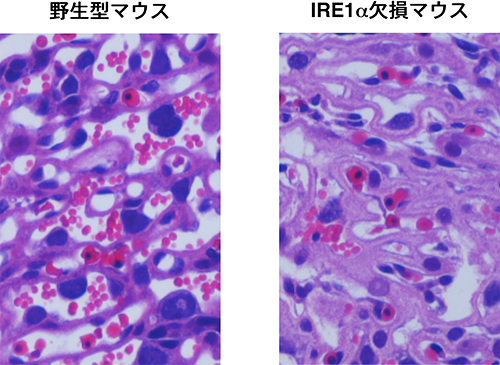
図4 野生型マウスとIRE1αを欠損させたマウスの胎盤迷路部の組織切片
胎盤迷路部は母子間のガス、栄養、および老廃物の交換を行う場所で、母親に由来する血管と胎児に由来する血管を高度に発達させる。
それぞれのマウス胎盤は、共に妊娠13日目の段階で母マウスから取り出した。
(左)正常な胎盤迷路部の組織切片写真では、赤血球が多く観察できる。
(右)IRE1α欠損マウスでは赤血球は比較的少なく、血管の発達が悪いことが分かる。
