2009年11月11日
独立行政法人 理化学研究所
内耳の神経回路形成に重要な役割を持つ膜タンパク質「SLITRK6」を発見
-新たなニューロトロフィン調節因子として機能-
ポイント
- SLITRK6欠損マウスで内耳の神経突起数の減少をキャッチ
- ニューロトロフィン欠損の内耳と同様の異常を、SLITRK6欠損マウスで確認
- 感音性難聴の発症機構の理解や治療法の改善に役立つと期待
要旨
独立行政法人理化学研究所(野依良治理事長)は、耳の最も奥にある器官で聴覚や平衡感覚の働きを担う内耳の神経回路形成に重要な役割を持つタンパク質「SLITRK6」を発見しました。理研脳科学総合研究センター(利根川進センター長)行動発達障害研究チームの有賀純チームリーダー、片山圭一研究員、仏・モンペリエ大学のエーゼル・ジン(Azel Zine)教授らによる共同研究グループの成果です。
内耳は、耳の最内部にある器官で、蝸牛、前庭・三半規管などから構成され、聴覚・平衡感覚などにかかわります。これまでに内耳の神経回路形成では、ニューロトロフィン(神経栄養物質)※1と呼ばれる分泌性タンパク質を介した情報伝達系が重要な役割を果たすことが知られていました。ニューロトロフィンやその受容体を欠損したマウスは、内耳の神経細胞が正しく突起を伸ばすことができない、細胞死を起こしてしまう、などの異常を示し、正常な神経回路を形成できません。
研究グループは、主に脳神経系に存在し、神経突起の伸展を調節する機能を持つとされている細胞膜貫通型タンパク質SLITRKファミリー※2の1つ「SLITRK6※2」を欠損するマウスを作製したところ、ニューロトロフィン欠損マウスに似た内耳の異常を観察しました。SLITRK6は、内耳の神経細胞がシナプスを作る標的である感覚上皮※3という組織に存在しています。SLITRK6欠損マウスから単離した感覚上皮細胞は、培養皿の中でも神経突起を引きつける働きが弱く、感覚上皮で産生されているニューロトロフィンの発現を調べたところ、SLITRK6欠損マウスでは内耳のニューロトロフィン発現量が低下していました。この培養皿に外部からニューロトロフィンを加えると、神経突起は正常マウスと同じ程度に伸びました。これらのことから、SLITRK6は、内耳のニューロトロフィン量を調節することで、内耳の神経回路形成に関与していることが明らかとなりました。今回の発見は、感音性難聴※4の発症機構の理解や治療法の改善に役立つものと期待されています。
本研究成果は、米国のオンライン科学雑誌『PLoS ONE』(11月11日号)に掲載されます。
背景
理研の研究グループは2002年から、遺伝子情報のコンピュータ解析を基に、脳機能に重要な遺伝子を予測し、その遺伝子産物の機能を探る研究プロジェクトを進めてきました。その成果の1つとして、6種類の細胞膜貫通型タンパク質からなるSLITRKファミリーを見いだしました。SLITRKファミリーのうち、SLITRK1~SLITRK5が脳神経全体で広く発現するのに対し、SLITRK6タンパク質だけは内耳など脳以外の組織でも発現しています。また、SLITRK1タンパク質は、米国のグループがトゥレット症候群※5との関連を指摘しており、理研の研究グループでも、SLITRK1欠損マウスで強い不安抑うつ傾向などの行動異常が認められることを報告しています。しかし、動物の発生過程におけるSLITRKファミリーの役割は、いまだ明らかになっていませんでした。
内耳は耳の最内部の器官で、聴覚にかかわる蝸牛、平衡感覚にかかわる前庭器官などが含まれています。これらの器官では、感覚上皮の中に存在している有毛細胞※6が感覚の情報を最初に受け取り、その情報を内耳の神経節※7にある神経細胞を介して脳へと伝えます。発生の過程では、感覚上皮に向かって、神経節からの神経突起が伸び、シナプスを形成することで、内耳の神経回路が形成されます。これまでの研究から、内耳の神経回路形成では、神経栄養物質ニューロトロフィンのうちBDNF※1とNTF3※1が重要な役割を持つことが知られていました。これらのニューロトロフィンやニューロトロフィン受容体※1を欠損したマウスでは、内耳の中にある神経細胞が正しく突起を伸ばすことができない、細胞死を起こしてしまう、などの異常が表れます。また、ニューロトロフィンを介した情報伝達系は内耳に限らず、神経細胞の成長、生存、シナプス伝達の調節などに多様な役割を持つことが知られています。
研究手法と成果
SLITRK6は、内耳の感覚上皮全体に存在しています。研究グループは、SLITRK6の役割を調べるために、ES細胞を用いた遺伝子相同組み換えにより、SLITRK6欠損マウスを作製し、内耳の異常を解析しました。その結果、このマウスでは、ラセン神経節※7から蝸牛の感覚上皮への神経突起の数が減少し(図1)、前庭神経節※7から前庭器官の一部である後半規管膨大部稜への投射がしばしば無くなる(図2)ことが明らかになりました。
また、SLITRK6欠損マウスのいくつかの発生段階で、ラセン神経節や前庭神経節の細胞数を測定したところ、ラセン神経節では胎仔齢16日目から、前庭神経節では13日目から細胞数が減少し始め、それらの時期と一致して細胞死の頻度が増えていることが分かりました(図3)。
次に神経突起伸展の異常が、感覚上皮細胞、神経節細胞どちらの不具合によるものなのかを調べるために、正常あるいはSLITRK6欠損マウスから切り出した感覚上皮細胞・神経節細胞を組み合わせて培養皿の中で培養しました。その結果、SLITRK6欠損マウスの感覚上皮細胞は、正常マウスの感覚上皮細胞に比べて、神経突起伸展を促進する作用が弱いことが明らかになりました(図4)。
そこで、研究グループは、神経突起伸展の異常は、感覚上皮細胞で発現する分泌性因子の減少が原因ではないかと考え、分泌性タンパク質であるニューロトロフィン(BDNF、NTF3)のメッセンジャーRNA(mRNA)量を定量しました。その結果、感覚上皮細胞におけるBDNF、NTF3の発現量はいずれも20%程度低下していることが明らかになりました。さらに、培養皿の培養液に外部からNTF3を添加し、正常およびSLITRK6欠損マウス由来のラセン神経節細胞を培養したところ、両者とも同じ程度の神経突起の伸展を示すことが分かりました(図5)。
SLITRK6欠損マウスに表れた内耳の神経回路の異常は、ニューロトロフィン欠損による異常とよく似ています(表1)。このことと感覚上皮細胞におけるニューロトロフィンの発現低下から、SLITRK6欠損マウスに表れた内耳の神経回路形成の異常の少なくとも一部は、ニューロトロフィンを介した情報伝達の低下によるものと推測できます。
今後の期待
研究グループはこれまでに、SLITRK6変異マウスが難聴傾向を示すことを見いだしています。今後、SLITRK6の分子機能調節機構を解明することができると、感音性難聴の発症機構の理解や、治療法の改善に結びつくと考え、研究を進めています。同時に、今回見いだしたSLITRK6の機能は、いまだに不明な点の多いSLITRKファミリータンパク質の機能解明の突破口になることが期待できます。
発表者
理化学研究所
脳科学総合研究センター 行動発達障害研究チーム
チームリーダー 有賀 純(あるが じゅん)
Tel: 048-467-9791 / Fax: 048-467-9792
お問い合わせ先
脳科学研究推進部 納富 さより(のうどみ さより)Tel: 048-467-9757 / Fax: 048-462-4914
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ニューロトロフィン(神経栄養物質)、BDNF、NTF3、ニューロトロフィン受容体
ほ乳類の主なニューロトロフィン(神経栄養物質)として、NGF、BDNF、NTF3、NTF4 (NTF5とも呼ばれる)が知られている。これらは中枢神経系、末梢神経系あるいはその標的組織に幅広く発現している。これらのうちBDNF、NTF3は内耳での発現が強く、BDNFは主に前庭の神経回路形成に働き、NTF3は主に蝸牛の神経回路形成に働くものと考えられている。ニューロトロフィン受容体のうちNTRK2はBDNFのシグナルを受け取り、NTRK3はNTF3のシグナルを受け取ることが知られている。BDNF欠損マウスとNTRK2欠損マウス、NTF3欠損マウスとNTRK3欠損マウスに表れた内耳の異常は、それぞれ非常によく似ている。 - 2.SLITRKファミリー、SLITRK 6
神経系に発現する新規の細胞膜貫通型タンパク質ファミリーとして、2003年理研脳科学総合研究センターの発生発達研究グループにより報告された1,2)。培養皿中ではニューロトロフィンの1つNGF がPC12細胞の突起伸展を促す過程に影響を与えることが知られていた。一個の膜貫通領域を持つタンパク質で、アミノ末端側にはロイシンリッチリピートというタンパク質-タンパク質間の結合によく用いられるドメインが2個存在し、カルボキシ末端側にはニューロトロフィン受容体と部分的に類似のアミノ酸配列が存在する。SLITRK6は脳の視床の一部、内耳の感覚上皮、舌、嗅上皮などでも発現していることが知られており3)、感覚受容に関連した機能を持つのではないかと推測されていた。
1) Aruga, J., Mikoshiba, K.: Identification and characterization of Slitrk, a novel neruonal transmembrane protein family controlling neurite outgrowth. Mol. Cell. Neurosci. 24, 117-129. (2003)
2) Aruga, J., Yokota, N., Mikoshiba, K.: Human SLITRK family genes, genomic organization and expression profiling in normal brain and brain tumor tissue. Gene 315, 87-94 (2003)
3) Aruga, J.: Slitrk6 expression profile in the mouse embryo and its relationship to that of Nlrr3. Gene Expr. Patterns 3, 727-733. (2003)
- 3.感覚上皮
外界からの刺激を受容し、さらに刺激を神経系に伝える機能を持つ上皮の組織。内耳の感覚上皮のほかに、嗅上皮や網膜なども含まれる。内耳の感覚上皮は、蝸牛ではカタツムリ型の管の中に細長い帯のような形をして1カ所に存在しており、前庭器官では卵形嚢と球形嚢にそれぞれ1つずつある斑、三半規管にそれぞれ1つずつある膨大部稜の計5カ所にある。内耳の感覚上皮には有毛細胞と支持細胞が存在している。有毛細胞と支持細胞には共通の幹細胞があり、支持細胞の幹細胞が有毛細胞に分化できることが知られている。SLITRK6は内耳の感覚上皮全体に検出されるが、新生仔では支持細胞に強く分布している。 - 4.感音性難聴
内耳もしくはそれ以降の聴覚経路に起因する難聴。感覚神経性難聴ともいう。原因としては遺伝子変異、ウイルス感染、薬物、音響外傷、加齢、聴神経腫瘍などがある。小さい音が聞こえない、話し言葉が分かりにくい、大きな音がやかましい、聞きたい音が聞きにくいなどの症状がある。最近の論文ではマウスを使った遺伝子治療の試みも報告されている1)。
1) Gubbels SP, Woessner DW, Mitchell JC, Ricci AJ, Brigande JV.: Functional auditory hair cells produced in the mammalian cochlea by in utero gene transfer. Nature 455, 537-541 (2008)
- 5.トゥレット症候群
多発性のチック(突発的、急速、反復性、非律動的、常同的な運動あるいは発声で、発症が18歳未満で4週間以上持続するもの)を主症状とする疾患で、小児期に発症し慢性化する。多動症(ADHD)や強迫性障害を合併する例もある。これまでに理研の行動発達障害研究チームでは、SLITRK1変異マウスが行動異常を示し、脳内ノルアドレナリンの分布に変化があること、トゥレット症候群の治療にも用いられるクロニジン(ノルアドレナリン作働薬)が不安様症状を改善することを報告している1,2)。
1) Katayama, K-i, Yamada, K., Ornthanalai, V. G., Inoue, T., Ota, M., Murphy, N.P., Aruga, J.: Slitrk1-deficient mice display elevated anxiety-like behavior and noradrenergic abnormalities. Mol. Psychiatry (2008) Epub ahead of print
2) トゥレット症候群関連遺伝子の機能解明 (Katayama et al., 2009)
- 6.有毛細胞
有毛細胞には特殊な繊毛が生えていて、音や頭の回転運動(角加速度)、直線運動(直線加速度)によりこの繊毛にゆがみが生じ、それが有毛細胞の中で電気信号に置き換えられる。有毛細胞は感覚上皮の中に存在している。 - 7.神経節、ラセン神経節、前庭神経節
有毛細胞でとらえられた聴覚、頭の加速度に関する感覚は、まず内耳の神経節にある神経細胞で受け取られて、中枢神経系の聴覚、平衡感覚をつかさどる領域に伝えられる。内耳の神経節は大きくラセン神経節と前庭神経節に分けられる。ラセン神経節は蝸牛の有毛細胞からの情報を受け取り、前庭神経節は前庭器官の有毛細胞からの情報を受け取る。
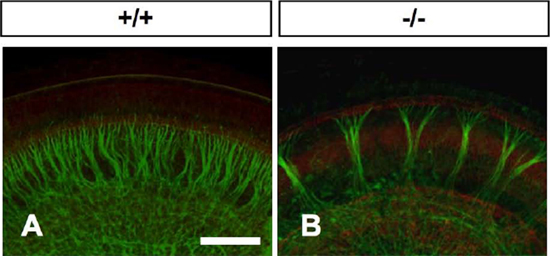
図1 胎仔齢16日目の胚でのらせん神経節からの神経突起
(緑:ニューロフィラメントに対する免疫染色)
正常マウス(+/+)に比べ、SLITRK6欠損マウス(-/-)では、ラセン神経節から蝸牛の感覚上皮への神経突起(緑)の数が減少している。
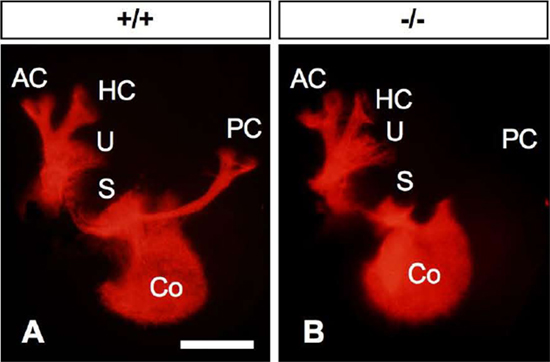
図2 胎仔齢13日目の胚での前庭神経節からの神経突起
AC:前半規管膨大部稜、Co:蝸牛、HC:水平半規管膨大部稜、U:卵形嚢、S:球形嚢
正常マウス(+/+)では、前庭神経節から後半規管膨大部稜(PC)への投射が見られるが、SLITRK6欠損マウス(-/-)では見られない。蝸牛の神経節にはこの時期、まだはっきりとした異常が現れていない。
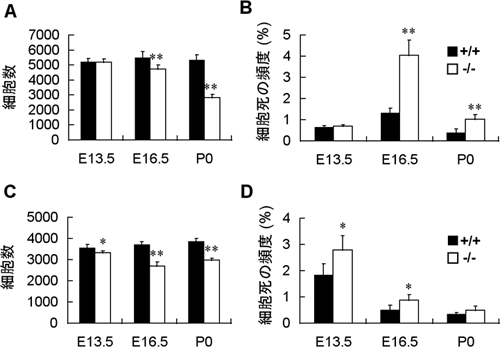
図3 正常マウス(+/+)およびSLITRK6欠損マウス(-/-)における
ラセン神経節(A, B)、前庭神経節(C,D)の細胞数(A,C)、細胞死の頻度(B,D)の比較
ラセン神経節では胎仔齢16日目(E16.5)から、前庭神経節では胎仔齢13日目(E13.5)から細胞数が減少し始め、それらの時期と一致して細胞死の頻度が増えている。これらの細胞死のタイミングはそれぞれNTF3欠損マウス、BDNF欠損マウスで見られる細胞死のタイミングと一致している。ラセン神経節では細胞数減少が出生時(P0)まで続いている。
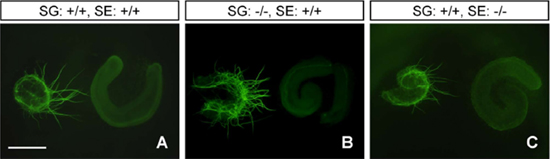
図4 正常マウス(+/+)およびSLITRK6欠損マウス(-/-)由来のラセン神経節(SG)と蝸牛感覚上皮(SE)の同時培養
SLITRK6欠損マウス由来の蝸牛感覚上皮(SE)は、ラセン神経節(SG)からの神経突起伸展を促す作用が弱い(C)。
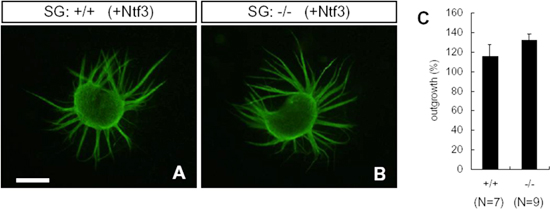
図5 正常マウス(+/+)およびSLITRK6欠損マウス(-/-)由来のラセン神経節(SG)のNTF3添加後の突起伸展
NTF3添加後は、正常マウス(+/+)とSLITRK6欠損マウス(-/-)との間で、ラセン神経節細胞の突起伸展に差は認められなかった(A, B)。神経突起の成長を神経節のサイズを基準として比較したが、有意な違いは認められなかった(C)。
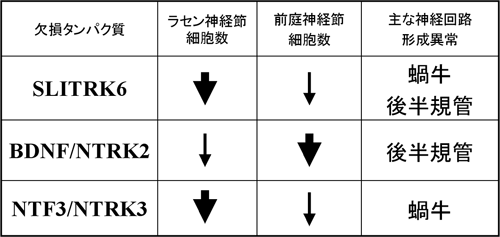
表1 SLITRK6欠損マウスと、ニューロトロフィン(BDNF、NTF3)またはその受容体(NTRK2、NTRK3)遺伝子欠損マウスに表れた内耳の異常の比較
細い矢印は弱い減少、太い矢印は強い減少を示している。SLITRK6欠損マウスに表れた異常は、BDNFまたはNTRK2欠損マウス、NTF3またはNTRK3欠損マウスに表れた異常の両方を併せ持っている。このことは、BDNFとNTF3が両方とも発現低下した結果と合致するものといえる。
