2009年12月15日
独立行政法人 理化学研究所
葉緑体タンパク質をコードする遺伝子変異体の表現型をDBで公開
-低炭素社会の構築に必須な、葉緑体機能研究のための基盤整備へ貢献-
ポイント
- 葉緑体タンパク質1つ1つの機能を欠損したシロイヌナズナをプレート上で観察
- 表現型が異常な変異体の写真や遺伝子情報をデータベースで公開
- トランスポゾンやT-DNA挿入ホモラインを作出、ストックセンターに分譲
要旨
独立行政法人理化学研究所(野依良治理事長)は、シロイヌナズナの葉緑体タンパク質※1を産生すると予想した遺伝子に、トランスポゾン※2またはT-DNA※3を挿入して破壊したタグライン※4を大規模に収集し、植物体の形態変化を育成プレート上で観察・分類した結果、異常な表現型を示した変異体の原因遺伝子の情報と写真を含むデータベースを作成し、一般公開しました。これは、理研植物科学研究センター(篠崎一雄センター長)機能開発研究グループの明賀史純研究員とゲノム情報統合化ユニットの秋山顕治技師らによる共同研究※5の成果です。
葉緑体は植物細胞の重要な細胞内小器官の1つで、炭素同化を担う光合成や窒素・硫黄同化などを担う基本代謝、さまざまな生合成など多彩な代謝機能を行っています。この極めて重要で複雑な葉緑体機能を調べるために、豊富なゲノム情報や代謝情報を集積したデータベースの活用と、完全長cDNAや突然変異体などの解析用材料基盤の利用は必要不可欠です。
研究グループは、これまでにいくつかの国際的な研究機関が作製したシロイヌナズナ突然変異体の中から、葉緑体に移行すると予想されるタンパク質を産生する核内の遺伝子の1つ1つに、トランスポゾンやT-DNAを挿入したタグラインを大規模に収集し、それらのタグがホモの状態で挿入して遺伝子の機能が欠損した植物体※6を単離しました。これらの植物体を育成プレート上で網羅的に観察し、目に見える変異が生じた植物体を写真で撮影し、変異体出現率や表現型情報を取得しました。その結果、「野生型の芽生えの表現型を示すホモ挿入体」1,290ライン、「ホモ挿入体が異常な芽生えの表現形を示す変異体」111ライン、「ホモ挿入体が得られなかった変異体」122ラインを単離しました。これらの遺伝子や表現型情報などの詳細をデータベースにまとめ、ウェブ上で自由に閲覧・検索可能にしました。
今回の研究は、核内の遺伝子から産生する葉緑体タンパク質の遺伝子型と表現型とを結びつけるもので、シロイヌナズナ遺伝子の機能解析への網羅的アプローチのために欠かせません。今後、遺伝子機能のさらなる解析のために、変異体を選択する上で有益なリソースとなります。葉緑体機能の理解は、CO2固定、物質生産、食料生産の基礎をなす植物機能の解明につながるため、今回作成したデータベースは、低炭素社会の構築へ向けた植物研究に大きく貢献すると期待できます。
本研究成果は、英国の科学雑誌『The Plant Journal』オンライン版に近く掲載され、データベースは、ウェブサイト(英語のみ)で公開しています。
背景
葉緑体は、光合成※7を行う独立した生物である「ラン藻※8」の祖先が、太古に植物の祖先の細胞に取り込まれて生まれたと考えられており、その証拠に、現在でも独自のゲノムを保持しています。しかし、ラン藻由来の大部分の遺伝子は、進化の過程で宿主細胞の核に移動しています。そのため葉緑体を形作るタンパク質(葉緑体タンパク質)の多くが核ゲノムにコードされており、細胞質で合成された後、葉緑体内へ輸送されます。一部の例外を除いて、葉緑体タンパク質のN末端には、葉緑体に運ばれるために必要な数十アミノ酸からなる「トランジットペプチド」を含んでいます。このトランジットペプチドには特定の定まった配列はありませんが、既に、その存在の有無を予測するコンピュータープログラムが複数作成されています。個々のプログラムを用いた場合、シロイヌナズナ全ゲノム中にはトランジットペプチドを持つ葉緑体タンパク質の予測数は、3,000~5,000個程度と予想されます。これらのプログラムを組み合わせてより正確性を高めた場合、最小数の2,090個の葉緑体タンパク質※9に絞り込むことができます。この数は、やや控え目な数ですが、研究グループが今回行った葉緑体タンパク質の変異体の大規模収集のための第一歩となります。
双子葉植物のモデル植物であるシロイヌナズナは、全ゲノム配列の解読が終了した最初の植物体で、遺伝子の機能研究を行うための国際的な基盤材料が整備されつつあります。特に遺伝子にトランスポゾンやT-DNAを挿入したタグラインの整備は、さまざまな国際的な研究機関が進めており、現在ではシロイヌナズナの全ゲノムにある約26,000個の遺伝子の1つ1つについて、そのタグラインをほぼ取得することが可能となっています。しかし、これらのタグラインの多くは、2本(一対)の染色体の1本だけにタグが挿入した植物体(ヘテロ挿入体)であるため、1本の染色体上の遺伝子の機能を欠損しても、ほかの1本の染色体上の遺伝子が機能します。そのため、一見すると野生型と変わらないように見えます。そこで本研究では、2本の染色体の両方にタグを挿入して、遺伝子の機能を欠損した植物体(ホモ挿入体)の作出を行いました。
研究手法と成果
研究チームは、葉緑体タンパク質をコードすると予想した遺伝子に、トランスポゾンやT-DNAを挿入した3,246ライン(6種類)のタグラインを、米国・英国・日本の国際的な種子ストックセンター※10から入手しました。そのうち、既にほかの研究機関がホモ挿入体の収集を行っているSALKライン※11の一部を除いた1,722ラインを対象に、ホモ挿入体の収集と表現型データを調べました。
ホモ挿入体の収集方法は、トランスポゾンのタグラインとT-DNAのタグラインとで異なる手法をとりました。トランスポゾンタグラインでは、トランスポゾンの挿入部位は理論上1本の染色体あたり1つであるため、トランスポゾンの内部にコードされているマーカー遺伝子※12を利用した遺伝解析(発芽率検定)を行うと、ホモ挿入体を確認することが可能です。一方、T-DNAタグラインでは、T-DNAの挿入部は複数の場合があるため、目的の遺伝子内にT-DNAが挿入していることを、PCRによるジェノタイピング※13で確認しました。具体的には、1,722ラインのホモ挿入対の有無を育成プレート上で育て、トランスポゾンライン1,107ラインそれぞれについて3世代(合計17個体)、T-DNAタグライン615ラインそれぞれについて最低2世代(合計16個体)を用いて調べました。その結果、4分の3を占める1,290ラインのタグラインから「野生型の芽生えの表現型を示すホモ挿入体」を単離することができました。しかし、「ホモ挿入体が得られなかった変異体」が122ライン(91遺伝子)ありました(表1)。この一部の鞘の内部を観察したところ、初期の種子形成時に異常が見つかりました(図1)。つまり、「ホモ挿入体が得られなかった変異体」122ラインは、致死変異体であると考えられます。
また、「ホモ挿入体が異常な芽生えの表現形を示す変異体」111ライン(76遺伝子)の特徴を目視で観察し、白色32ライン(21遺伝子)・薄緑色35ライン(24遺伝子)・斑入り7ライン(5遺伝子)・形態異常28ライン(21遺伝子)の4つに分類・単離し、分類できなかった19ライン(5遺伝子)と区別しました(図2)。
これらタグラインの遺伝子情報や表現型情報は、検索が可能な形式でデータベースを整備し、公開しました(図3)。このデータベースには、遺伝子情報だけではなく、変異体の表現型写真や発芽率など多くの情報を提供しています。さらに、ウェブを通して変異体コレクションの詳細な情報はもとより、AGIコード※14、変異体ライン番号、表現型によって検索が可能です。また、1つの変異体に対して複数の写真画像データを閲覧することができるため、明確に分類できず、研究者の主観的な言葉の表現に頼らざるをえない表現型でも、実際に見て比較することができます。
今後の期待
研究チームは、シロイヌナズナのタグラインから多数のホモ挿入体を収集しました。これらホモ挿入体のタグライン※15は、葉緑体機能に異常があるものの目視では野生型と区別できない変異体を検索するための有益なリソースです。例えば、顕微鏡観察で分かる葉緑体の数や大きさが異なる変異体、測定機器の使用で分かる光合成が異常な変異体、または生物学的または生化学的測定で分かるストレス応答関連の変異体を同定することができる可能性があります。
また、データベースに含めた「ホモ挿入体が異常な芽生えの表現形を示す変異体」や「ホモ挿入体が得られなかった変異体」の情報は、葉緑体機能のさらなる解析のために、変異体を選択する上で有益な情報を提供することになります。今後、なぜその遺伝子が働かなくなることでさまざまな形態変化が起きるのか、というメカニズムを各遺伝子について詳細に調べることで、葉緑体の機能研究の進展が期待できます。
葉緑体の機能研究は、光合成によるCO2固定、物質生産、食料生産の基本的な機能の解読につながります。本データベースを利用した葉緑体研究は、低炭素社会の構築に貢献する植物研究への展開が期待できます。
発表者
理化学研究所
植物科学研究センター センター長
機能開発研究グループ グループディレクター
篠崎 一雄(しのざき かずお)
Tel: 045-503-9579 / Fax: 045-503-9580
機能開発研究グループ 研究員
明賀 史純(みょうが ふみよし)
Tel: 045-503-9625 / Fax: 045-503-9584
お問い合わせ先
横浜研究推進部 企画課Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.葉緑体タンパク質
葉緑体を形成したり、葉緑体が機能するために必要なタンパク質のこと。これらのタンパク質の多くは遺伝子が細胞の核にコードされており、細胞質で作られたのち葉緑体に輸送される。シロイヌナズナゲノムには約3,000~5,000のタンパク質が葉緑体に輸送されていると考えられている。これにより葉緑体は正常に機能することができる。 - 2.トランスポゾン
特定の塩基配列を持ちゲノム上を動くDNA断片。転移因子とも呼ばれる。国際的なシロイヌナズナ研究基盤整備プロジェクトでは、シロイヌナズナゲノム中の異なる位置にトウモロコシのDsまたはSpmと呼ばれるトランスポゾンを挿入した植物体が多数作出されている。また、トランスポゾンが挿入した部位近傍の配列情報から挿入位置をまとめたデータベースも作成されている。これらのシロイヌナズナの種子は、国際ストックセンターに保存されており、利用可能となっている。 - 3.T-DNA
アグロバクテリウム( A. tumefaciens)は、多くの双子葉植物および一部の裸子植物・単子葉植物にクラウンゴールと呼ぶコブ様の腫瘍を起こす。この菌はTiプラスミド(pTi)と呼ばれる巨大なプラスミドを有しており、その一部であるT-DNA(transfer DNA)と呼ばれるDNA断片を植物細胞に注入し、T-DNAは相同組換えにより植物細胞のゲノムにランダムに挿入される。これを利用して、シロイヌナズナゲノム中の異なる位置にT-DNAが挿入したものが多数作出され、ライン化されている。 - 4.タグライン
トランスポゾンやT-DNAがゲノム内にランダムに挿入した変異体系統群のこと。トランスポゾンやT-DNAが遺伝子内または遺伝子近傍に挿入した場合には、遺伝子が機能できなくなり、遺伝子突然変異体となる。シロイヌナズナではこれまでに、ほぼすべての遺伝子内にトランスポゾンやT-DNAが挿入した突然変異体が作出されている。 - 5.共同研究
理研植物科学研究センター機能開発グループ(篠崎一雄グループディレクター、明賀史純研究員、黒森崇研究員、飯泉治子テクニカルスタッフ、流水利恵テクニカルスタッフ)、ゲノム情報統合化ユニット(櫻井哲也ユニットリーダー、秋山顕治技師)、静岡大学(本橋令子準教授)、理研基幹研究所ケミカルバイオロジー研究基盤施設(伊藤卓也専任研究員)との日本国内の共同研究による。 - 6.ホモの状態で挿入して遺伝子の機能が欠損した植物体
シロイヌナズナは2倍体であり、同じ大きさで同じ形をした染色体(相同染色体)が2本ずつ対で存在する。そのため、1本の遺伝子上だけにタグを挿入(ヘテロ挿入体)した場合には、もう1本の染色体上の遺伝子の働きにより機能は維持される。一方、相同染色体の両方にタグを挿入して、遺伝子の機能を欠損した植物体(ホモ挿入体)の場合は、遺伝子の機能を失うことになる。 - 7.光合成
植物が行う反応で、光エネルギーから変換した化学エネルギーを使って、水と空気中の二酸化炭素から炭水化物(ショ糖やグルコースやデンプンなどの糖類)と酸素を合成する反応。緑色植物ではこの反応は葉緑体で行われる。 - 8.ラン藻
シアノバクテリアとも呼ばれる植物と同じタイプの酸素発生型光合成を行う原核生物で、太古の地球に出現・繁殖し、それまでの嫌気的な大気を現在に近い酸素を豊富に含む好気的大気に変えたと考えられている。今から10~20億年前に、ほかの細胞との内部共生によって現在の葉緑体の祖先となったと考えられており、原核生物から植物に至る光合成の進化を考える上で重要な生物である。 - 9.2,090個の葉緑体タンパク質
この予測数は、4つの予測プログラム(iPSORT, PCLR, Predotar, TargetP)のうち、少なくとも3つが葉緑体に移行すると判定した場合に葉緑体タンパク質としたものである。Richly, E and Leiser D(2004)の論文を参照した。しかし、この予測数は控えめな数であり、多くのほかの論文では3,000個程度が葉緑体を構成するタンパク質であるといわれる。 - 10.種子ストックセンター
モデル植物であるシロイヌナズナでは、有償ではあるが少額で種子などの遺伝子材料を提供する国際的な種子ストックセンターが存在している。本研究では、日本の理研バイオリソースセンター(RIKEN BRC)、米国のオハイオ州立大学のシロイヌナズナリソースセンター(ABRC)とコールドスプリングハーバー研究所(CSHL)、英国のノッティンガムシロイヌナズナストックセンター(NASC)からタグラインを分与された。 - 11.SALKライン
米国・カリフォルニア州にあるソーク研究所が作出したT-DNAタグラインのこと。現在、ストックセンターを通して種子を提供しているタグラインの中で最も多い13万ライン以上のラインを作出している。T-DNAの挿入位置の情報は T-DNA Expressから検索可能である。 - 12.マーカー遺伝子
シロイヌナズナゲノム中にトランスポゾンやT-DNAが挿入していることを確認するために、トランスポゾンやT-DNAの配列の内部に導入した抗生物質耐性遺伝子や除草剤耐性遺伝子などを指す。抗生物質や除草剤を加えた育成培地で発芽試験を行うと、選択マーカーを含むトランスポゾンやT-DNAを持つ耐性の植物体と持たない非耐性の植物体が判別可能である。 - 13.ジェノタイピング
植物体の遺伝子型を調べること。本研究の場合には、T-DNA挿入個所の近接配列に設計したプライマーを用いてPCR解析を行い、それぞれの植物個体がホモにT-DNAを持つのか、ヘテロにT-DNAを持つのか、あるいはT-DNAを持たないのかを明らかにした。 - 14.AGIコード
Arabidopsis Genome Initiative コード遺伝子のこと。シロイヌナズナの個々の遺伝子についているIDナンバーと同じ役割を持ち、これによりシロイヌナズナの遺伝子情報が統合されており、研究の推進に役に立っている。 - 15.ホモ挿入体のタグライン
一部のラインについては既にホモ挿入体の種子を 理研バイオリソースセンターへ寄託し、一般でも入手することが可能。

表1 トランスポゾンまたはT-DNAタグラインの表現型解析
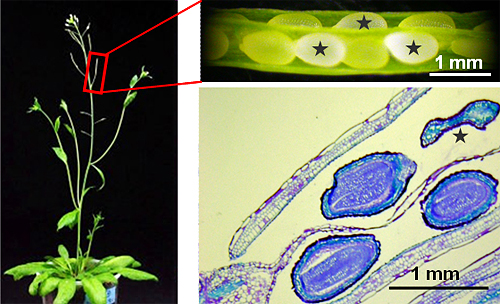
図1 ホモ挿入体が得られなかった植物体の鞘中の異常な種子の写真
自家受粉させたヘテロ挿入体の鞘中の成熟期の種子を観察したところ、野生型と比べて異常な種子の出現率が高いことが分かった。
右上:異常な種子は白または茶色になる(★)。
右下:0.1%トルイジンブルー液による染色写真。

図2 野生型と変異体の表現型の分類
野生型植物体と4種類の変異体の発芽後3週間育てた芽生えの写真。ホモ挿入体を収集している間に目視で観察し、さまざまな表現型を示す変異体を得た。本研究では、これらの変異体を4つの表現型に分類し、データベースに掲載した。
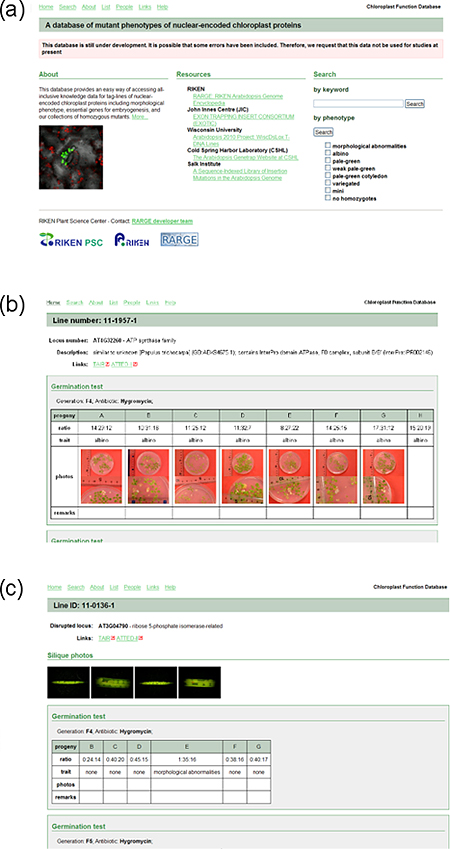
図3 The Chloroplast Function Database
(a)トップページ
(b)表現型が異常な変異体の一例
(c)ホモ挿入体が得られなかった変異体の一例
