ポイント
- 溶液反応を超高速光電子分光でリアルタイムに追跡することに初めて成功
- 水、重水の中の電子の溶媒和安定化エネルギーを、それぞれ3.27eV、3.20eVと決定
- 溶液中の電子の様子を追跡し、溶媒効果の本質を探る実験手法を確立
要旨
独立行政法人理化学研究所(野依良治理事長)は、ヨウ化ナトリウム(NaI)の水溶液の液体ビーム※1とピコ秒(1ピコ秒は1兆分の1秒)レベルの超高速分光機能を持った時間分解光電子分光※2を使った新しい実験手法を開発して、これまで直接観測ができなかった水の中の電子(水和電子※3)の安定化エネルギー※4を3.27eV、重水※5の中の電子の安定化エネルギーを3.20eVと決定し、このエネルギーの値をめぐる長年の論争を決着させました。これは、理研基幹研究所(玉尾皓平所長)鈴木化学反応研究室の鈴木俊法主任研究員らの成果です。
19世紀以来、液体のアンモニア中にナトリウムなどのアルカリ金属を溶解させると青い色を発色することから、溶液の中に電子が放出して安定化した「溶媒和※6電子」の存在が知られていました。特に、水の中で安定化した電子は水和電子と呼ばれ、水溶液中での電子移動反応や放射線による化学反応に重要な役割を果たしています。しかし、水和電子の安定化エネルギーは実験的観測が極めて困難で、長く手つかずのまま、その値は議論の対象となっていました。
水和電子のエネルギーを正確に測定するためには、水溶液から電子を真空に放出させ、その運動エネルギーを測定する光電子分光が必要です。しかし、電子の放出は高真空中で行う必要がある一方、水の蒸気圧が高いため、液体表面からの水蒸気の揮発量が多く、高真空を保つことは非常に困難でした。さらに、水和電子は反応性が高く、寿命が短いため、水和電子を生成し、直ちに分析する超高速分光が必要でした。
研究グループは、ヨウ化ナトリウム(NaI)の水溶液を細いガラス菅(内径25μm)から滑らかな液体流にして真空中に射出し、溶液中に溶けているヨウ素原子の負イオン(I-)に、深紫外フェムト秒レーザー光※7(波長226nm:1nmは10億分の1m)を照射しました。ヨウ素イオンは、電子を緩やかに水中に放出し、ヨウ素原子と水和電子が隣り合わせに弱く結合した状態となり、やがて両者は離れて行くことが分かりました。その後、第2のフェムト秒レーザー光(波長274nm)を水中の水和電子に照射し、真空に放出した電子の運動エネルギーを分析しました。第2のレーザー光の照射エネルギーを低く抑えることで、水中を走る電子の運動エネルギーを抑制し、電子と水分子の間の非弾性散乱※8が起こりにくいように工夫しました。さらに、水和電子が水溶液表面のものではなく、水中(バルク)に溶け込んでいるものであることも確認し、電子の安定化エネルギーを水中の場合が3.27eV、重水中の場合が3.20eVと決定しました。
本手法は、水と電子の基本的な相互作用を明らかにしただけでなく、化学反応の担い手である電子を溶液中の分子から直接観測したもので、複雑な溶液化学反応の本質を電子運動の観点から解明する新たな突破口を開くことになりました。今後、生命科学の基礎過程の解明にも役立つと期待されます。
本研究成果は、英国王立化学会の科学雑誌『Physical Chemistry Chemical Physics』オンライン版(3月11日付け)に掲載されました。
背景
極性(電気的な偏り)を持つ溶媒中に注入された電子は、周りの溶媒分子の極性を配向させて安定化します。19世紀、アンモニアに溶解したアルカリ金属が青い色を発色することが発見されましたが、この現象は、アンモニア(溶媒)中に溶け込んだ電子(溶媒和電子)の光吸収によるものと分かっています。一方、水中の溶媒和電子は、水和電子と呼びます。これら溶媒和電子や水和電子という言葉は、電子そのものだけでなく、電子の周りに配向している溶媒の集団(クラスター)を含む全体を指します。1個の水分子は、これだけでは余分な電子をつなぎ止める能力がありませんが、集団となった水分子は、電子を取り囲んで安定化します。具体的には、電子の最近接距離にある6個の水分子(H2O)が、それぞれが持つ1個のOH結合の水素原子(H)を電子の雲に突き出す形をとることで安定した集団を形成し、さらにこの集団をほかの水分子が二重、三重に取り巻きます(図1)。しかし、真空中に自由に存在する電子と、水中に閉じ込められた電子のエネルギーの差(安定化エネルギー)については、実験値が得られておらず、信頼できる結果が待たれていました。
水和電子は、水という最も基本的な液体の中に、電子という最も基本的な素粒子が捉えられた(結合した)状態にあります。そして、生体や水溶液中の電子移動反応や、放射線による遺伝子の損傷など、さまざまな化学反応で重要な役割を果たしています。このように重要な役割を担っているにもかかわらず、これまで水和電子の安定化エネルギーを測定することは非常に困難でした。測定には、水溶液から直接電子を高真空中へ放出させて、その運動エネルギーを分析することが必要ですが、水は蒸気圧が高く揮発量が多いため、電子分析装置の高真空状態を妨げる原因となっていました。また、水和電子は、反応性が高く短寿命であるため、そのエネルギーを測定するためにはピコ秒レベルの超高速分光が必要でした。
これまでは、水分子が数十個から数百個凝集した水分子クラスターを特殊な方法で作り、このクラスターに電子を捕獲させて安定化エネルギーを測定した後、それらのエネルギーを無限大の大きさの水クラスターに外挿して水和電子の安定化エネルギーを推測していました(図2点線)。しかし、1990年にこの推測値が発表されて以降、量子化学計算、分子動力学計算、さらにクラスターの赤外分光によって、これらの水クラスターでは、電子がクラスター内部に存在しているのではなく、クラスター表面の水酸基(OH)に付着していることが分かってきました。しかも、クラスターには大きく分けて構造異性体※9が3種類も存在し、その内の1つの構造異性体は、さらに2つに分類されることも分かり、水和電子の安定化エネルギーの値に関する議論は混迷を極めていました。
研究手法と成果
研究グループは、内径25μmのガラスキャピラリー(菅)から、ヨウ化ナトリウム(NaI)の水溶液を細いビーム状にして噴出し、真空内に導入しました。高真空を保つため、分析機器には射出した液体を受け止めて瞬時に凍らせる仕組みや、特殊な排気システムを導入して、液体ビームの時間分解光電子分光を実現しました。液体ビームに対して、波長が226nm、パルス幅が0.25ピコ秒の第1のレーザー光パルスを照射し、水溶液中のヨウ素イオンを励起電子状態に変化させました。励起状態のヨウ素イオンは不安定で、約0.2ピコ秒後に電子がヨウ素原子から離れ、中性のヨウ素原子と電子が隣合わせに分布する状態(接触状態)となり、その0.6ピコ秒後にはさらに安定な中間体(接触対状態)が生成しました。この中間体は、20ピコ秒程度の間に徐々に解離・拡散し、100ピコ秒以上経過した後では、水和電子とヨウ素原子が分離した状態となりました。このような時間変化は、第1のレーザー光パルス後、さまざまなタイミングで第2のレーザー光パルス(波長260~274nm、パルス幅0.1ピコ秒)を水溶液に照射して観測する手法により解明することができました。
最後に、100~400ピコ秒の時間が経った後に、第2のレーザー光パルスで液体から電子を放出させ、電子の運動エネルギーを分析し、水和電子の安定化エネルギーを測定しました。この実験では、溶液中で水分子が捕捉している電子を第2のレーザー光パルスで解放しますが、電子は厚い溶液の層を通り抜けて真空に飛び出す必要があります。その過程で電子が運動エネルギーを失ってしまうと、正しいエネルギー測定ができません。研究グループは、電子が溶媒分子(水)と衝突してエネルギーを失う過程(非弾性散乱)を可能な限り抑えるために、第2のレーザー光パルスの照射エネルギーを低く抑えることで、水中を走る電子の運動エネルギーを4eV以下となるように制御しました。水分子の電子を励起するために必要なエネルギーは5eV以上であるため、4eV以下の運動エネルギーでは周りの水分子の相互作用は小さくなります。
その結果、測定した水和電子の安定化エネルギーは、水(H2O)中で3.27eV、さらに重水(D2O)中で3.20eVと求めることができました(図2)。H2OとD2Oを比較すると、D2Oの電子の安定化エネルギー値の方がわずかに低いことが初めて分かりました。この差は、最もエネルギーの低い状態でも分子は振動しているという「ゼロ点振動」のために、重量の重いD2Oの方がH2Oよりも水素結合※10が強いことと対応します。こうしてH2OとD2Oで得た結果を比較することで、水和電子の溶媒和構造を解明する手がかりをつかむことができるようになりました。
さらに、こうした高い時間分解能を持つ測定を0ピコ秒から400ピコ秒まで通して行うことで、観測している電子がクラスター表面に付着しているものではなく、クラスター内部に溶け込んでいるものであることも確認しました。
今後の期待
孤立した分子であっても、溶液中であっても、化学反応は電子運動が重要な役割を果たします。特に溶液中では、1個の分子が持つ電子の運動が周りの溶媒によって影響を受け、それが多種多様な化学反応の溶媒効果となって表れます。溶媒は、溶液化学を制御するために化学者が古くから用いる道具の1つです。今回開発した手法は、溶液中の電子状態をリアルタイムに追跡できるため、溶媒効果の本質を物理学的に明らかにすることが可能になります。さらに、ほかの実験手法で得られる相補的な情報を統合して、より現実の世界の溶液化学の姿を描き出すことができると考えられます。その先には、水が重要な役割を担う生命化学反応の素過程解明へと発展することが期待できます。
発表者
理化学研究所
基幹研究所 鈴木化学反応研究室
主任研究員 鈴木 俊法(すずき としのり)
Tel: 048-467-1411 / Fax: 048-467-1403
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.液体ビーム
直径が5~25μmの液体の細い流れ。水道の蛇口から出た水を見ると、始めは滑らかに見える流れでも、下流では流れに乱れがあるため分裂する。乱れのほとんど無い滑らかな流れを層流、乱れが大きいものを乱流と呼び、液体ビームとは、十分に細く長い管から液体を押し出した層流である。 - 2.時間分解光電子分光
分子の中の電子を光で放出させ、その電子の運動エネルギーを分析する実験法を光電子分光と呼ぶ。さらに、レーザー光パルスを2つ使い、第1のレーザー光で分子に化学反応を起こさせ、時間差をおいた第2のレーザー光で電子を放出させることで、分子内の電子の運動のスナップショットをとる手法を時間分解光電子分光と呼ぶ。レーザー技術の発展により、レーザーの時間幅は、1980年代から今日に至るまで急速に短くなり、時間分解光電子分光の時間分解能は20フェムト秒(1フェムト秒は10の15乗分の1秒)に達している。 - 3.水和電子
水中で溶媒和された電子を中心として、その周りに配向した水分子の集団全体を指す。電子の最も近傍には6個の水分子が上下、左右、前後の6方向からOH結合の水素原子(H)を電子に向けて、電子のエネルギーを安定化する。これらの水分子は電子との相互作用によって、水分子内部の振動周波数が低下することが分かっている。 - 4.安定化エネルギー
真空中に自由に存在する電子と、水中に閉じ込められた電子のエネルギーの差。 - 5.重水
水が水素2つと酸素1つで構成されているのに対し、重水は重水素2つと酸素1つで構成されている。重水素は水素の同位元素の1つで、水素の原子核が陽子1つなのに対し、重水素は陽子1つと中性子1つから構成されている。 - 6.溶媒和
液体の中に分子が溶け込んでいるとき、液体を溶媒、分子を溶質と呼ぶ。この時、溶質の周りには溶媒分子が集まって、異分子である溶質を含めた全体のエネルギーが最も安定になる。このような集合状態を溶媒和と呼ぶ。 - 7.深紫外フェムト秒レーザー光
深紫外の光とは波長範囲において200~300nmのものを指す。フェムト秒レーザーの光源は800nmの光を発生するが、特殊な結晶(非線形結晶)に照射することで波長が短く、エネルギーの高い光を発生させている。 - 8.非弾性散乱
衝突の前後で反応系の内部のエネルギーが変化する散乱を非弾性散乱と呼ぶ。電子が水溶液中で水分子との間に起こす非弾性散乱の確率は、電子の運動エネルギーに依存する。 - 9.構造異性体
分子式が同じで構造が異なる化合物を互いに構造異性体という。 - 10.水素結合
分子間で水素原子をはさんで電気的な引力が働くときに生じる結合を水素結合という。化合物の沸点、水に対する溶解度などの物性を決める上で重要な働きをしており、その有無で化合物の特性が大きく異なる。
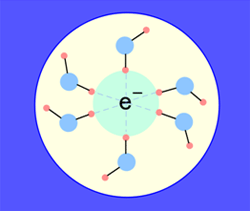
図1 水和電子の構造
平均的な構造は水分子が6つ配位した形を取り、その周囲を第二、第三の溶媒和圏が取り囲んでいるが、各瞬間で見るとこのような対称性は崩れている。
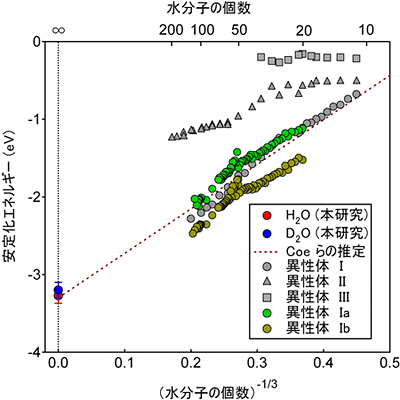
図2 決定した水和電子のエネルギーと過去の水分子クラスター(H2O)nの値の比較
左端(水分子の個数=∞)にある2つの点が本研究の結果。点線は、1990年に米国ジョンズホプキンス大学のジェームズ・コーらが報告した水分子クラスターの実測値をもとに外挿した直線。現在では、より詳細な実験により、水分子クラスター内部にある水和電子の安定化エネルギーのデータ値はこの直線上には存在しないことが分かっている。今回の測定結果から、外挿した直線から得られる安定化エネルギーの推測値だけは、偶然に実測値にほぼ等しかったことが分かる。
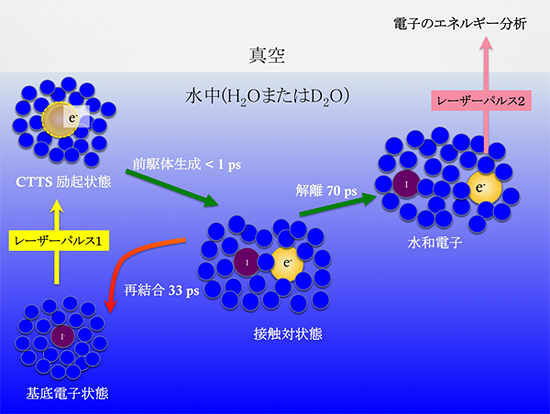
図3 NaI水溶液を用いた実験の概念図 (オレンジ:電子の分布、紫:ヨウ素原子、青:水分子)
基底電子状態のヨウ素イオンに第1のレーザー光パルスを照射し、ヨウ素イオンを励起状態にする。この状態は不安定で、約0.2 ピコ秒後に電子がヨウ素原子から離れ、中性のヨウ素原子と電子が隣合わせに分布する状態(接触状態)となり、その0.6ピコ秒後にはさらに安定な中間体(接触対状態)が生成する。この中間体は、20ピコ秒程度の間に徐々に解離・拡散し、100ピコ秒以上経過後では、水和電子とヨウ素原子が分離した状態となる。その後、第2のレーザー光パルスを照射して水和電子の安定化エネルギーを測定した。
