2010年4月19日
独立行政法人 理化学研究所
生きた細胞を簡便に数分程度の化学反応で蛍光標識することに成功
-高速6π-アザ電子環状反応を活用し、蛍光物質などで簡便に細胞を標識化-
ポイント
- 生きた細胞の表面へ、極低濃度の蛍光物質をたった10分で簡単標識
- 標識したリンパ球のマウス生体内での正常な動きを鮮明に可視化
- 標識物質を工夫し、がんなどの検出技術への応用が期待
要旨
独立行政法人理化学研究所(野依良治理事長)は、有機合成反応の1つである「高速6π-アザ電子環状反応※1」を活用し、10分という短時間で、簡便に、生きた細胞の表面を極低濃度のTAMRA(蛍光波長580nm、オレンジ色)やCy5(蛍光波長670nm、赤色)などの蛍光物質で標識する技術を開発しました。さらに、標識したリンパ球が、生体内で正常なホーミング※2をしている様子を可視化することに成功し、標識したリンパ球が正常な機能を保っていることを証明しました。国立大学法人大阪大学大学院理学研究科天然物有機化学研究室(深瀬浩一教授)の田中克典助教、キシダ化学株式会社(大阪市中央区本町橋、岸田充弘代表取締役)の小山幸一研究員と分子イメージング科学研究センター(渡辺恭良センター長)分子プローブ機能評価研究チーム(尾上浩隆チームリーダー)田原強研究員、分子プローブ動態応用研究チーム(渡辺恭良チームリーダー)野崎聡研究員との共同研究による成果です。
研究グループは、1998年に関西学院大学の勝村成雄教授と大学院生の田中らが発見した高速6π-アザ電子環状反応を活用し、ラットの培養細胞に10-8M(モル)という低濃度の蛍光プローブを37℃で10分間作用させました。その結果、細胞にダメージを与えることなく、細胞表面を選択的に蛍光標識することに世界で初めて成功しました。さらに、この新たな細胞標識法を用いて、マウスから取り出したリンパ球を試験管内で蛍光標識し、マウスに投与すると、リンパ節や脾(ひ)臓などリンパ球が集積する体内組織に、標識したリンパ球が集まる様子を蛍光イメージングで観察することができました。
今回開発した細胞標識法は、たった10分程度の短時間の化学反応で簡便に標識できるだけでなく、蛍光物質以外のさまざまな物質でも細胞を標識することができます。この方法により、標識細胞の生体内での動きを観察できるようになるだけでなく、人工的に細胞の持つ機能を広げることが可能となり、生物学や基礎医学、さらには臨床医学に対しても幅広く応用できると期待されます。
本研究成果は、ドイツの科学雑誌『ChemMedChem』オンライン版に近日掲載予定です。
背景
1998年、関西学院大学の勝村成雄教授と大学院生の田中らが、海産天然物誘導体のホスホリパーゼA2酵素の機能を非可逆的に阻害する機構として、リジン残基との間で素早い「6π-アザ電子環状反応」が関与していることを発見しました。研究グループはこの新規反応の発見を基に、すでにペプチドやタンパク質への標識分子として使用されている各種金属の配位子「DOTA※3標識プローブ」を改良して、生体高分子のソマトスタチンを[68Ga]- DOTAで標識し、膵臓に存在するソマトスタチン受容体を効率良くPET(陽電子放射断層画像撮影法)※4イメージングすることに成功しています(Angew. Chem. Int. Ed., 2008, 47, 102-105)。近年の細胞工学技術の発展で、細胞の機能を人為的に改変することが可能となり、機能を改変した細胞の生体内での動きを観察して、正常な細胞の本来の機能を明らかにする研究が活発化してきています。その観察方法には、一般的には蛍光タンパク質や蛍光分子、蛍光量子ドットなどの蛍光標識が広く用いられています。しかし、蛍光標識を用いる手法では、蛍光を発する細胞を準備するまでに、多くの時間と労力を要するという問題点があります。研究グループはこれまで、蛍光物質に限らずさまざまな標識物質に適用でき、さらに、短時間で簡便に細胞を標識する技術の開発に取り組んできました。今回、既存の蛍光標識法を基に、細胞表面で温和な条件の下、極低濃度、数分という短時間で化学的に共有結合を起こす標識技術の開発に挑みました。
研究手法と成果
研究グループは、これまでのスクシンイミジルエステル化合物※5などによる標識法とは異なり、ヘキサトリエン-β-カルボニル化合物※6の高速6π-アザ電子環状反応を活用して、低濃度の蛍光プローブを、短時間で素早く、しかも100%の収率で、タンパク質のリジン残基に標識する方法を新たに開発しました(図1)。具体的には、ラット由来の脳腫瘍細胞に対して10-8M(モル)の蛍光分子TAMRA(蛍光波長580nm、オレンジ色)を37℃で10分間作用させ、ほぼ100%の細胞を標識することに成功しました。この方法では、マイクロチューブ内で簡単に調製できる標識プローブの溶液を、浮遊状態、または接着した生細胞に対して、緩衝溶液中で、37℃、10分間作用させた後、培養液により細胞を洗浄するだけで簡単に標識細胞を得ることができます。同様の条件下でスクシンイミジルエステル化合物を作用させても、細胞はまったく標識されないことからも、高速電子環状反応を活用した新たな細胞標識法の有用性は明らかです。何よりも、“生体試料と標識プローブの溶液を混ぜて完了”という至って簡単な操作だけで標識できるため、最も利便性の高い標識法といえます。
この標識法では、スクシンイミジルエステル化合物による標識法と比較すると、1,000倍以下の希釈濃度でも反応が進行するため、生体試料の活性を損なうことなく、試料の“外側”に位置する反応性の高いアミノ基だけで反応が選択的に進行します。実際、蛍光分子TAMRAは、細胞膜に発現する糖タンパク質のN-カドヘリンと同じ位置に確認され、細胞膜だけを選択的に標識していることが分かりました。
新たな細胞標識法の信頼性を確認するために、蛍光標識した細胞が機能を保持しているか、さらに、マウスの生体内で標識細胞の動きを観察できるかどうかを調べました。リンパ球は、胸腺、骨髄などの特定の場所で産生され、まず特定の組織に入った後、この場を離れて全身を巡り、再び特定の組織に戻っていきます。この現象はリンパ球のホーミングと呼ばれています。そこで、新たな方法で標識したリンパ球が、正しいホーミングを保っているかどうかを調べました。具体的には、正常マウスから単離したリンパ球に、Cy5蛍光基(蛍光波長670nm、赤色)を標識し、この標識したリンパ球を、ヌードマウスに尾静脈から投与して、マウスを生きた状態のままで蛍光イメージングしました(図2)。その結果、標識したリンパ球の正しいホーミング、すなわちリンパ節や脾(ひ)臓などのリンパ組織へ集積する様子が観察でき、これまでの生体内蛍光イメージングに比べ、鮮明な画像を得ることに成功しました。
今後の期待
本研究で開発した標識方法は、蛍光分子だけでなく各種金属の配位子でも、生きた細胞を標識することが可能です。従って、より簡便に標識細胞を利用したPETやMRイメージング技術※7などへ応用できるようになります。特異的な機能を持つさまざまな物質で細胞を標識すると、標識細胞の生体内での動きを観察できるだけでなく、自在に細胞の持つ機能を拡大でき、生物学や基礎医学、さらには臨床医学に対しても幅広く応用できると期待されます。
発表者
理化学研究所
分子イメージング科学研究センター
分子プローブ機能評価研究チーム
チームリーダー 尾上 浩隆(おのえ ひろたか)
研究員 田原 強(たはら つよし)
Tel: 078-304-7121 / Fax: 078-304-7123
分子イメージング科学研究センター
分子プローブ動態応用研究チーム
チームリーダー 渡辺 恭良(わたなべ やすよし)
研究員 野崎 聡(のざき さとし)
Tel: 078-304-7124 / Fax: 078-304-7126
お問い合わせ先
神戸研究推進部 企画課Tel: 078-306-3007 / Fax: 078-306-3039
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.高速6π-アザ電子環状反応
1-アザトリエンの末端炭素原子と窒素原子が結合してピリジン誘導体を与える反応をアザ電子環状反応と呼ぶ。この反応は古くから良く知られていたものの、長い反応時間と高い反応温度が必要とされ、さらに収率も良くなかったことから積極的に合成法として活用されることは少なかった。しかし1998年に、アザ電子環状反応を強力に促進させる置換基効果が発見されて以来、この“高速アザ電子環状反応”は天然物の合成に限らず、生物分野や医療分野への応用、例えば、生体分子や細胞の標識、あるいはエンジニアリングのための次世代クリック型反応として大きな注目を集めるようになった。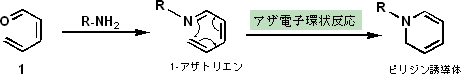
- 2.ホーミング
リンパ球は、胸腺、骨髄などの一次リンパ組織で産生され、血管系を経てリンパ節、パイエル板、脾臓などの二次リンパ組織の間を繰り返して循環する。リンパ球はリンパ組織内で外来抗原などの刺激により特定のリンパ球(エフェクター細胞やメモリー細胞)などへ分化し、リンパ組織内の特定の領域(ヘルパーTリンパ球は傍皮質領域、Bリンパ球は皮質内の胚中心、プラズマ細胞は髄索領域)やほかの特定の組織へと分布するようになる。一方、分化しなかったリンパ球はリンパ管を経てそのリンパ組織を離れ、胸管を介して血管系に戻り、さらに再循環現象を繰り返す。このようなリンパ球の移動現象は一般にリンパ球ホーミング(lymphocytehoming)と呼ばれている。 - 3.DOTA
1,4,7,10-Tetraazacyclododecane-N,N',N'',N'''-tetraaceticacidの略。金属イオンを結合する化合物。PETイメージングでは、主に放射線を放出する68Ga(ガリウム)や64Cu(銅)を結合した状態でタンパク質などの高分子を標識するために用いる。 - 4.PET(陽電子放射断層画像撮影法)
Positron Emission Tomographyの略。ごく微量の放射線を出す原子を薬などの分子に導入し、そこから出る放射線を測定することで、薬が体内のどこにあるかを見る方法。PETで見ることができる放射線を出す原子には、炭素や窒素、酸素、フッ素および金属などを用いる。 - 5.スクシンイミジルエステル化合物
カルボン酸の活性エステルの1つであり、水酸基をエステル化またはアミノ基をアミド化する際に利用される。アミノ基は水酸基に優先して反応を受ける。合成有機化学に加えて、ペプチドやタンパク質のアミノ基に対して標識する際やバイオコンジュゲートの方法として使用される。 - 6.ヘキサトリエン-β-カルボニル化合物
アミノ基を高速6π‐アザ電子環状反応によって修飾するための化合物の総称。 - 7.MRイメージング
Magnetic Resonance Imagingの略。磁気と電磁波、それに水素原子の動きを利用して、主に身体の解剖学情報な情報を得る技術。水素原子には、磁気に反応する性質があるため、磁場をつくる装置の中で体に電磁波を当てると、体内の水素原子が反応して信号を発することから、その信号をとらえて、コンピューターで解析して画像にしている。
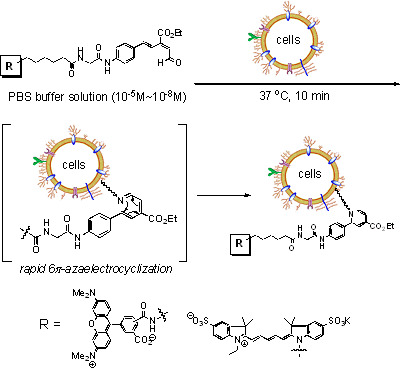
図1 6π-アザ電子環状反応による細胞表層の標識
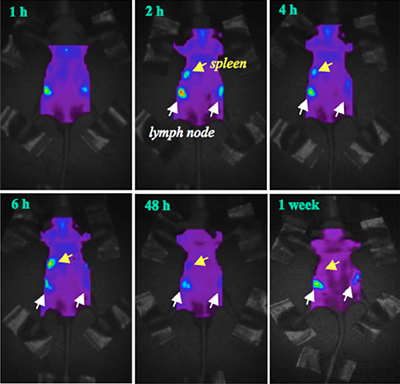
図2 リンパ球ホーミングの非侵襲的蛍光イメージング
1万個の蛍光標識したリンパ球をマウスの尾静脈から投与し、リンパ球のホーミングを時間ごとに蛍光イメージング装置で観察した。投与2時間後には、脾(ひ)臓(spleen)とリンパ節(lymph node)への蛍光標識したリンパ球の集積をはっきりと観察した。リンパ節への集積は、投与後1週間でも観察することができ、脾臓では48時間後まで集積を認めた。
