2010年10月6日
独立行政法人 理化学研究所
固定化した酸を使ったタンパク質自動加水分解装置を初めて開発
-熟練技術に頼っていたタンパク質分析の自動化に貢献-
ポイント
- タンパク質溶液をセットするだけで、アミノ酸まで完全に加水分解
- 固定化した酸を触媒として使うため、装置の腐食がなく、分解の制御も容易に
- 中和も不要で環境に優しく、機能性ペプチド・アミノ酸産生の産業利用にも期待
要旨
独立行政法人理化学研究所(野依良治理事長)は、スルホン酸基を固定化した固体酸※1を触媒※2として用いると、タンパク質をアミノ酸までほぼ完全に分解できることを発見し、この固体酸触媒を組み込んだ自動加水分解装置の開発に世界で初めて成功しました。これは、理研基幹研究所(玉尾皓平所長)ケミカルバイオロジー研究基盤施設バイオ解析チームの益田晶子協力研究員と堂前直チームヘッドによる研究成果です。
タンパク質の定量や、生命現象の鍵となるタンパク質の翻訳後修飾※3を解析するためには、タンパク質をアミノ酸にまで加水分解して分析するアミノ酸分析※4が必要不可欠な手法となっています。従来、タンパク質の加水分解には、加水分解物との分離が容易なため、塩酸などの揮発性の酸を用いる方法が利用されてきました。この方法は、試料の酸化を防ぐための脱気、ガラス封管などの煩雑な手作業を必要とするため、作業の熟練度が結果に大きく作用します。操作を簡便にして作業者の個人差によるバラつきを避け、同じ結果を出すためには自動化が有効ですが、使用する酸の高い揮発性から金属製の部品が腐食されるため、一連の操作の装置化が困難でした。
研究チームは、揮発性の酸を試料に加える従来の手法ではなく、酸を固定化した固体酸触媒に試料を添加することで装置の腐食も防ぐ自動加水分解装置を考案しました。固体酸触媒は低分子物質の分解に使われているものがありましたが、タンパク質(高分子)に対しては触媒として機能せず、ほとんど分解しませんでした。さまざまな固体酸触媒で試験を重ねた結果、タンパク質の精製に使っているスルホン酸基を持った陽イオン交換体※5が固体酸触媒としても有用で、タンパク質を最も効率よく分解できることを見いだしました。この陽イオン交換体は、タンパク質吸着のための大きく開いた穴を持っており、そこに密集する官能基※6(スルホン酸基)がタンパク質の加水分解にも有利でした。そこで、この陽イオン交換体を固体酸触媒として反応管に充填して組み込んだタンパク質の自動加水分解装置を開発し、実際にタンパク質の牛血清アルブミンを注入したところ、期待どおりタンパク質をほぼ完全にアミノ酸まで分解できました。この方法は、加水分解物の中和が不要なため環境にもやさしく、食品などの産業分野でも有用で、最近注目の高まっている機能性ペプチドの産生への応用も期待されます。
本研究成果は、米国の科学雑誌『Analytical Chemistry』オンライン版に近く掲載されます。
背景
アミノ酸分析は、タンパク質化学などの基礎科学分野で非常に重要であるだけでなく、応用面でも、食品や化粧品、医薬品などさまざまな製品開発や品質管理に広く使われています。タンパク質を加水分解して得られるアミノ酸や遊離アミノ酸を簡便に分析するために、1960年代には、液体クロマトグラフィーとニンヒドリン発色反応※7による検出を組み合わせた自動アミノ酸分析計が開発され、市販の装置が入手可能です。この自動アミノ酸分析計は、定量性があり信頼性も高いという優れた特徴がある反面、分析時間が長い、感度が低く分析にはナノ(1ナノは10億分の1)モル程度のアミノ酸が必要という課題も抱えていました。そのため近年になると、あらかじめ蛍光物質でアミノ酸をラベルした後、逆相クロマトグラフィー※8で迅速に分離を行う手法が開発され、感度が3桁ほど高いピコ(1ピコは1兆分の1)モル程度のアミノ酸を分析することが可能となっています。しかし、分析の第一段階として必要なタンパク質の加水分解では、塩酸やメタンスルホン酸などの強酸、水酸化ナトリウムなどの強アルカリ、プロテアーゼなどの酵素を用いた古典的な方法が使われています。一般的には、加水分解後に容易に除去できる揮発性の塩酸などの酸が使われ、6モル/リットルという高濃度の塩酸とともに、110℃で24時間加熱する方法を使います。この加水分解操作は煩雑で、試料の脱塩、酸化を防ぐための脱気、封管などの複雑な手作業を伴うため、分析の精度向上や試料の微量化促進の妨げになっていました。操作の簡便化、試料の微量化を進めるためには自動化が必須ですが、アミノ酸分析の要である加水分解では揮発性の酸を使用するため、装置の腐食が自動化の大きな壁となっていました。
研究手法と成果
研究チームは、揮発性の酸を用いる従来の方法とまったく逆の発想で、固定化した酸(固体酸触媒)を反応管に充填し、試料であるタンパク質溶液を反応管へ送液すると、装置へのダメージもなく、タンパク質をアミノ酸まで加水分解できると考えました。この考えを実現するためには、効率よくタンパク質を加水分解し、固体酸触媒として機能する物質を探す必要がありました。まず、無機の固体酸や低分子分離用の陽イオン交換体で試験しましたが、タンパク質を分解する能力がほとんどないことが分かりました。そこで、タンパク質が十分に入る大きさの穴を持ったタンパク質用の陽イオン交換体を候補に挙げました。陽イオン交換体を固体酸触媒として利用する例は、低分子の有機反応では報告されていましたが、タンパク質などの高分子では分離・精製以外では用いられず、触媒として用いることは常識を覆す利用方法でした。牛血清アルブミンを標準タンパク質溶液として加水分解の試験を手動で実施し、いくつかの陽イオン交換体の候補で反応温度、時間、耐熱性などを評価した結果、スルホン酸基を持つ陽イオン交換体のうち、タンパク質吸着能力の高いものがタンパク質をほぼ完全にアミノ酸に分解することを発見しました。さらに研究チームは、この陽イオン交換体を充填した反応管を、市販の高速液体クロマトグラフィー装置に組み込んだ自動加水分解装置(図1)を開発しました。実際にこの装置を用いて牛血清アルブミン水溶液を自動で加水分解したところ、手動と同等にタンパク質を加水分解することに成功し、従来法と同等のアミノ酸組成を得ました(図2)。
今後の期待
固体触媒は、回収が容易で環境負荷が少ないため、近年大変注目を集めています。今回の研究成果は、熟練を要することが障壁になっていたタンパク質の加水分解において、懸案の自動化を実現し、タンパク質化学でのアミノ酸分析の利用を促進するだけでなく、機能性ペプチドや有用なアミノ酸の産生にも利用を広げることとなります。この技術は、環境負荷を軽減できるだけでなく、触媒の再利用が可能で大量処理も容易なうえ、加水分解物の中和が不要なため、加水分解物をそのまま利用することが可能です。さらに、温度や時間などの反応条件を簡単に調整できるため、タンパク質分解の程度を制御できます。今後は、食品分野を始めとするさまざまな分野で産業利用が広がると期待できます。
発表者
理化学研究所
ケミカルバイオロジー研究基盤施設 バイオ解析チーム
チームヘッド 堂前 直(どうまえ なおし)
Tel: 048-467-9510 / Fax: 048-462-4704
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.固体酸
酸として働く固体で、一般の液体の酸と同様の性質をもつ。シリカ-アルミナ混合物、酸化バナジウムのような無機化合物や陽イオン交換体などがその例である。 - 2.触媒
化学反応の反応速度を速める物質で、自身は反応の前後で変化しない物質。 - 3.翻訳後修飾
遺伝情報に基づいて作られたタンパク質のアミノ酸に、糖鎖やメチル基などが付加されること。この修飾は、細胞の発生・分化、細胞間相互作用、組織形成、タンパク質自体の折り畳み(フォールディング)の促進など、さまざまな生体内のプロセスに関与し、生命現象の鍵となっている。 - 4.アミノ酸分析
タンパク質を加水分解したアミノ酸または遊離のアミノ酸の構成比や絶対量を分析する方法。 - 5.陽イオン交換体
基材に負電荷を持たせることで溶液中の陽イオンと結合・解離可能なものをいう。水の純化やタンパク質の精製などに用いられている。 - 6.官能基
物質の化学的属性や反応性による原子団の分類で、化学的な性質を化合物に与える原子群を指す。ここではスルホン酸基のこと。陽イオン交換体では、硫酸の1つのヒドロキシル基をプロピル基やエチル基に置換したスルホプロピル基やスルホエチル基の形で使われる。このスルホン酸基はプロトンが解離することによってタンパク質との相互作用点になるほか、酸点として強酸の特性をもつ。 - 7.ニンヒドリン発色反応
ニンヒドリン(2,2-ジヒドロキシインダン-1,3-ジオン)水溶液とアミノ酸などアミノ基を持つ化合物が反応して紫色に発色する反応。 - 8.逆相クロマトグラフィー
紙の上でインクがぬれてにじむ際に色素が分離するように、固定相(紙)と移動相(水)の親和性の差により試料を分離する方法をクロマトグラフィーという。中でも極性の低い固定相に極性の高い移動相を用いる分離方法を逆相クロマトグラフィーという。
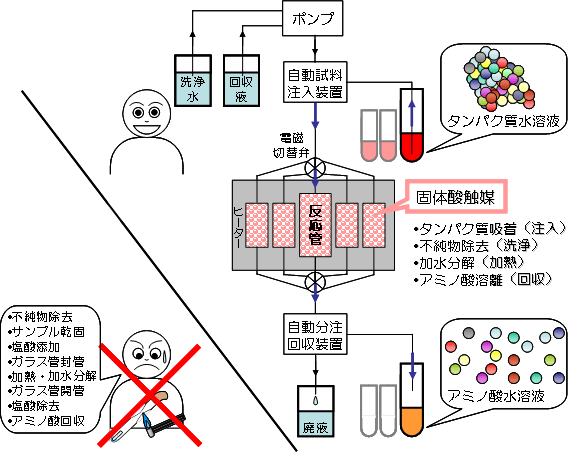
図1 タンパク質を注入するだけでアミノ酸として回収可能な全自動加水分解装置
開発した全自動加水分解装置は、手動で行う複雑な操作(不純物除去、試料乾固、塩酸添加、ガラス管封管、加熱加水分解、ガラス管開管、塩酸除去、アミノ酸回収)を、注入・洗浄・加熱・回収の4ステップに簡略化して自動で行う。基本的な装置の構成は、ポンプ、試料を注入する自動試料注入装置、固体酸触媒を充填した反応管、生成したアミノ酸を回収する自動分注回収装置から成る。タンパク質水溶液は、自動試料注入装置によって反応管に導入する(図中の青矢印)。また、複数の試料を独立して別の反応管に導入するために、注入に応じて自動的に反応管を切り替えられる電磁切り替え弁を取り入れた。反応管内の固体酸触媒に試料が吸着した後、洗浄水を反応管に流して不純物を除去、反応管ごと加熱してタンパク質を加水分解し、最後に回収液を送液して生成したアミノ酸を回収する。必要な操作はタンパク質水溶液をセットするだけで、熟練を要する操作を含まないため、これまでアミノ酸分析になじみのない研究者も容易に試行できるようになった。
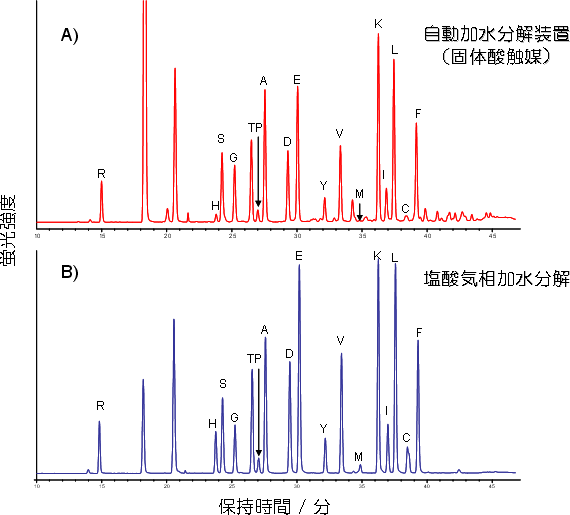
図2 自動加水分解装置と従来法の塩酸で加水分解したときのアミノ酸分析結果
加水分解で得たアミノ酸は蛍光ラベル化し、逆相クロマトグラフィーで分離した。図中の記号はアミノ酸の1文字表記である。図中A)、B)のパターンはほぼ等しく、固体酸触媒でも牛血清アルブミンを従来法と同等に加水分解できることが分かった。
