2010年11月26日
独立行政法人 理化学研究所
独立行政法人 科学技術振興機構
国立大学法人 京都大学
国立大学法人 金沢大学
温室効果ガス「亜酸化窒素」を発生させる酵素の立体構造を世界で初めて解明
-嫌気呼吸から酸素呼吸へと呼吸酵素が進化した手がかりを得る-
ポイント
- 活性中心の2つの鉄原子が一酸化窒素(NO)を亜酸化窒素へと変換
- 嫌気呼吸から酸素呼吸へ、呼吸酵素の分子進化の鍵となる構造変化を解明
- NO消去能を阻害して新規抗菌薬の開発へ期待
要旨
独立行政法人理化学研究所(野依良治理事長)、国立大学法人京都大学(松本紘総長)、国立大学法人金沢大学(中村信一学長)は、温室効果ガスである亜酸化窒素(N2O)を生産する酵素である「一酸化窒素還元酵素(NOR)」の立体構造を世界で初めて明らかにし、2つの鉄原子からなるこの酵素の活性中心が地球温暖化の原因である亜酸化窒素(N2O)を生成するときの反応機構を突き止めました。これは、理研放射光科学総合研究センター(石川哲也センター長)城生体金属科学研究室の城宜嗣主任研究員ら、独立行政法人科学技術振興機構(JST)戦略的創造研究推進事業ERATO型研究「岩田ヒト膜受容体構造プロジェクト」の岩田想研究総括(京都大学 大学院医学研究科 教授)、日野智也研究員(京都大学 大学院医学研究科 客員研究員)と、金沢大学 福森義宏教授らとの共同研究の成果です。
N2Oは、二酸化炭素(CO2)の約300倍強力な温室効果ガス※1であり、オゾン層を破壊する最も強力な気体です。土壌や海中に存在する微生物の呼吸により生じるN2Oは、人類による窒素系肥料の使用でその排出量が年々増加しており、21世紀の地球環境を議論する上で注目を集めています。N2Oを産生する微生物は、脱窒※2と呼ばれる呼吸をしており、酸素ではなく硝酸イオンなどの窒素酸化物を使って生きるためのエネルギーを得ています。この脱窒の過程で、微生物が持っている呼吸酵素NORがN2Oを産生しています。
研究グループは、大型放射光施設SPring-8※3を用いたX線結晶構造解析により、脱窒細菌が持つ膜タンパク質NORの構造を解明することに成功しました。全体構造は、細胞膜を貫通する13本のヘリックス(らせん構造)で構成しており、その内部に2つの鉄からなる反応活性中心が存在していました。これら鉄原子周辺の詳細な構造から、温室効果ガスN2Oの産生の仕組みを明らかにし、微生物によるN2Oの排出を抑制するための戦略を立てる重要な手がかりを得ることができました。
NORは地球上に酸素が無かった太古の時代の微生物の呼吸に必須でしたが、30億年前に起こった光合成による酸素の発生に伴って、酸素呼吸のための酵素へと進化したと考えられています。従って今回の結果は、N2Oを作り出す仕組みを考える上で重要な構造情報を提供するとともに、生物が地球環境の変化に適応するために、どのような戦略で呼吸酵素の分子構造と機能を変化させてきたのか、その分子進化の仕組みを議論するための大きな手がかりとなります。
本研究成果は、米国の科学雑誌『Science』オンライン版(11月25日付け:日本時間11月26日)に掲載されます。
背景
現在の地球上の生物の多くは、酸素(O2)を使って呼吸し、生体エネルギーATP(アデノシン三リン酸)を得ています。しかし、地球上に酸素が出現したのは、今から30億年前といわれており、それ以前に生存していた微生物は、酸素の代わりに、窒素や硫黄の酸化物を使って呼吸を行っていました。酸素が出現した後も、土壌に存在する細菌や、人体内に寄生しさまざまな病気の原因となる細菌のいくつかは、酸素の無い環境、すなわち嫌気条件でも生きていけるような呼吸の仕組みを保持して生き残っています。これらの細菌のいくつかは、硝酸イオン(NO3-)や亜硝酸イオン(NO2-)を窒素ガス(N2)まで還元する硝酸呼吸により、ATPを得ています(図1)。この過程は、窒素固定の逆過程で、脱窒と呼ばれています。脱窒は、工業的あるいは生物的窒素固定や落雷によって地表に取り入れられた窒素原子を再び大気へと循環させる唯一の生物過程で、脱窒細菌が地球規模での窒素原子の循環を維持する上で非常に重要な役割を担っています。この脱窒過程の途中で作り出される一酸化窒素(NO)※4は、細胞に対する毒性が非常に強い有毒ガスのため、脱窒細菌は速やかに別の気体である亜酸化窒素(N2O)※5に変換します。この変換を担う酵素が、今回研究グル―プが構造解析に成功した「一酸化窒素還元酵素(Nitric Oxide Reductase;NOR)」です。NORは、酸素呼吸の重要な酵素であるチトクロム酸化酵素(Cytochrome c Oxidase;COX)※6と共通の祖先を持っています。酸素の出現により、生物が嫌気呼吸から酸素呼吸へと進化して行く過程で、NORはその機能をNO還元(NO→N2O)から、O2還元(O2→H2O)へと変換させて、COXへ分子進化したと考えられています。
近年、NORは環境面から非常に注目されています。NOR酵素反応の生成物であるN2Oが、二酸化炭素CO2の約300倍強力な温室効果ガスで、しかもオゾン層を破壊する21世紀で最も強力な気体であることが明らかとなっています。しかし、人類の産業活動が活発になり、例えば窒素系の人工肥料を多量に使うために、脱窒細菌のNORが作り出すN2Oがどんどん増加しています。N2Oは、手術の際の麻酔ガスとして使われ、笑気ガス(laughing gas)と呼ばれていますが、重大な環境破壊の一因となっていることから、”No laughing matter※7(笑い事ではないよ)”とタイトルを付けた報告も発表されています。このような状況の下、NORがN2Oを作り出す仕組みの解明が望まれていました。
研究グループは、緑膿菌(Pseudomonas aeruginosa)由来のNORの結晶構造の解明に挑みました。
研究手法と成果
NORは、脱窒細菌の細胞膜に埋もれたタンパク質です。このような膜タンパク質は、一般的にX線結晶構造解析に適した質の良い結晶を得ることが大変難しいとされています。これまでデータベースに登録されてきたタンパク質の立体構造(約69,000個)のうち、膜タンパク質の数は200個程度(約0.3%)にすぎません。研究グループは、NORの立体構造を解明するために、2003年から結晶化を始め、試料調製法や結晶化条件の検討を重ね、膜タンパク質の結晶化で成功例の多い、抗体を使った結晶化法※8を適用し、構造解析に使える良質の結晶を得ることに成功しました。取得した結晶について、SPring-8の理研ビームラインBL26B2およびBL41XUを用いたX線結晶構造解析を行い、世界で初めて膜タンパク質である脱窒細菌NORの立体構造を2.7Åの分解能で決定しました。
構造解析の結果、NORは13本の膜貫通へリックスと親水性ドメインで構成しており、その全体構造はCOXの主要サブユニットと非常によく似ていました(図2)。この結果は、両呼吸酵素が同一の祖先を有しているという今までの予想の構造的な裏付けとなりました。しかし、酵素が持っている反応活性中心の構造は、両酵素で異なっていました(図3)。NORでは、活性中心は1つのヘム分子※9と1つの鉄原子から構成され、COXではこの鉄原子が銅原子となっています。NORには鉄原子を固定するためにグルタミン酸が存在しており、このグルタミン酸はNORによるNO還元(N2O産生)の反応を触媒する上で最も重要です。それに対して、COXの銅原子を固定する役割はヒスチジンとチロシンが担っています。このようなアミノ酸の構造の違いが、NORのNO還元(N2O産生)とCOXのO2還元(H2O産生)の機能の違いとなっています。さらに、これらの酵素反応に使われる水素イオンを供給する道筋もまったく異なっていることが分かりました。このように、地球環境の変化に伴って、生物がNOからO2へと呼吸基質を変換していった過程では、全体の構造は変えずに、酵素反応に重要な部位のいくつかのアミノ酸の変異の積み重ねによって分子の構造を変化させる必要があったことが確かとなりました。
今後の期待
今回、NORが有毒ガスNOを無毒化し、温室効果を持ちオゾン層を破壊する気体でもあるN2Oを作り出す仕組みを考える上で重要な構造情報が得られたといえます。どちらの気体も、未来の地球上の生物の生命活動に深く関与します。NORの構造情報を得たことによって、微生物の作り出すN2Oの排出量を押さえるためにはどうしたらよいのか、このことを考える手がかりを初めて得ることができました。
また、今回の成果により、嫌気呼吸、微好気(酸素濃度が低い)呼吸ならびに好気(酸素濃度が高い)呼吸の酵素、いわゆる呼吸酵素ファミリーに属する3種類の酵素の構造が明らかになりました。呼吸という生命維持に不可欠な生理反応が、地球上に酸素が出現する以前の時代から現在に至るまでどのように進化してきたか、この大命題を議論するための重要な構造情報が出そろったのです。今後は、さらなる精緻な構造解析、反応解析と生化学や分子生物学(変異導入など)を駆使することにより、生物が呼吸機能を変化させて地球環境の変化に適応するために、どのような戦略で呼吸酵素の分子構造を変化させてきたのかをさらに詳しく明らかにしていきます。
さらに、NORは、たびたび新聞などのマスコミで大きく取り上げられる院内感染の問題とも深く関係しています。例えば、今回NORを精製した緑膿菌の中には、免疫力が低下している患者に対する日和見感染※10の原因となるものもあります。これらの細菌は、NORを使って、白血球の一種であるマクロファージが産生するNOを消去しながら体内で生存することが知られています。今回解明したNOR立体構造を基にNO消去能を阻害する薬剤をデザインすることができると、まったく新しい抗菌剤の開発につながると期待できます。
発表者
理化学研究所
放射光科学総合研究センター 城生体金属科学研究室
主任研究員 城 宜嗣(しろ よしつぐ)
Tel: 0791-58-2817 / Fax: 0791-58-2818
播磨研究所 研究推進部 企画課
Tel: 0791-58-0900 / Fax: 0791-58-0800
(JSTの事業に関すること)
独立行政法人 科学技術振興機構
イノベーション推進本部 研究プロジェクト推進部
小林 正(こばやし ただし)
Tel: 03-3512-3528 / Fax: 03-3222-2068
お問い合わせ先
独立行政法人 科学技術振興機構 広報ポータル部Tel: 03-5214-8404 / Fax: 03-5214-8432
国立大学法人 京都大学 総務部広報課
Tel: 075-753-2071 / Fax: 075-753-2094
国立大学法人 金沢大学 広報戦略室
Tel: 076-264-5024 / Fax: 076-234-4015
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.温室効果ガス
地表から放射される赤外線を吸収し、大気温を上昇させる効果を持つガス分子。最もよく知られた温室効果ガスは二酸化炭素(CO2)であるが、CO2の温室効果を1とすると、メタン(CH4)はその21倍、亜酸化窒素(N2O)では実に約300倍の効果を持つ。 - 2.脱窒
窒素酸化物(NOx;硝酸イオンと亜硝酸イオン)を窒素ガス(N2)として大気中に変換することやその工程のこと。脱窒反応を行う細菌を脱窒細菌と呼ぶ。 - 3.大型放射光施設SPring-8
兵庫県の播磨科学公園都市にある世界最高の放射光を生み出す理化学研究所の施設。放射光とは、光速に近い速度で加速した電子の進行方向を電磁石で変えたときに発生する、強力な電磁波(X線)のこと。SPring-8の名前はSper Photon ring-8GeVに由来する。SPring-8では、この放射光を用いて、ナノテクノロジー、バイオテクノロジーや産業利用まで幅広い研究が行われている。 - 4.一酸化窒素(NO)
窒素1原子と酸素1原子からなる単純な構造の気体。高い化学反応性を持つフリーラジカルであり、活性酸素と同様、人体には有害なガス分子。NOxの主成分。人体内においてもNO合成酵素により作り出されるが、このNOは細胞情報伝達物質として血管弛緩、血液凝固阻害、記憶・学習、殺菌などさまざまな生理作用に関与している。その一例として、血中の白血球の1つであるマクロファージは、NOを産生して、体内に侵入した細菌やウイルスを殺菌する。 - 5.亜酸化窒素(N2O)
吸入すると筋肉が弛緩し、顔が引きつったような表情になることから笑気ガスとも呼ばれ、手術時の麻酔・鎮静、一部の車のエンジンなどにも利用されている。一方でオゾン層破壊作用およびCO2の約300倍の効果を持つ温室効果ガスでもあり、京都議定書で排出規制がかけられた。常温においては反応性の低い安定した気体。 - 6.チトクロム酸化酵素(Cytochrome c Oxidase; COX)
酸素呼吸にとって最も重要な酵素。電子、水素イオン、酸素分子を使って水を作り出し、この反応に伴って、アデノシン三リン酸(ATP)合成に必要なエネルギーを生成する。 - 7.No laughing matter
2009年8月、アメリカ海洋大気局の研究者らは、亜酸化窒素(N2O)がオゾン層を破壊する最大の要因となっているとする試算に関する論文を Science誌に発表した( Science 326, 123-125, 2009)。この報告を受けて Science誌では、N2Oがlaughing gas(笑気ガス)と呼ばれていることに掛けて「Nitrous Oxide: No Laughing Matter(笑いごとではないよ)」という題名の解説文を掲載した( Science 326, 56-57, 2009)。 - 8.抗体を使った結晶化法
結晶がなかなかできないタンパク質に対し、これに特異的に結合する、比較的結晶化しやすいタンパク質である抗体分子を用いることによって目的タンパク質を結晶化しやすくさせる手法。従来は、水溶性タンパク質において行われていた手法だが、1995年、本研究グループの1人岩田想らにより膜タンパク質であるバクテリア由来のチトクロム酸化酵素に適用され、その立体構造解析に初めて成功した。以来、11種類の膜タンパク質の立体構造がこの手法を用いて決定されており、NORが12種類目の成功例となる。 - 9.ヘム分子
鉄原子がポルフィリン分子の中心に配位した錯体分子。ヘモグロビンやシトクロムなどタンパク質の補欠分子族として用いられ、電子伝達や酸素分子などのガス分子の結合、化学反応の触媒として機能する。 - 10.日和見感染
通常ならば感染症を起こさないような、体内にいる病原性の低い病原体が、免疫力の低下によって増殖することにより発症する感染症。
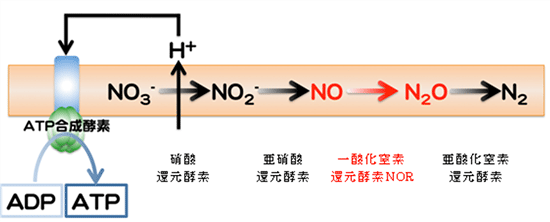
図1 脱窒と硝酸呼吸によるATP生産
脱窒では、窒素酸化物(硝酸イオンNO3-や亜硝酸イオンNO2-)を順次還元し、最終的には窒素ガスN2を発生させる。その途中で一酸化窒素NOと亜酸化窒素N2Oが作り出される。それぞれのステップ(→)は、それぞれ異なる酵素によって触媒される。膜タンパク質である硝酸還元酵素が細胞膜を介した水素イオン濃度勾配を作り出し、そのイオン濃度勾配を用いてATP合成酵素がADPからATPを合成する(硝酸呼吸)。
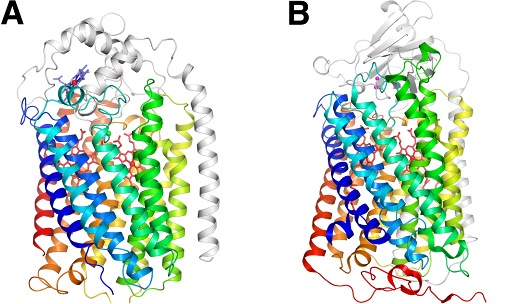
図2 (A)緑膿菌のNORの全体構造と(B)ウシ心筋のCOXの主要サブユニットの構造比較
膜貫通領域の虹色で示した合計13本のヘリックスの配置はNORとCOXのサブユニットで非常に良く似ており、両酵素の祖先が共通のタンパク質であることを構造的に裏付けている。
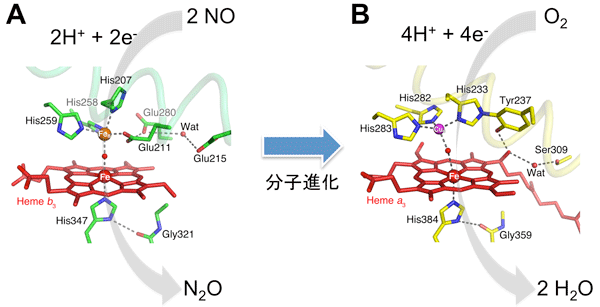
図3 (A)NORと(B)COXの触媒活性中心の構造
NORの活性中心には2つの鉄原子(赤とオレンジ色の球)が存在し、ここで一酸化窒素NOは亜酸化窒素N2Oに変換される。NORの片方の鉄(FeB:オレンジ球)がCOXでは銅(CuB:紫球)に置き換わっている。また、これらの金属原子の周りに存在するアミノ酸側鎖の種類や配置も異なっている。この置換により、COXは酸素を還元する反応活性を獲得したといえる。
