ポイント
- コントラストよく細胞周期を追跡するFucci2
- 薬に対する個々の細胞応答を多面的にキャッチ
- 蛍光イメージング技術の創薬への応用
要旨
独立行政法人理化学研究所(野依良治理事長)は、オリンパス株式会社(菊川剛代表取締役社長)と共同で、細胞周期をリアルタイムで可視化する技術を薬効評価実験に応用し、抗がん剤にさらされた細胞が示す細胞周期異常を多面的に解析しました。その結果、分裂をスキップして核DNA量を増大させる現象など多様な細胞応答を観察することに成功しました。抗がん剤を細胞周期制御の観点で再評価する必要性を示す研究データです。理研脳科学総合研究センター(利根川進センター長)細胞機能探索技術開発チームの宮脇敦史チームリーダー、独立行政法人科学技振興機構(JST)戦略的創造研究推進事業ERATO型研究「宮脇生命時空間情報プロジェクト」(研究総括 宮脇敦史)の阪上(沢野)朝子研究員らと、オリンパス株式会社の小林民代研究員との共同研究による成果です。
細胞は、細胞周期を刻みながら分裂を繰り返して増殖します。生物の発生や再生では、細胞の増殖と分化とが協調的に制御されて、組織、器官、個体が形成されます。しかし、そうした協調的制御が破綻して細胞の増殖が無制限に繰り返されると、がんが発生します。研究チームは、2008年2月に、細胞周期を蛍光で可視化するFucci技術※1の開発を報告しました。Fucciプローブは、分裂後からDNA複製前の時期にある細胞の核を赤色の蛍光で、DNA複製から分裂前の時期にある細胞の核を緑色の蛍光でそれぞれ標識します。近年、Fucci技術を活用することで、生物個体の形態形成、創傷治癒、がん化などのメカニズムに関して新たな知見がもたらされてきています。また、がんの治療評価や診断法開発、さらには移植後の胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)の増殖をモニターする技術の開発に役立つことが期待されています。
今回、抗がん剤に対する細胞の応答性を調べる研究にFucci技術を活用し、個々の細胞が見せる反応を定量的に観察することを試みました。古典的な抗がん剤として有名なetoposide(エトポシド)で処理した細胞の反応を経時的に調べたところ、低濃度ではG2(分裂前準備期)期における細胞周期進行が停止する現象(G2 arrest)、中濃度では細胞核が分断化する現象(nuclear mis-segregation)、また高濃度では細胞分裂をスキップして核DNA量が増大する現象(endoreplication)が観察されました。nuclear mis-segregationを示す細胞が死に向かうのに対して、endoreplicationを示す細胞は、抗がん剤に対する抵抗性を獲得したものと見みなされます。この結果は、高濃度の抗がん剤投与によってがん細胞がより悪性化する可能性を示しており、現行の抗がん剤開発におけるスクリーニング方法に一石を投じるものと注目されます。
本研究成果は、英国の科学雑誌『BMC cell biology』に近く掲載されます。
背景
細胞の分裂(増殖)は、細胞周期と呼ばれるサイクルに従って進行します(図1上)。細胞周期は、分裂が起こるM(Mitosis)期と、DNAの複製が起こるS(Synthesis)期、それぞれの間をつなぐG1(Gap1)期、G2(Gap2)期からなります。周期は、G1→S→G2→M→G1→・・・の順に進み、G1期とG2期には、それぞれS期とM期に入るための準備と点検が行われます。
研究チームは、2008年2月に、蛍光タンパク質を用いて細胞周期をリアルタイムで可視化するFucci(Fluorescent ubiquitination-based cell cycle indicator)技術を開発しました(2008年2月8日プレスリリース)。Fucciプローブは、G1期にある細胞の核を赤色の蛍光で、S/G2/M期にある細胞の核を緑色の蛍光で標識します。蛍光顕微鏡で観察すると、個々の細胞がどの細胞周期にあるかを瞬時に知ることが可能です。すでにFucci技術は世界中に普及し、さまざまな分野で使用されています。
研究手法と成果
(1)改良版Fucci(Fucci2)の開発
研究チームはFucci改良版の開発を進め、蛍光タンパク質としてmCherry(励起極大波長;580nm、蛍光極大波長;610nm)とmVenus(励起極大波長;515nm、蛍光極大波長;528nm)を用いたFucci2を作製しました。mCherryとmVenusは、世界中で多用されている蛍光タンパク質であり、オリジナルのFucciに比べ、2色の波長が離れているために、G1期、S/G2/M期をより簡単に分離してイメージングできるという利点があります。研究チームは次に、このFucci2をNMuMG細胞およびHeLa細胞に恒常的に発現させた細胞株(NMuMG/Fucci2、HeLa/Fucci2)を樹立しました。
(2)抗がん剤の評価実験
古典的な抗がん剤etoposideで処理した際のNMuMG/Fucci2細胞およびHeLa/Fucci2細胞の反応を解析しました。etoposideは、DNA topoisomerase II という酵素の阻害剤として知られており、この薬で処理した細胞は、主にG2期で細胞周期が停止し(G2 arrest)、いずれ細胞死に至ると考えられています。解析には、以下の3つの方法を用いました。
- (a) 核染色を施して細胞の核DNA量を統計的に解析するFACS※2、
- (b) 個々の細胞の核DNA量と画像データを取得・保存・解析するCELAVIEW(high content screening装置)※3
- (c) 生細胞の画像を時間を追って取得・保存するタイムラプスイメージング※4。
HeLa/Fucci2細胞は、低濃度から高濃度のetoposideに対し、G2 arrestを示しました。一方NMuMG/Fucci2細胞は、予想に反して、etoposide濃度に依存して多様な反応を示すことが判明しました(図2、3)。具体的には、低濃度のetoposideはG2 arrestを引き起こすのに対し、中濃度のetoposideは、細胞核の分断化現象(nuclear mis-segregation)を引き起こしました。さらに、高濃度のetoposideは、細胞分裂をスキップして核DNA量を指数関数的に増やす特異な細胞周期進行モード(endoreplication)を誘起しました(図1下)。
今回Fucci技術を導入する事で、etoposide暴露の後に、細胞がG2 arrestからendoreplicationサイクルに移行する瞬間を捉えることに成功しました。
細胞の核分断化や核DNA量増大化を詳細に解析するためには、上記方法の(b)CELAVIEWおよび(c)タイムラプスイメージングを行うことが必要です。しかし、従来の薬剤応答の評価実験は、(a)FACSに頼ることが多く、ある時間一点における細胞集団のデータを主に扱ってきました。今回の結果は、たとえ遺伝的背景が同じでも、直面する状況に応じて、1個1個の細胞が多様な応答を示すことを明らかにしています。
今後の期待
創薬事業において、培養細胞を用いた抗がん剤の探索や評価のための技術開発は大きな課題です。今回の研究成果により、Fucci技術を含むハイコンテントスクリーニング法が確立し、創薬業界に貢献することが期待されます。将来は、個人ごとに人工多能性幹細胞(iPS細胞)が樹立され、診断やおよび治療が検討されるオーダーメイド医療が発展すると考えられます。培養細胞を対象に薬剤をより多面的に評価する技術にFucciが加わることがますます期待されます。
発表者
理化学研究所
脳科学総合研究センター 先端基盤技術研究コア 細胞機能探索技術開発チーム
チームリーダー 宮脇 敦史(みやわき あつし)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.Fucci技術
理研と東京都臨床医学総合研究所による共同特許出願中。現在、Takara-clontech社、Invitrogen-life technology 社、amalgaam-MBL社がさまざまなタイプのFucciを発売している。Fucci技術を利用した材料は学術機関に対して無償で配布を行っている( Fuccil)。また、Fucciを恒常的に発現する細胞株はRIKEN BioResource Center Cell Bank より、FucciトランスジェニックマウスはRIKEN BioResource Center Experimental Animal Division より配布している。 - 2.FACS
Fluorescent activated cell sorter解析のこと。細胞に核染色剤を導入することで、細胞のDNA量を統計的に解析することが可能。 - 3.CELAVIEW(high content screening装置)
顕微鏡ベースの解析装置で、細胞個々のDNA含量に加え、画像データを取得・解析することができる。マルチウェルプレートにも対応しており、多数の細胞を一度に処理することが可能。NMuMG/Fucci2のetoposideに対する反応の多様性を、多面的にかつ統計的に解析できる。 - 4.タイムラプスイメージング
顕微鏡下の生きた細胞や組織を経時的に観察する手法。コンピュータから顕微鏡とCCDカメラを制御し、時間を追って画像を取得・保存する。それらの画像をつなぎ合わせて動画を作成すると、生きた細胞や組織の動態を“観る”ことができる。NMuMG/Fucci2細胞がそれぞれの濃度のetoposideに対し、どのような経過を経てnuclear mis-segrigation やendoreplicationに至るのかを知ることができる。
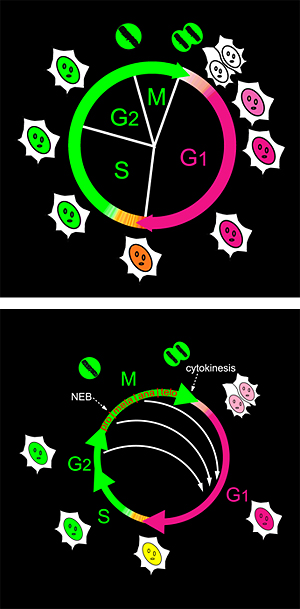
図1 細胞周期とFucci
- 上;
細胞周期とFucciの対応
細胞周期は分裂期(M)、複製前休止期(G1)、DNA複製期(S)、分裂前準備期(G2)より構成されている。分裂期に2つになった娘細胞が、休止期(G1)を経て、DNA複製を行い(S期)、遺伝情報を倍加させて再び分裂期に突入して2つの細胞になる。分化した細胞はG0期(休眠期)と呼ばれているがこの図では示していない。 - 下;
endoreplicationとFucciの対応
NEB;核膜崩壊(nuclear envelope breakdown)、cytokinesis;細胞質分裂
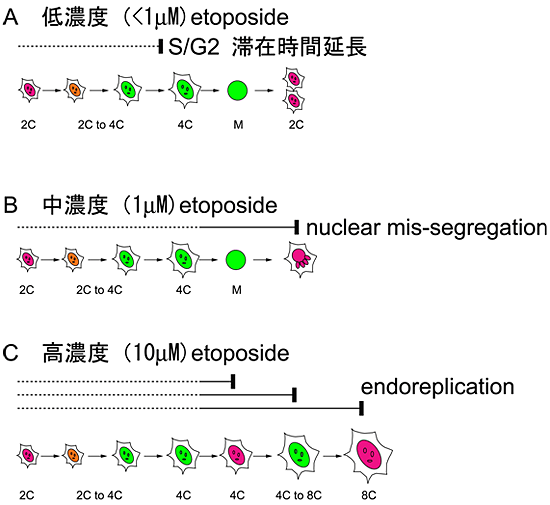
図2 NMuMG/Fucci2細胞をetoposideで処理した際の3つの細胞応答多様性
- A; 低濃度(<1μM)etoposide で処理すると、NMuMG/Fucci2細胞は緑色の時期(G2期)の滞在時間延長(G2 arrest)が起こる。
- B; 中濃度(1μM)etoposideで処理すると、多くのNMuMG/Fucci2細胞は赤色の時期(G1期)で核がずたずたの症状(nuclear mis-segregation, mitotic catastrophe)を示す。
- C; 高濃度(10μM)etoposideで処理すると、NMuMG/Fucci2細胞は緑色や赤色の時期で大きな核の細胞が出現する。これらはendoreplicationという戦略により核内遺伝子情報を倍加させながら健康的に生存している。2C、4C、8Cはそれぞれ核DNA量。
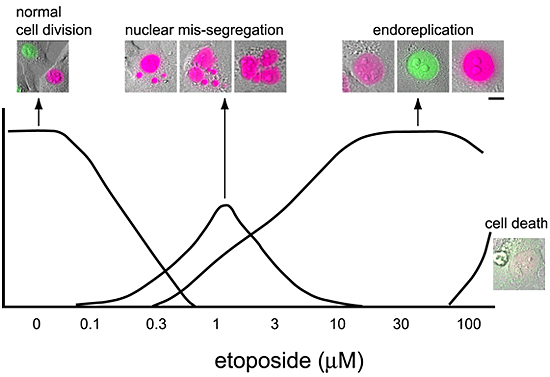
図3 NMuMG/Fucci2細胞のetoposide応答性のまとめ
etoposide濃度と細胞の反応-正常な細胞周期(normal cell division)、nuclear mis-segregation、endoreplication、細胞死(cell death)-をまとめたグラフ、およびそれぞれの分画の代表的な画像。スケールバーは10μm。縦軸は細胞数。
