ポイント
- フィーダー細胞の固定化により、継代培養ごとの調製が不要で幹細胞への混入も回避
- 培養したマウスiPS細胞をマウスに移植し、多分化能の維持を確認
- 幹細胞の大量培養法として有効、再生医療の実現に貢献
要旨
独立行政法人理化学研究所(野依良治理事長)は、iPS細胞※1など幹細胞を培養するとき必要な生きたフィーダー細胞※2の代わりに、化学固定化したフィーダー細胞を用いる方法を開発し、マウスのiPS細胞でその有用性を実証しました。これは理研基幹研究所(玉尾皓平所長)伊藤ナノ医工学研究室の岳暁珊(ユエ シャオシャン)国際プログラム・アソシエイト(現米国ノートルダム大学博士研究員)、伊藤嘉浩主任研究員らと、脳科学総合研究センター動物資源開発支援ユニットの高橋英機支援ユニットリーダー、および東京工業大学フロンティア研究機構の赤池敏宏教授らとの共同研究による成果です。
iPS細胞やES細胞※3をはじめとする幹細胞をシャーレ上で培養するとき、その特徴である多分化能(未分化性)を維持するには、多様な栄養を供給する生きたフィーダー細胞が必要です。フィーダー細胞には、実験の目的に応じてさまざまな細胞種が用いられますが、従来は、継代培養※4ごとの調製の手間や、培養中にフィーダー細胞が幹細胞へ混入する危険性もありました。実際、ヒト幹細胞の培養でマウス由来のフィーダー細胞を使うと、ヒト細胞がマウス由来細胞の影響を受けることも分かり、安心・安全な新しい培養系や培養基材の開発が急務となっています。
これまでに研究グループは、グルタルアルデヒド※5やホルムアルデヒド※6で化学固定化したフィーダー細胞を用いて、ヒト造血幹細胞※7やマウスES細胞、サルES細胞などの培養に成功してきました(J. Biosci. Bioeng. ,(2006,2007))。今回、同様に化学固定化したフィーダー細胞で、マウスiPS細胞の培養に成功し、特にグルタルアルデヒドで固定化した場合には、3回再利用した後でも約95%の細胞が多分化能を維持していることを確認しました。また、凍結乾燥して長期間保存できること、必要な時に解凍して使用できることも分かりました。固定化しているため、フィーダー細胞が幹細胞に混入する恐れもありません。実際に、培養後のマウスiPS細胞をシャーレ上で神経細胞に分化させたり、マウスの皮下に移植して三胚葉※8を含むテラトーマ※9を形成させたりしたことから、iPS細胞が多分化能を維持していることを実証しました。
今後、ヒトiPS細胞でも有効性を示すと、再生医療で必要とされる幹細胞を安心・安全・簡便・安価に培養できるようになると期待できます。
本研究成果は、米国のオンライン雑誌『PLoS ONE』(3月2日付け)に掲載されます。
背景
iPS細胞やES細胞はじめとする幹細胞は、多様な細胞に分化できる性質(多分化能)と増殖性(自己増殖能)を持つため、再生医療、創薬開発などへの応用が期待されています。特にiPS細胞は、ES細胞が抱える倫理的な問題や拒絶反応の問題を解決できると考えられており、多分化能を維持したまま効率よく増殖させることができる、安心・安全な培養方法の開発が求められています。これまで幹細胞の培養には、増殖のための栄養を供給し、多分化能を維持するのに適した環境を整える生きたフィーダー細胞が必要でした。しかし従来の方法では、フィーダー細胞に異種動物由来の細胞がそのまま用いられているため、臨床応用での混入の危険性が指摘されるとともに、技術的に煩雑な工程や継代培養ごとの調製が必要でした。また、マウス由来のフィーダー細胞がヒト由来の幹細胞表面をマウス様に修飾することも分かってきたため、新たな合成基材や培養液の開発が進められています。
研究グループはこうした問題の解決を目指し、化学的に固定化したフィーダー細胞を用いて、新しいiPS細胞培養法の開発に取り組みました。
研究手法と成果
2006年と2007年に、研究グループは、グルタルアルデヒドやホルムアルデヒドで化学固定化したフィーダー細胞を用いて、ヒト造血幹細胞やマウスES細胞を培養できることを明らかにしてきました(図1)。今回、同様の方法でマウス胚性線維芽細胞に由来したフィーダー細胞を化学固定化して、マウスiPS細胞の培養床として用いました。具体的には、フィーダー細胞をグルタルアルデヒド水溶液やホルマリン(ホルムアルデヒドの水溶液)に室温で30分浸して化学固定化しました(図2)。この培養床でマウスiPS細胞を培養したところ、未分化状態を示すNanog※10というタンパク質(図3)やアルカリフォスファターゼ※11という酵素の発現を確認しました。特にグルタルアルデヒドで固定化した場合には、同じフィーダー細胞を3回再利用しても、95%近い細胞が多分化能を維持することが分かりました。次に、培養したマウスiPS細胞の多分化能を調べるために、シャーレ上で神経細胞へと分化誘導させると狙い通り分化が進むこと、7週齢のマウスの皮下に移植すると4週間後には1cm程度の三胚葉を含むテラトーマを形成していること(図4)を見いだし、マウスiPS細胞が確かに分化能力を維持していることを実証しました。
今後の期待
今回の実験により、化学固定化したマウス由来のフィーダー細胞が培養床として十分な機能を持つことを確認しました。固定化により幹細胞への混入を防ぐことができるため、異種動物由来のフィーダー細胞を用いるときに懸念される混入を回避できます。今後は、この化学固定化したフィーダー細胞が、ヒトiPS細胞へも適用可能かどうか検討していきます。また、異種動物の細胞を用いない、つまり、化学固定化したヒト由来のフィーダー細胞でヒトiPS細胞を培養する、というより安心、安全で効率的な幹細胞培養法の確立も目指していきます。
原論文情報
- Xiao-Shan Yue, Masako Fujishiro, Chieko Nishioka, Takashi Arai, Eiki Takahashi, Jian-Sheng Gong, Toshihiro Akaike and Yoshihiro Ito*. “Feeder cells support the culture of induced pluripotent stem cells even after chemical fixation”. PLoS ONE, 2012, PONE-D-11-19849R2
発表者
理化学研究所
基幹研究所 伊藤ナノ医工学研究室
主任研究員 伊藤 嘉浩(いとう よしひろ)
Tel: 048-467-5809 / Fax: 048-467-9300
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.iPS細胞
皮膚組織などの体細胞の特定遺伝子を組み換えることで誘導された、多分化能を持つ幹細胞(万能細胞)のこと。受精卵を利用しないで得られる万能細胞であるため、再生医療へ応用する場合、ES細胞が抱える倫理的問題を解決できると考えられている。また、患者自身の細胞から作ることができるので、iPS細胞から分化した細胞を患者に移植しても拒絶反応が起きにくいと考えられている。 - 2.フィーダー細胞
増殖や分化を起こさせようとする細胞の培養条件を整えるとき、補助の役割を果たす他の細胞種のこと。通常フィーダー細胞には、あらかじめ死なない程度に抗生物質を投与したりガンマ線を照射したりして増殖しないようにする。ES細胞培養の場合は、マウス胎仔由来の線維芽細胞が用いられるが、実験の目的や細胞によってさまざまな細胞種がフィーダー細胞として用いられる。 - 3.ES細胞
胚性幹細胞のこと。受精卵の一段階である胚盤胞から内部細胞塊を取り出して樹立する万能細胞の一種。さまざまな細胞に分化し、増殖する能力を持った発生初期の胚由来の細胞。 - 4.継代培養
植え継ぎ。細胞が増殖して密度が高くなりすぎたり、培地中の栄養分が無くなったりしたとき、細胞の一部を新しい培地に移し、再び培養を行うこと。 - 5.グルタルアルデヒド
生化学や形態学といった生物学分野では、生物試料を自己分解や腐敗から防ぐため、固定とよばれる化学的な処理を行う。グルタルアルデヒドは、固定力が強く、細胞の微細構造を正確に保存することができるため、特に透過型や走査型電子顕微鏡で観察する際には基本的な固定液として広く使用されている。ホルムアルデヒドよりも細胞内への浸透は遅いが、固定力は強いという特徴がある。 - 6.ホルムアルデヒド
高い反応性や細胞透過性を持つ試薬のため、細胞内のタンパク質や核酸の可逆的な架橋剤として、また、細胞や組織の固定液として広く使用されている。水溶液はホルマリン。 - 7.造血幹細胞
血球系細胞に分化可能な幹細胞のこと。ヒト成体では主に骨髄に存在し、白血球、赤血球、血小板、肥満細胞、樹状細胞を生み出す。 - 8.三胚葉
外胚葉、中胚葉、内胚葉の総称。 - 9.テラトーマ
奇形腫のこと。神経、皮膚、筋肉など、さまざまな組織が混在する。 - 10.Nanog
転写因子の1つ。2003年、胚性幹細胞に多能性という独特な性質を与える主な要因であることが明らかにされ、幹細胞の分子マーカーとなっているタンパク質。 - 11.アルカリフォスファターゼ
アルカリ性条件下でリン酸エステル化合物を加水分解する酵素。幹細胞の種類に共通した分子マーカーとして広く用いられる。
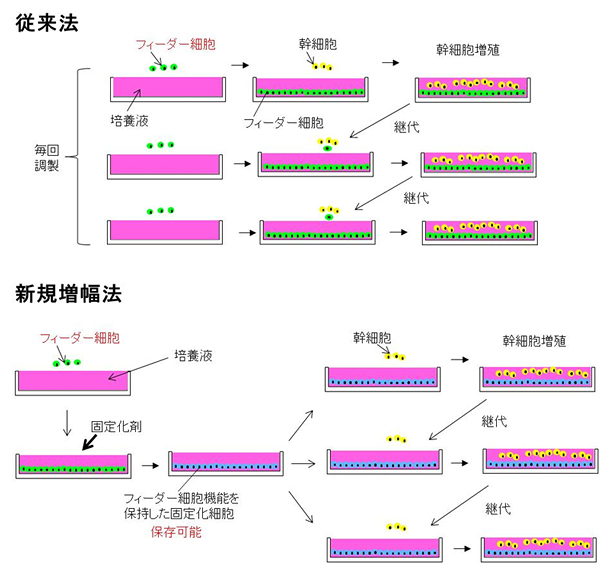
図1 従来法と化学固定化法で処理したフィーダー細胞による幹細胞培養法の比較
- 上: 従来法 継代ごとに調製が必要なうえ、増殖した幹細胞を取り出すとき、フィーダー細胞が混入する恐れがある。
- 下: 化学固定化法 ホルムアルデヒドやグルタルアルデヒドなどの固定化剤でフィーダー細胞を固定化するため、幹細胞への混入を防ぐことができる。
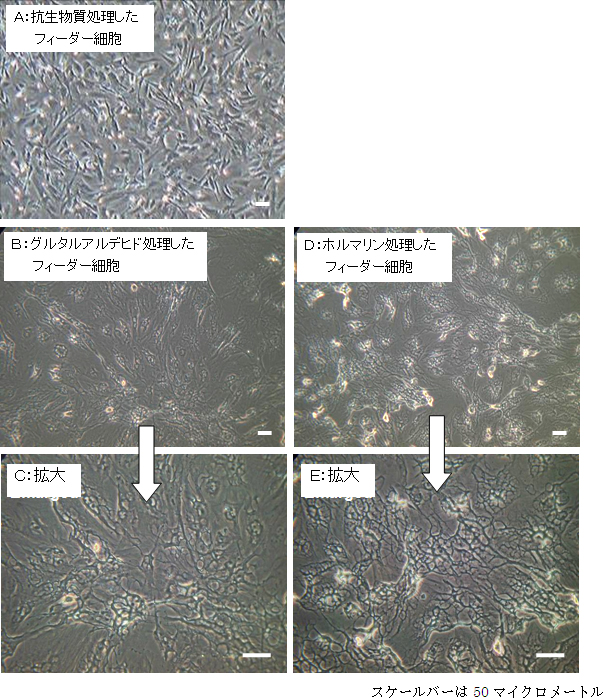
図2 マウス胚性線維芽細胞由来のフィーダー細胞を処理した様子
- A:従来法である抗生物質(マイトマイシンC)による処理
- B、C:グルタルアルデヒドによる固定化(B)とその拡大図(C)
- D、E:ホルムアルデヒドによる固定化(D)とその拡大図(E)
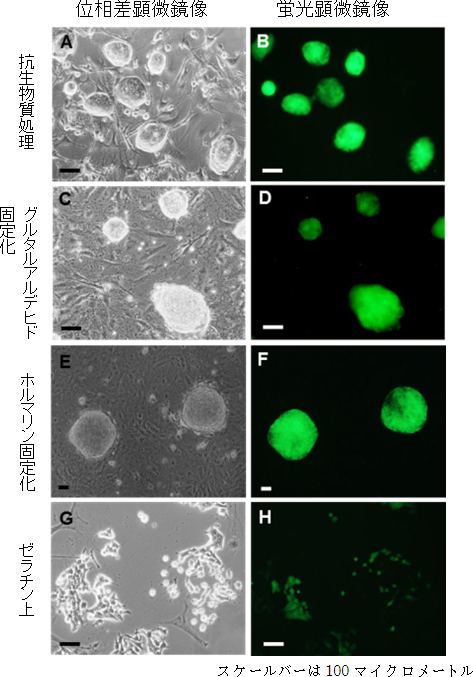
図3 マウス由来のフィーダー細胞で培養したマウスiPS細胞の多分化能
- A、B:抗生物質(マイトマイシンC)で処理したフィーダー細胞上のマウスiPS細胞
- C、D:グルタルアルデヒドで固定化したフィーダー細胞上のマウスiPS細胞
- E、F:ホルマリンで固定化したフィーダー細胞上のマウスiPS細胞
- G、H:ゼラチン上のマウスiPS細胞
多分化能の指標となるNanogに緑色蛍光タンパク質(GFP)を導入し、マウス胚性線維芽細胞由来のフィーダー細胞で培養したマウスiPS細胞の状態を位相差顕微鏡(染色しないで観察できる光学顕微鏡)と蛍光顕微鏡で調べた。従来の抗生物質で処理した場合と同様に、グルタルアルデヒドやホルムアルデヒドで化学固定化した場合でも多分化能を維持していることが分かる。一方、ゼラチン上で培養した場合は、フィーダー細胞がないため適切な環境が整わず、多分化能が失われた。
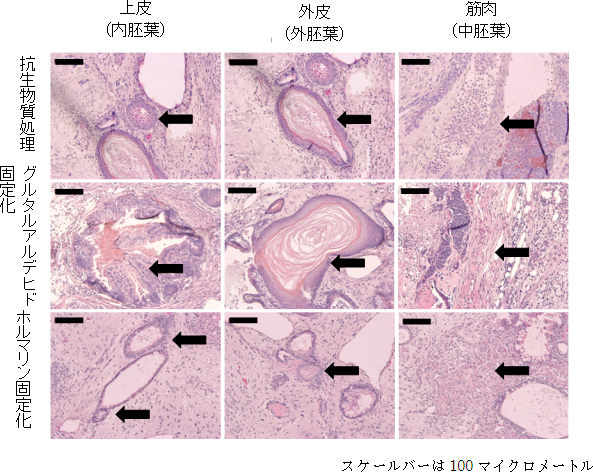
図4 培養細胞をマウスに移植してできたテラトーマの様子
- 上: 抗生物質(マイトマイシンC)処理のフィーダー細胞で培養したiPS細胞が形成したテラトーマ
- 中: グルタルアルデヒド固定化のフィーダー細胞で培養したiPS細胞が形成したテラトーマ
- 下: ホルムアルデヒド固定化のフィーダー細胞で培養したiPS細胞が形成したテラトーマ
抗生物質(マイトマイシンC)、グルタルアルデヒド、ホルムアルデヒドそれぞれで処理したマウス胚性線維芽細胞由来のフィーダー細胞を用いて、マウスiPS細胞を7継代培養した。次に、7週齢のマウスの皮下に移植し、4週間後にテラトーマをヘマトキシリン・エオジン染色で観察。テラトーマ中に三胚葉を認識した(矢印)。
