2013年3月22日
独立行政法人理化学研究所
学校法人日本医科大学
独立行政法人医薬基盤研究所
慢性閉塞性肺疾患(COPD)の増悪に関与するタンパク質を同定
-COPD増悪の新たな診断法や治療法の開発に道-
ポイント
- COPD患者135人のSIGLEC14遺伝子型とCOPDの増悪の関連を解析
- 糖鎖を認識するタンパク質「Siglec-14」がCOPDの増悪に関与
- Siglec-14を持たないCOPD患者は、持つ患者に比べて増悪頻度が4分の1以下
要旨
理化学研究所(野依良治理事長)と日本医科大学(田尻孝学長)は、自然免疫細胞[1]で作られ、糖鎖[2]を認識するタンパク質「Siglec-14(シグレック14)[3]」の有無が、慢性閉塞性肺疾患(COPD)の増悪の起こりやすさに関与することを発見しました。これは、理研基幹研究所(玉尾皓平所長)ケミカルバイオロジー研究領域システム糖鎖生物学研究グループの安形高志チームリーダー、谷口直之グループディレクター(理研-マックスプランク連携研究センター兼任)らと、日本医科大学呼吸ケアクリニックの木田厚瑞特任教授、石井健男講師らによる共同研究グループの成果です。
COPDは「肺の生活習慣病」とも呼ばれ、呼吸困難を伴う慢性の呼吸器疾患です。2008年の世界保健機関(WHO)の統計では全世界において死因の第4位を占め、将来的な患者数の増加が予想されています。COPDは、細菌やウイルス感染などが引き金となって息切れや痰などの症状が急激に悪化(増悪)すると、最悪の場合は死につながりますが、現況ではステロイド剤の投与以外に有効な治療法がないため、新たな治療法の開発が望まれています。
共同研究グループは、Siglec-14タンパク質がCOPD増悪に関わる細菌と接着すること、Siglec-14タンパク質をコードするSIGLEC14遺伝子の型によりこのタンパク質を持つ人と持たない人がいることに着目し、SIGLEC14遺伝子の型がCOPD患者の「増悪しやすさ」に影響するかどうかを検討しました。具体的には、135人のCOPD患者のSIGLEC14の遺伝子型を解析し、1年間の増悪の回数を調べました。その結果、Siglec-14タンパク質を持たない遺伝子型の患者は、このタンパク質を持つ遺伝子型の患者に比べて、年平均の増悪頻度が4分の1以下であることを突き止めました。
この結果は、SIGLEC14の遺伝子型を基に増悪の起こりやすさを判定することで医療の個別化(オーダーメイド医療)が実現できることを示唆します。今後、Siglec-14タンパク質を起点とする一連の免疫細胞の活性化を抑制することにより、COPD増悪の新たな治療法開発につながると期待できます。
本研究成果は医薬基盤研究所(山西弘一理事長)の「先駆的医薬品・医療機器研究発掘支援事業」の支援により行われ、スイスの科学雑誌『Cellular and Molecular Life Sciences』のオンライン版(3月21日付:日本時間3月22日)に掲載されます。
背景
慢性閉塞性肺疾患(chronic obstructive pulmonary disease;COPD)は「肺の生活習慣病」とも呼ばれ、痰や咳、息切れなどを伴う慢性の呼吸器疾患です。COPDの発症は、喫煙などの外的要因とさまざま遺伝的要因が関係していると考えられています。また、細菌やウイルス感染により症状が急激に悪化(増悪)すると、患者の生活に支障をきたし、最悪の場合は死につながります。COPD増悪の治療法は、現在のところ吸入ステロイド剤などに限られており、新しい治療法の開発が望まれています。
共同研究グループは、COPDの増悪に関わるヘモフィルス・インフルエンザ菌とSiglec-14タンパク質が接着することに注目しました。Siglec-14タンパク質は、マクロファージや好中球などの自然免疫細胞で作られ、糖鎖を認識する能力を持つタンパク質の1つです。Siglec-14の機能はまだ良く分かっていませんが、自然免疫細胞の活性化に関わると考えられています。また、Siglec-14タンパク質をコードするSIGLEC14遺伝子の型によってこのタンパク質を持たない人が多数(日本人では約4人に1人)いることが知られています。そこで、共同研究グループは、SIGLEC14遺伝子の型がCOPD患者の「増悪しやすさ」に影響するのではないか、との仮説を立て、その検証に挑みました。
研究手法と成果
日本医科大学呼吸ケアクリニックでCOPDの診断を受けた135人の患者(男性128人、女性7人、平均年齢72.5歳)の協力の下、それぞれのSIGLEC14遺伝子の型を調べました。SIGLEC14遺伝子の型には、祖先型(Siglec-14タンパク質を作る型)と欠損型(Siglec-14タンパク質を作らない型)があります。両親から欠損型を受け継いだ(欠損型ホモ接合[4])人はSiglec-14タンパク質を持ちません。一方、両親から祖先型を受け継ぐ(祖先型ホモ接合)か、両親の一方から祖先型、他方から欠損型を受け継いだ(ヘテロ接合[4])人は、Siglec-14タンパク質を持ちます。1年間にわたって、これらの患者の増悪の回数を調べたところ、Siglec-14タンパク質を持たない患者は持つ患者に比べて、年平均の増悪頻度が4分の1以下と少ないことが判明しました(図1)。
また、Siglec-14タンパク質を持つ自然免疫細胞と持たない自然免疫細胞のモデルを作り、ヘモフィルス・インフルエンザ菌で刺激すると、持つ細胞は持たない細胞よりも強い炎症性の反応を示すことが明らかとなりました。
これらの結果から、Siglec-14タンパク質を持つ患者は炎症性の反応が強く、過剰な炎症が起こるため、増悪の頻度が高くなるというメカニズムを提唱しました(図2)。
今後の期待
SIGLEC14の遺伝子型を調べて増悪を起こしやすい人と起こしにくい人を特定することにより、医療の個別化(オーダーメイド医療)が実現すると期待できます。また、Siglec-14を持たない患者がより増悪を起こしにくいことから、Siglec-14を起点とした炎症性の反応経路を阻害すると、増悪の治療や予防につながると考えられます。今後、Siglec-14を起点としたCOPD増悪の新しい診断法となるバイオマーカーや治療法の開発に向け研究を推進していきます。
原論文情報
Takashi Angata, Takeo Ishii, Takashi Motegi, Ritsuko Oka, Rachel E. Taylor, Paula Campos Soto, Yung-Chi Chang, Ismael Secundino, Cong-Xiao Gao, Kazuaki Ohtsubo, Shinobu Kitazume, Victor Nizet, Ajit Varki, Akihiko Gemma, Kozui Kida, and Naoyuki Taniguchi. “Loss of Siglec-14 reduces the risk of chronic obstructive pulmonary disease exacerbation”. Cellular and Molecular Life Sciences, 2013,
doi: 10.1007/s00018-013-1311-7
発表者
理化学研究所
基幹研究所 システム糖鎖生物学研究グループ 糖鎖認識研究チーム
チームリーダー 安形 高志(あんがた たかし)
学校法人日本医科大学
呼吸ケアクリニック
特任教授(所長)木田 厚瑞(きだ こうずい)
講師 石井 健男(いしい たけお)
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
学校法人日本医科大学 総務部広報課
Tel: 03-3822-2131 / Fax: 03-3824-4446
独立行政法人医薬基盤研究所 研究振興部
Tel: 072-641-9803 / Fax: 072-641-9831
補足説明
- 1.自然免疫細胞
「病原体などが共通に持つ構造パターンを認識して、異物の排除や免疫系の活性化に関わる細胞」のこと。顆粒球(好中球、好酸球、好塩基球)、単球、マクロファージ、樹状細胞などが含まれる。これに対し、B細胞やT細胞のように「特定の抗原に特化した認識タンパク質を持ち、その抗原に特異的に反応する細胞」を獲得免疫細胞と呼ぶ。自然免疫細胞と獲得免疫細胞は相互に情報を交換することにより、免疫系を制御している。 - 2.糖鎖
核酸、タンパク質と並び「第三の生命鎖」と呼ばれる生体分子。細胞膜の表面に存在し、それぞれの細胞に特徴的な構造を外界に示すことで、自分がどんな細胞か、どんな状態にあるかを周囲の細胞に伝えている。白血球が炎症の起こっている場所に移動したり、ウイルスや細菌などの異物を排除したりする際の目印に糖鎖を使うなど、糖鎖は多様な生命現象に関わっている。 - 3.Siglec-14(シグレック14)
糖鎖を認識するタンパク質の1つ。マクロファージや好中球などの自然免疫細胞が作るタンパク質で、これらの細胞を活性化させる機能を持つ。Siglec-14タンパク質をコードする遺伝子の型によって、このタンパク質を持つ人と持たない人がいる。 - 4.ホモ接合、ヘテロ接合
母親から受け継いだ染色体と父親から受け継いだ染色体にある遺伝子の型が同一である状態をホモ接合とよぶ。 SIGLEC14遺伝子の場合、母親と父親からともに祖先型を受け継ぐケース(祖先型のホモ接合)と、ともに欠損型を受け継ぐケース(欠損型のホモ接合)がある。両親の一方から祖先型、他方から欠損型を受け継いだ状態をヘテロ接合とよぶ。祖先型ホモ接合とヘテロ接合の人の体内ではSiglec-14タンパク質は作られるが、欠損型ホモ接合の人の体内ではSiglec-14タンパク質は作られない。
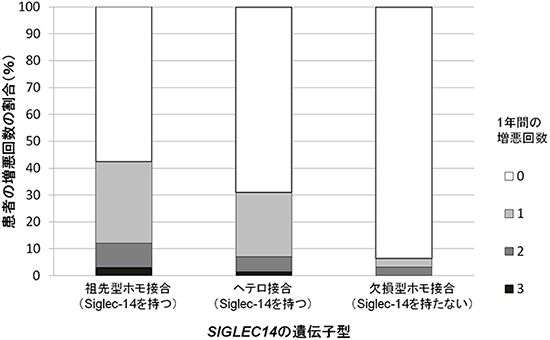
図1 SIGLEC14の遺伝子型がCOPDの増悪頻度に及ぼす影響
COPD患者135人のSIGLEC14遺伝子の型を調べ、Siglec-14タンパク質を持つ祖先型ホモ接合(33人)、ヘテロ接合(71人)、このタンパク質を持たない欠損型ホモ接合(31人)に分けて、1年間のCOPD増悪頻度を調べた。その結果、祖先型ホモ接合とヘテロ接合の患者に比べて、欠損型ホモ接合の患者は、増悪頻度が4分の1以下と少ないことが分かった。
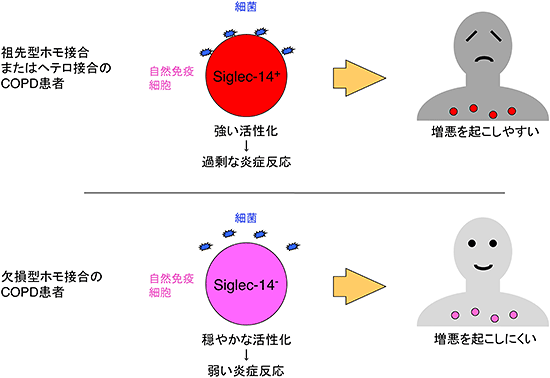
図2 今回推定したSIGLEC14の遺伝子型がCOPDの増悪に影響を及ぼすメカニズム
SIGLEC14遺伝子が祖先型ホモ接合とヘテロ接合の場合、増悪を起こす細菌がSiglec-14タンパク質を介して自然免疫細胞を強く活性化し、過剰な炎症が起こるため、患者は増悪を起こしやすい。一方、欠損型ホモ接合の場合、Siglec-14タンパク質を持たないため、この細菌による自然免疫細胞の活性化は穏やかで過剰な炎症が起きず、患者は増悪を起こしにくい。
