ポイント
- イノシトール三リン酸(IP3)受容体の欠損でスパインが異常に増加
- スパインの異常に伴い、重篤な小脳失調と運動学習の障害が発生
- 脊髄小脳変性症など神経疾患の病態を解明するヒントに
要旨
理化学研究所(理研、野依良治理事長)は、神経回路が完成した成熟後のマウスの小脳[1]で、神経細胞の一種であるプルキンエ細胞[2]のイノシトール三リン酸(IP3)受容体[3]が、樹状突起上にあるスパイン[4]の数を制御し、正常な神経回路を維持していることを明らかにしました。これは、理研脳科学総合研究センター(利根川進センター長)発生神経生物研究チームの御子柴克彦チームリーダー、菅原健之研究員、久恒智博研究員、運動学習制御研究チームらによる研究グループの成果です。
私たちの脳では、数千億個の神経細胞がシナプス[5]を介して結合し、神経回路を形成しています。シナプスは、神経細胞の樹状突起上にある無数のスパインと呼ばれる小さな突起に形成されます。スパインは、生後の発達過程で活発に形成され、成熟後は安定な構造になることで機能的な神経回路を維持します。一方で、一部のスパインは成熟後も学習や記憶、環境などにより再編成されます。そのため、成熟後の脳で神経細胞のスパインの形成が正しく制御されることは、学習や記憶、運動のコントロールなどの高次脳機能にとって非常に重要です。しかし、そのメカニズムは明らかにされていませんでした。
研究グループは、小脳の主要な神経細胞であるプルキンエ細胞だけでIP3受容体を欠損させたマウスで、プルキンエ細胞のスパインが異常に増加し、形が長くなっていることを発見しました。また、スパインの数の異常は、発達の過程ではなく成熟後に起こっていることが分かりました。さらに、スパインの異常に伴い、このマウスは重度の小脳失調と運動学習の障害を起こしました。これらの発見は、成熟後の小脳では、IP3受容体がプルキンエ細胞のスパインの数を正しく制御することで機能的な神経回路を維持し、このメカニズムが小脳の機能である運動のコントロールと学習に重要であることを示しています。この成果は、統合失調症や自閉症、あるいは脊髄小脳変性症[6]など多くの神経疾患の病態解明に役立つと期待できます。
本研究成果は、米国の科学雑誌『The Journal of Neuroscience』の7月24日号に掲載されました。
背景
私たちの脳では、数千億個の神経細胞がシナプスを介して結合し、神経回路を形成しています。シナプスは、神経細胞の樹状突起上にある無数のスパインと呼ばれる小さな突起に形成されます(図1)。スパインは生後の発達に伴って形成され、神経回路が完成した成熟後は安定な構造になり、発達期にできた神経回路を維持します。一方で、一部のスパインは成熟後も学習や記憶、環境などにより再編成されます。スパインにはグルタミン酸などの神経伝達物質に対する受容体が存在し、ほかの神経細胞から情報を受け取る部位であることから、高次脳機能に極めて重要な構造です。また、統合失調症や自閉症などのさまざまな神経疾患においてスパインの形や数に異常が見られることから、神経疾患とスパインの形成を制御するメカニズムとの関連が注目されています。そのため、神経細胞のスパインが成熟後の脳でどのように制御されるのかを知ることは、脳のメカニズムや神経疾患の病態の解明において重要な課題となっていますが、ほとんどが未解明のままでした。
神経細胞がシナプスから入力を受けると細胞内のカルシウム濃度が変化します。カルシウムは細胞内の情報伝達物質として非常に重要な働きをするため、カルシウム濃度を適切に調節することが求められます。この濃度調節に重要な役割を果たしている分子の1つが、イノシトール三リン酸(IP3)受容体です。IP3受容体は、細胞内のカルシウム貯蔵庫の1つである小胞体の膜上にあるイオンチャネル(イオンが通過する小孔)で、細胞外の刺激に応じて貯蔵庫からカルシウムを放出します。IP3受容体には3種類のタイプがあり、タイプ1のIP3受容体(IP3R1)は脳の神経細胞に広く存在し、特に小脳のプルキンエ細胞に豊富に発現しています。
研究グループはこれまでに、全身でIP3R1を機能不全にしたマウス(IP3R1ノックアウトマウス)が、運動が円滑に遂行できなくなる小脳失調やけいれん様発作を起こすこと、また記憶や学習の基礎とされる神経可塑性[7]の異常を示すことを明らかにしています。しかし、IP3R1が脳神経系に広く発現していること、また、IP3R1ノックアウトマウスが生後20日前後の未成熟なうちに死亡してしまうため、成熟後の脳でプルキンエ細胞のIP3R1がどのような役割を果たしているのか、その解明に至っていませんでした。
研究手法と成果
研究グループは、成熟後の脳でプルキンエ細胞のIP3R1が果たす役割を明らかにするために、プルキンエ細胞だけでIP3R1を欠損させた遺伝子改変マウス(プルキンエ細胞特異的IP3R1欠損マウス)を作成しました。そして、このマウスの歩行機能を調べたところ、6週齢から小脳失調症状に見られる“ふらつく”などの歩行障害を示すことが分かりました。さらにこの症状は、週齢が進むにしたがって強くなり、正常な姿勢を保っていられないほど重症化しました。(図2)。また、プルキンエ細胞特異的IP3R1欠損マウスのプルキンエ細胞でのIP3R1の発現を週齢を追って解析した結果、小脳失調症状が現れる6週齢になると、ほとんどのプルキンエ細胞でその発現がなくなることが分かりました(図3)。これらの結果から、プルキンエ細胞のIP3R1の発現が消失する時期と小脳失調の発症時期が一致することが明らかになりました。
次に研究グループは、小脳失調を示す変異マウスでは、しばしば小脳の萎縮や神経細胞の脱落が観察されることから、プルキンエ細胞特異的IP3R1欠損マウスの小脳の形態について調べました。その結果、小脳の萎縮やプルキンエ細胞の脱落は観察されませんでした。ところが、プルキンエ細胞の形態を詳細に解析したところ、樹状突起とスパインの形態に異常が観察されました。このマウスのプルキンエ細胞は、正常マウスと比べて樹状突起の分岐が少なくなっていました(図4)。さらに、正常マウスの樹状突起にはある程度の間隔を空けてスパインが形成されているのに対し、隙間がほとんどないほどにスパインの数が異常に増加し、形も長くなっていました(図5)。このスパインの異常は、小脳の神経回路がほぼでき上がる時期である3週齢では観察されず、成熟してから生じたものであることが分かりました(図5)。さらに、この異常に増加したスパインがシナプスを形成しているのかを調べた結果、これらは小脳皮質に存在する顆粒細胞(神経細胞の一種)の神経軸索である平行線維とシナプスを形成し、機能していることが明らかになりました(図6)。これらの結果は、プルキンエ細胞特異的IP3R1欠損マウスの小脳では、発達の過程で一度正常にプルキンエ細胞のスパインが形成され、正しく神経回路ができ上がったにもかかわらず、成熟後に正常な神経回路を維持するメカニズムが破綻したということを意味しています。これにより、IP3R1がプルキンエ細胞のスパインの数を制御することが、小脳の正常な神経回路を維持するのに重要であることが明らかになりました。
さらに研究グループは、小脳の機能の1つである運動学習について調べました。その結果、プルキンエ細胞特異的IP3R1欠損マウスでは、記憶や学習に必要な神経可塑性が失われていることを発見しました。また、小脳が担う運動学習の1つである眼球運動の適応[8]について解析したところ、正常マウスでは、1時間の学習で眼球運動の適応が起こったのに対し、プルキンエ細胞特異的IP3R1欠損マウスでは適応が起こらず、運動の学習ができないことが分かりました(図7)。IP3R1が運動学習に必須な分子であることを生体で明らかにしたのは初めてのことです。
以上の結果から、成熟後の小脳において、IP3R1がプルキンエ細胞のスパインの数を制御することで機能的な神経回路を維持し、このメカニズムが小脳の機能である運動のコントロールや学習に中心的な役割を果たしていることが示されました(図8)。
今後の期待
今回、研究グループは、成熟後の小脳神経ネットワークを維持するメカニズムにIP3R1が極めて重要な役割を果たしていることを明らかにしました。今後は、IP3R1を介した貯蔵庫からのカルシウム放出がどのようにして神経回路を制御しているのか、その詳細なメカニズムの解明を進めていきます。また、統合失調症や自閉症など多くの神経疾患と神経細胞のスパイン形態異常の関連が注目されていることから、これら神経疾患の病態解明に本研究の成果が貢献することが期待できます。特に近年、日本で特定疾患に指定されている難病である脊髄小脳変性症の原因遺伝子として、IP3R1が同定されました。本研究の成果は、発症メカニズムが不明であり、有効な治療法がなかった脊髄小脳変性症の病態を理解する上でも重要な発見であり、治療法の確立につながる可能性を秘めています。
原論文情報
- Takeyuki Sugawara, Chihiro Hisatsune, Le Dinh Tung, Tsutomu Hashikawa, Moritoshi Hirono, Mitsuharu Hattori, Soichi Nagao and Katsuhiko Mikoshiba.
"Type 1 inositol trisphosphate receptor regulates cerebellar circuits by maintaining the spine morphology of Purkinje cells in adult mice.
The Journal of Neuroscience, 2013, 33(30): 12186-12196,doi: 10.1523/JNEUROSCI.0545-13.2013
発表者
理化学研究所
脳科学総合研究センター 発生神経生物研究チーム
チームリーダー 御子柴 克彦 (みこしば かつひこ)
お問い合わせ先
脳科学研究推進室
Tel: 048-467-9757 / Fax: 048-467-4914
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.小脳
歩行などの運動や平衡感覚の調節を担う脳の部位。運動の学習にも関わる。小脳に異常があると円滑な動作ができなくなり、平衡感覚が悪化して歩行障害などを引き起こすこともある。 - 2.プルキンエ細胞
小脳皮質に一層に並ぶ神経細胞で、小脳の中で唯一の出力細胞。特徴的な形をした大型の神経細胞で、よく発達した樹状突起を分子層に伸ばし、顆粒細胞の軸索である平行線維と下オリーブ核から伸びる登上線維からの情報を受ける。軸索は白質を通って深部小脳核へ投射する。 - 3.イノシトール三リン酸(IP3)受容体
細胞内のカルシウム貯蔵庫の1つである小胞体の膜上に局在するカルシウムチャネル。細胞外の刺激(神経伝達物質やホルモンなど)に応じて産生されるイノシトール三リン酸(IP3)が結合することによりチャネルが開き、小胞体内のカルシウムを細胞質に放出することで、細胞内のカルシウム濃度を調節する。 - 4.スパイン
神経細胞の樹状突起にあるとげ状の構造物。神経伝達物質を受け取る受容体や細胞内のシグナル伝達に関わるさまざまな分子が集積する脳において重要な構造。 - 5.シナプス
神経細胞と神経細胞のつなぎ目。シナプスで結合した神経細胞のネットワークが神経回路である。シナプスでは、シナプス前部である神経細胞の軸索終末からグルタミン酸などの神経伝達物質が放出され、シナプス後部である神経細胞のスパインがこれを受け取ることによって情報が伝達される。 - 6.脊髄小脳変性症
小脳・脳幹・脊髄を中心とする神経細胞が変性・脱落し、歩行障害などの強い運動障害をきたす疾患。孤発性、遺伝性を含めて多くの種類が知られている。常染色体優性遺伝性の脊髄小脳変性症は、現在までに約30種類が知られており、その原因となる遺伝子が多数同定されているが、その分子病態は明らかにされておらず、現在、治療法はまったく存在しない。 - 7.神経可塑性
シナプス入力の強さや頻度に応じて、神経細胞間の情報伝達の効率が柔軟に変化すること。記憶や学習の基礎になると考えられている。 - 8.眼球運動の適応
眼球運動とは、動物の頭や周囲の景色が動いたときに、視野のズレを補正するために眼球が反射的に動くことをいう。動物の周りの景色が動いた場合、その動きがある程度以上速くなると、眼球の動きは視野の動きに十分ついていくことができずにずれが生じるが、動物に視野の動きを見続けさせることにより、眼球の動きが次第に大きくなり、景色の動きについていけるようになる。この現象を眼球運動の適応と呼ぶ。
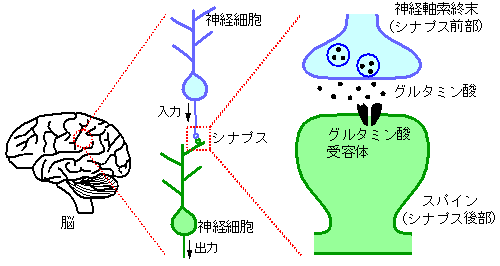
図1 神経細胞の構造
神経細胞同士はシナプスで結合し神経回路を形成する。神経細胞のスパインは、シナプス前部である神経軸索終末とシナプスを形成する後部構造であり、神経伝達物質を受け取る受容体やシグナル伝達物質が多く存在するため、脳機能に不可欠な構造である。
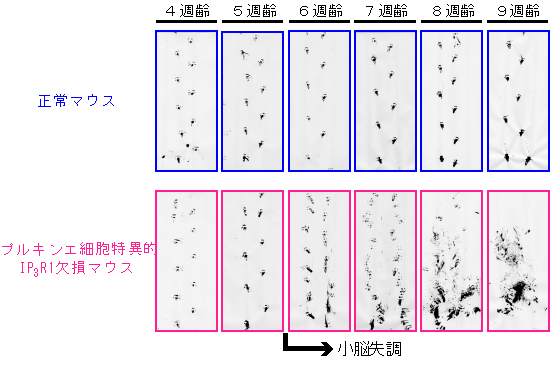
図2 歩行機能の実験結果
各週齢のマウスの足跡を記録した。プルキンエ細胞特異的IP3R1欠損マウスは、6週齢からふらつくなどの小脳失調症状を示し、8週齢以降になると正しい姿勢を保っていられないほど重い症状を示す。
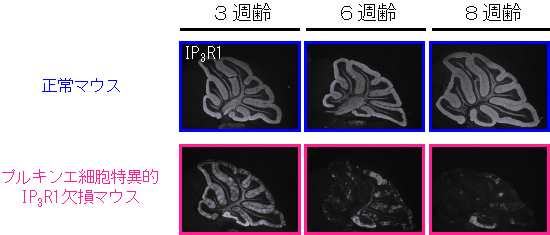
図3 プルキンエ細胞でのIP3R1の発現の比較
各週齢のマウスの小脳切片をIP3R1に対する抗体で染色した。正常マウス、プルキンエ細胞特異的IP3R1欠損マウスとも小脳の神経回路がほぼでき上がる3週齢では、ほとんどのプルキンエ細胞でIP3R1が発現しているが、プルキンエ細胞特異的IP3R1欠損マウスでは、成熟後の6週齢以降になると大部分のプルキンエ細胞でその発現が消失する。
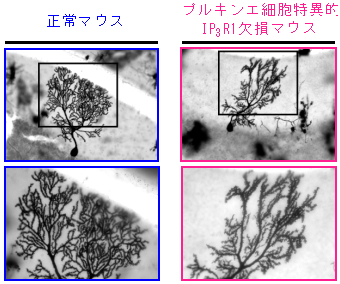
図4 プルキンエ細胞の樹状突起の形態観察結果
成熟後の正常マウスのプルキンエ細胞はよく発達した樹状突起の枝を持つのに対し、プルキンエ細胞特異的IP3R1欠損マウスのプルキンエ細胞では、樹状突起の分岐が少なく隙間が多い形態を示す。
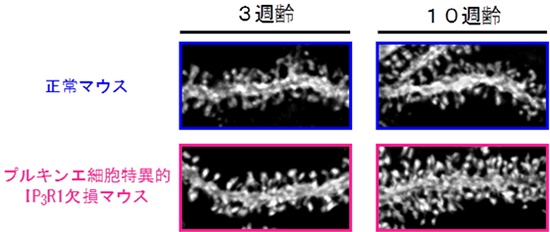
図5 プルキンエ細胞のスパイン形成の観察結果
プルキンエ細胞特異的IP3R1欠損マウスでは、小脳の神経回路がほぼ完成する3週齢で、正常にプルキンエ細胞のスパインが形成されていたにもかかわらず、10週齢でスパインの数が異常に増加する。また、その形も異常に長くなっていた。つまり、プルキンエ細胞特異的IP3R1欠損マウスでは、正しいスパイン密度および形態を維持するメカニズムが破綻している。
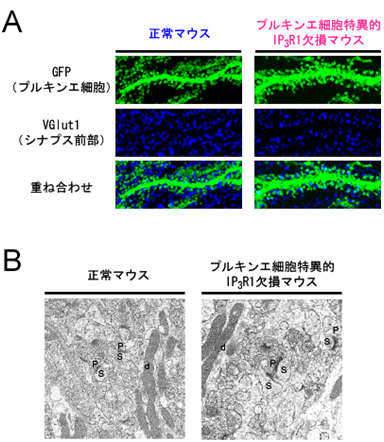
図6 スパインのシナプス形成観察結果
- (A) プルキンエ細胞だけで緑色蛍光タンパクGFPが発現するマウスの小脳切片を用意し、顆粒細胞の軸索である平行線維の軸索終末(シナプス前部)をVGlut1で染色した。正常マウスと同様に、プルキンエ細胞特異的IP3R1欠損マウスのプルキンエ細胞のスパインがVGlut1のシグナルと重なることから、異常に増加したスパインが平行線維とシナプスを形成していることが分かる。
- (B) 小脳の電子顕微鏡による観察画像。プルキンエ細胞特異的IP3R1欠損マウスで異常に増加したスパイン(S)が平行線維の軸索終末(P)とシナプスを形成していことが確認された。(d)はプルキンエ細胞の樹状突起。
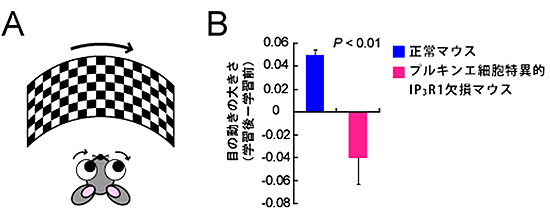
図7 眼球運動の適応についての解析結果
- (A) 眼球運動の適応とは、外界の景色(この実験ではチェックパターンのスクリーン)の動きに対して、その動きについていけるように目の動きを補正する現象。正常マウスでは1時間の学習により、スクリーンの動きとのずれが小さくなるよう、目の動きが大きくなる。
- (B) 正常マウスでは1時間の学習により、目の動きが大きくなったのに対し、プルキンエ細胞特異的IP3R1欠損マウスでは、この適応が生じなかった。
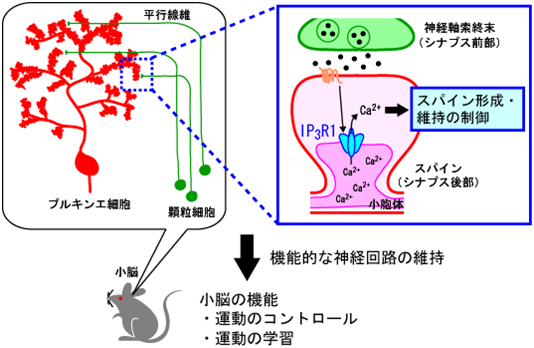
図8 本研究の結果から示唆される成熟脳でのIP3R1の役割
成熟後の小脳において、IP3R1はプルキンエ細胞のスパインの数を制御することで機能的な神経回路を維持し、このメカニズムが小脳の高次機能に重要な役割を果たしている。
