2013年8月8日
独立行政法人理化学研究所
株式会社ダナフォーム
蛍光プローブ「Eprobe」のリアルタイムPCRへの応用
-個別化医療の進展に合わせ簡便・正確な遺伝子検査、病原体検出法の確立へ-
ポイント
- 配列特異的に蛍光を発するEprobeによるリアルタイムPCRの検出系を開発
- 1つのEprobeで遺伝子増幅の検出と遺伝子の変異検出が可能
- 複数色のEprobeを用いることにより1チューブで異なる遺伝子配列に対応
要旨
理化学研究所(理研、野依良治理事長)と理研ベンチャー[1]のダナフォーム(三谷康正代表取締役社長)は、人工核酸を利用した蛍光プローブ「Eprobe(イープローブ)®」とリアルタイムPCR法[2]を組み合わせることで、特定の遺伝子配列のコピー数や発現量、変異の有無を従来法に比べて正確に検出する方法を開発しました。これは、理研ライフサイエンス技術基盤研究センター(渡辺恭良センター長)核酸診断技術開発ユニットの臼井健悟ユニットリーダー、マティアス ハーベス(Matthias Harbers)客員研究員、花見健志研究員、ディアン デロベル(Diane Delobel)リサーチアソシエイトらと、理研予防医療・診断技術開発プログラム(林崎良英プログラムディレクター)、およびダナフォームとの共同研究グループの成果です。
個別化医療や感染症医療の進展に伴い、患者個人の遺伝子変異の判別や病原体由来の核酸(DNAやRNA)の検出を、より安価・正確・迅速・簡便に行うための技術開発が求められています。現在一般的に用いられているリアルタイムPCR法は、特定の遺伝子配列を鋳型としてDNAを増幅し、その量を蛍光プローブで定量化します。しかし現在の蛍光プローブは、定量性や遺伝子変異検出の応用面に課題があり、より優れた手法の開発が試みられてきました。
共同研究グループは、特定の遺伝子配列を認識して蛍光を発する「Eprobe」の開発に成功しました。Eprobeは、リアルタイムPCR法の反応過程で特定の鋳型配列への結合と解離を繰り返し、その際に生じる蛍光の発光と消失を測定することで、増幅された鋳型DNAの定量や遺伝子の変異検出を行う新しいタイプの蛍光プローブです。Eprobeは複雑な配列デザインを必要とせず、これまでのリアルタイムPCRと同じ手法で遺伝子検査システムを構築できるため、今後、遺伝子多型の検査や感染症診断、分子標的薬の適合検査など、さまざまな臨床検査への応用が期待できます。
本研究成果は、米国のオンライン科学雑誌『PLOS ONE』(8月7日付け:日本時間8月8日)に掲載されます。
背景
細胞中の特定の遺伝子のコピー数や発現量を定量的に測定したり、遺伝子型の判別を簡便に検出するリアルタイムPCR法は、生命科学研究から遺伝子診断、病原体の検出など臨床分野にまで広く利用されています。この技術の進展には、PCR反応で増幅された鋳型DNA量を検出するための蛍光プローブの開発が寄与しています。一般的に用いられている蛍光プローブには、PCR反応で生じるDNAの2本鎖に入り込んで蛍光を発するインターカレーター型と、配列特異的な検出を可能とする蛍光色素を導入した人工核酸型があります。インターカレーター型の蛍光プローブは検出感度に非常に優れていますが、2本鎖DNAであればすべて結合してしまうため、ターゲット以外のDNAも検出し、正確な結果が得られないことがあります。そこで近年、特定のDNA配列を認識する人工核酸型の蛍光プローブを用いて、ターゲットのDNAのみを検出する、新しいリアルタイムPCR法の開発がさまざまな機関で行なわれています。
これまで報告されている人工核酸型の蛍光プローブは、2つの色素などの間に生じる蛍光共鳴エネルギー移動(Fluorescence resonance energy transfer:FRET)[3]を利用するものです。しかし、このプローブは構造が複雑で合成が難しいことや、蛍光プローブとDNAの結合による発色反応が非可逆的であるため、増幅したDNA2本鎖を検出できても、その後の1本鎖の解離を検出できないという欠点があります。リアルタイムPCR法による遺伝子型の判別では、野生型遺伝子と変異型遺伝子でDNAが2本鎖から1本鎖に解離する温度が異なることを利用するため、増幅後に解離した1本鎖DNAの配列を特異的に認識し定量化できる新しい人工核酸型のプローブの開発が求められていました。
研究手法と成果
共同研究グループは、励起子相互作用を持つ人工核酸[4]を利用して蛍光のスイッチングを行う蛍光プローブ「Eprobe(イープローブ)」を開発しました。Eprobeは、DNAの部品であるチミン塩基に蛍光色素を2つ持つ構造をしています。これらの蛍光色素は、ターゲットとなるDNA配列と結合していない1本鎖の状態では、励起子相互作用が働いて蛍光発光が抑制されています。EprobeがターゲットのDNA配列と結合し2本鎖を形成すると、2つの色素が分かれてDNAの2本鎖構造に入り込み、色素間の励起子相互作用が解除され蛍光を発します(図1)。リアルタイムPCRを行う際に十分な量のEprobeを加えておくと、合成直後の2本鎖DNAが加熱によりほどけて1本鎖になった後、温度を下げてプライマーがターゲット配列に結合するステップにおいてEprobeも結合します(図2)。このとき発する蛍光を測定することで、増幅DNAの検出を行います。また、PCRのDNA伸長過程における温度では、Eprobeが解離できるようにプローブの配列の長さを調整し、DNA合成酵素の伸長反応を阻害しないよう設計しました。
Eprobeを用いたリアルタイムPCR法による定量検出および遺伝子の変異判別を評価するため、ヒトがん細胞にみられる遺伝子変異の領域(EGFR[5])を対象に実験しました。まず、Eprobeの蛍光に伴う核酸増幅曲線のCt値[6]から算出される定量検出では、102~108コピーまで広い範囲を検出することができました(図3A、B)。次に変異判別の評価のため、野生型遺伝子と変異型遺伝子のそれぞれを増幅したPCR産物に対して、野生型配列をターゲットとするEprobeが解離するときの温度であるTm値[7]を解析しました。その結果、Eprobeの配列と完全にマッチする野生型のDNA配列ではピークが高温側に、1塩基のミスマッチが生じる変異型の場合にはピークが低温側に出現し、変異の有無を判別することができました(図3C、D)。これらの結果から、単一のEprobeを用いたリアルタイムPCR法によって、検出対象となるDNAの定量検出に加え、遺伝子変異の有無を同時に達成できることが明らかとなりました。
さらに、Eprobeが、同じ反応チューブでの1回のPCR反応で、異なるプライマーのセットを同時に用いて複数の遺伝子を増幅するマルチプレックスPCRに応用できるかを検証しました。異なる2つの遺伝子配列をターゲットとし、それぞれ緑と橙色の蛍光を発する色素(D514とD570)で標識したEprobeを用いた実験を行った結果、2つの蛍光色素それぞれの蛍光の増幅と融解に伴うシグナルを同時に検出できることが分かり、EprobeがマルチプレックスPCRにも応用できることが示されました(図4)。
今後の期待
個別化医療の普及や感染症医療において患者の傍らで迅速かつ簡便、正確に遺伝子検査ができるシステムを開発することは、迅速かつ適切な診断、診療さらには予防に寄与できます。そのため、このような遺伝子検査の重要性は高まっており、関連する市場は飛躍的に拡大しています。遺伝子検査のさらなる普及には、より安価、迅速、簡便、確実な検査システムの確立が必要です。
今回開発したEprobeは、配列デザインのシンプルさから、これまでのリアルタイムPCRと同じノウハウで遺伝子検査のシステムを開発することが可能です。この技術を発展させ、ウイルスなどの病原体に由来する低コピー数DNA、RNAの定量的検出、融解曲線解析における1塩基多型(SNP)の遺伝子型判別[8]、がん治療における分子標的薬の患者適合性の診断(投薬前の遺伝子変異検査)などへの応用が期待できます。今後Eprobeが、臨床での革新的な診断法の開発だけでなく、細胞イメージングと組み合わせることにより生命現象の機能解明を牽引するライフサイエンス技術となることが期待できます。
原論文情報
- Takeshi Hanami, Diane Delobel, Hajime Kanamori, Yuki Tanaka, Yasumasa Kimura, Ayako Nakasone, Takahiro Soma, Yoshihide Hayashizaki, Kengo Usui, Matthias Harbers. "Eprobe Mediated real-time PCR Monitoring and Melting Curve Analysis".
PLOS ONE, 2013 doi:10.1371/journal.pone.0070942
発表者
理化学研究所
ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 オミックス応用技術研究グループ 核酸診断技術開発ユニット
ユニットリーダー 臼井 健悟 (うすい けんご)
研究員 花見 健志 (はなみ たけし)
お問い合わせ先
ライフサイエンス技術基盤研究センター
チーフ・サイエンスコミュニケーター 山岸 敦(やまぎし あつし)
Tel: 078-304-7138 / Fax: 078-304-7112
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.理研ベンチャー
理研の研究成果を中核技術として起業し、一定の要件を満たすことで理研から認定を受けた企業。理研ベンチャーでは、最先端で活躍する理研の研究者が自然科学における研究テーマを追求する過程で考案した「新しい知見や技術」を日常の暮らしや産業技術に役立てることを目指し、研究成果の迅速な実用化と普及に取り組んでいる。現在22社が活動している。 - 2.リアルタイムPCR法
PCR法では、増幅対象(テンプレート)のDNA、DNA合成酵素(DNAポリメラーゼ)および大量のプライマーと呼ばれるオリゴヌクレオチドを予め混合し、これにDNAポリメラーゼが働くと、結合したプライマーの3’端を起点として1本鎖部分と相補的なDNAが合成される。DNAが合成された後、再び高温にしてDNA変性から繰り返す。PCR法は、DNA鎖長の違いによる変性とアニーリングの違いを利用して、温度の上下を繰り返すだけでDNA合成を繰り返し、DNAを増幅する技術である。リアルタイムPCR法は蛍光プローブを共存させ、反応の進行を蛍光シグナルの増減をリアルタイムで確認することができる。 - 3.蛍光共鳴エネルギー移動(Fluorescence resonance energy transfer:FRET)
近接した2個の色素間で励起エネルギーが、電子の共鳴により直接移動する現象。このため、片方の色素(供与体)で吸収された光のエネルギーによって他方の色素(受容体)にエネルギーが移動し、受容体側の色素から蛍光が放射される。 - 4.励起子相互作用を持つ人工核酸
理化学研究所の岡本晃充博士(現:東大教授)が開発した、標的核酸への結合の有無に応じて可逆的な蛍光のオン・オフを行う人工核酸。いくつかの蛍光色素が集合して平行型会合体(H会合体)を形成すると消光を示す励起子相互作用を利用している。これは、色素の双極子の配向に基づく励起軌道の分裂に起因する。H会合体の場合は、分裂した励起軌道のうち上位が許容遷移、下位が禁制遷移になる。色素は、上位軌道へのみ励起されるので、吸収スペクトルの短波長移動が観察される。その励起状態は、エネルギー的に安定な下位軌道へ速やかに遷移した後、そこから基底状態へ戻ろうとする。しかし、その過程は蛍光を伴わない放熱系であるので、蛍光発光は生じない。 - 5.EGFR
上皮成長因子受容体(Epidermal Growth Factor Receptor)。分泌性の増殖因子であるEGF(上皮成長因子)が結合する細胞膜上の受容体。この変異や過剰発現は、増殖因子に依存しない細胞の増殖を引き起こし、ヒトのさまざまな癌に関与することが知られている。 - 6.Ct値
増幅が指数関数的に起こる領域で一定の増幅産物量になるサイクル。これを横軸にとり、段階希釈した既知量のDNAをスタンダードにして、縦軸にプロットし、検量線を作成する。未知濃度のサンプルについても、同じ条件下で反応を行い、Ct値を求め、この値と検量線から、サンプル中の目的のDNA量を測定する。 - 7.Tm値
DNA2本鎖が1本鎖に解離する温度。センス鎖側に1塩基のミスマッチが生じると、アンチセンス鎖との親和性がフルマッチの場合に比べ下がるので、結果としてTm値が低下する。 - 8.1塩基多型(SNP)の遺伝子型判別
ヒトゲノムは30億塩基対のDNAから構成されているが、個々人を比較するとそのうちの0.1%の塩基配列に違いがあると見られ、これを遺伝子多型と呼ぶ。遺伝子多型のうち、1つの塩基が他の塩基に変わるものを一塩基多型(SNP)と呼ぶ。これにより遺伝子をもとに体内で作られる酵素などのタンパク質の働きが微妙に変化し、病気のかかりやすさや医薬品への反応に変化が生じる。SNPの遺伝子型判別はこれを解析する手法。
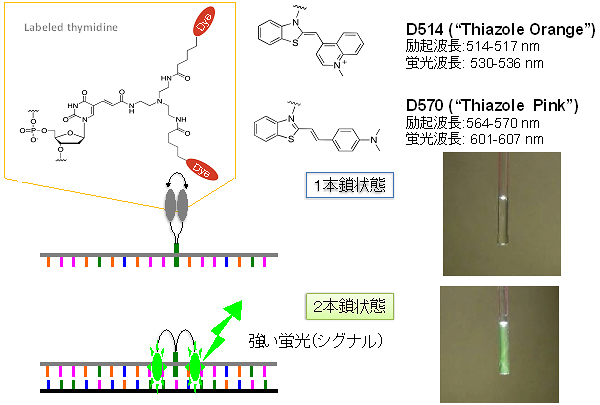
図1 配列特異的な認識を行なうEprobe
Eprobeはチミン塩基に2つの蛍光色素(Dye)を持つ。今回使用した蛍光色素は、蛍光色が緑色のD514(チアゾールオレンジ)と蛍光色が橙色のD570(チアゾールピンク)。図右上の写真は、励起子相互作用が働いて蛍光発光が抑制されている状態。1本鎖の状態では蛍光を発しないが、ターゲットのDNA配列と2本鎖を形成することによって強い蛍光シグナルを示す。
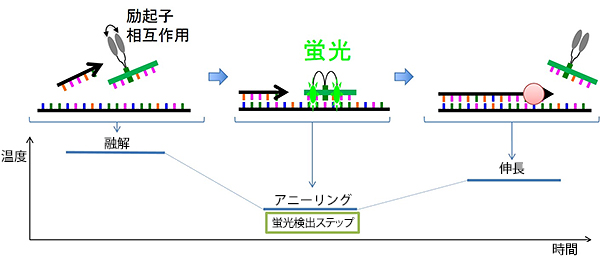
図2 Eprobe-PCRの概要
Eprobeは温度を下げてプライマーがターゲット配列に結合するアニーリングのステップにおいて、ターゲットのDNA鎖に結合し蛍光シグナルを発する。
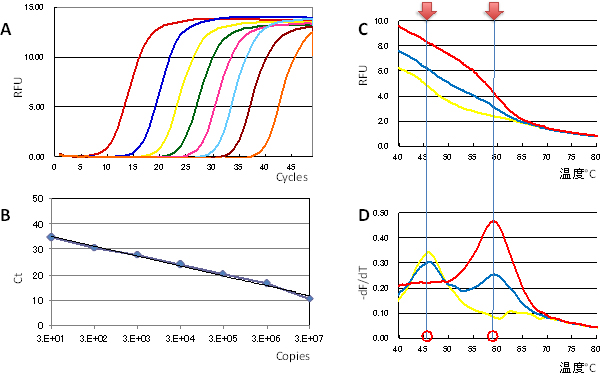
図3 Eprobeを用いたリアルタイムPCRでの増幅の定量検出と融解曲線解析
- A.異なる量のDNAに対する増幅曲線。縦軸は蛍光の強さで示されるPCR産物の量、横軸はPCR反応のサイクル数。グラフの各色は、一番左側にある赤線の基準のサンプル量(1.5×108コピー)から10倍ごとの段階希釈を示す。
- B.Aのグラフから読み取ったCt値と、その時のサンプルDNA量の対数を横軸としたグラフ。Ct値からDNAの定量解析が可能であることを示す。
- C.野生型配列のEprobeに対して、野生型(赤)、変異型(黄)、野生と変異のヘテロ型(青)のそれぞれを鋳型とするPCR反応での融解曲線。
- D.Cを一次微分したデータのグラフ。野生型のDNA配列ではピークが高温側に、変異型の場合にはピークが低温側に出現した。
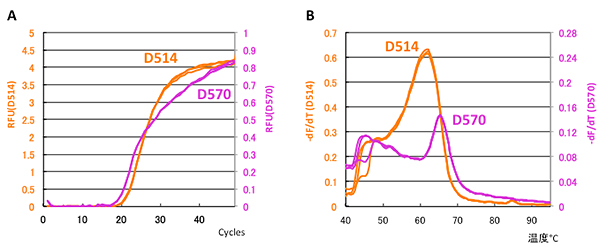
図4 D514とD570の2つの蛍光色素を用いたEprobeを用いたマルチプレックスPCRの結果
異なる2つの遺伝子配列をターゲットとした解析結果。(A)は増幅曲線、(B)は融解曲線の解析。Eprobeの2つの蛍光色素(D514とD570)、それぞれの増幅曲線及び融解曲線を同時に検出できていることが分かる。これにより、EprobeがマルチプレックスPCRにも応用できることが示された。
