ポイント
- タンパク質に糖鎖結合する機能とは逆の糖鎖分解反応も触媒することを発見
- OSTの触媒機能を担う部位が、この相反する2つの触媒を行う
- OSTの反応制御機構が分かれば活性低下による疾患の治療薬開発につながる
要旨
理化学研究所(理研、野依良治理事長)は、酵母において、糖鎖の結合(糖鎖修飾)を触媒する酵素「オリゴ糖転移酵素(OST)」が、本来のタンパク質の糖鎖修飾を触媒する機能だけでなく、それとは逆の分解活性の触媒機能も持ち、遊離糖鎖を生成することを明らかにしました。これは、理研グローバル研究クラスタ(玉尾皓平クラスタ長)理研-マックスプランク連携研究センター糖鎖代謝学研究チームの鈴木匡(ただし)チームリーダー、原田陽一郎特別研究員と、スイス連邦工科大学チューリッヒ校のマーカス エイビ(Markus Aebi)教授らによる共同研究グループの成果です。
糖鎖は、タンパク質や脂質などの生体分子に結合し、それら分子の性質を変化させたり、機能を付加するなど重要な役割を担っています。主に細胞小器官の1つである小胞体の内腔でさまざまな糖鎖修飾が行われ、糖鎖の種類によってタンパク質の品質管理や細胞内輸送、細胞間コミュニケーションなど、さまざまな生命活動の制御に関与します。ヒトや酵母を含む多くの真核生物では、複数の膜タンパク質から構成されるOSTが糖鎖修飾を触媒します。その時、OSTは小胞体膜上に存在するドリコール脂質[1]に構築された糖鎖(ドリコール結合型糖鎖)をひとまとめにタンパク質に結合させるユニークな性質を持つことが知られています。
正常な糖タンパク質は適切な場所へ輸送されますが、異常な糖タンパク質は細胞質に輸送されます。そこで、糖鎖を切り離す酵素「ペプチド:N-グリカナーゼ(PNGase)」によって糖鎖が取り除かれ、細胞質には切り離された糖鎖(遊離糖鎖)が生成されます。しかし、過去の研究から小胞体内腔にも遊離糖鎖が生成されることが知られており、その生成過程は長年不明のままでした。そこで、共同研究グループは、PNGaseに依存しない遊離糖鎖とOSTの関係性について、遺伝学および生化学的な手法を用いて検証を行いました。
OSTの触媒機能を低下させた変異酵母を作成して、遊離糖鎖の生成量を調べたところ、小胞体内の遊離糖鎖生成量が減少することが分かりました。さらに出芽酵母から精製したOSTとドリコール結合型糖鎖を混合し、試験管内で遊離糖鎖の生成反応を解析しました。その結果、OSTとドリコール結合型糖鎖の両者が存在するときだけ遊離糖鎖が生成されることが分かりました。これらの結果から、OSTはドリコール結合型糖鎖を分解して遊離糖鎖を生成することが明らかとなり、長年不明だった小胞体内の遊離糖鎖の生成機構の一端を解明できました。OSTの本来の機能はタンパク質の糖鎖修飾を適切に行うことですが、その機能とは逆の分解反応も触媒することが本研究によって明らかになりました。
最近、OSTの触媒を担うタンパク質をつくる遺伝子の変異が、先天性糖鎖合成異常症と呼ばれる全身性の重篤な症状を呈する病気の原因となることが明らかにされています。さらに知見を積み重ねることで、この病気の治療薬創出につながると期待できます。今後、OSTの糖鎖修飾活性と分解活性がどのように制御されているか、その分子機構の解明を目指します。
本研究成果は、米国の科学雑誌『The Journal of Biological Chemistry』に掲載されるに先立ち、オンライン版に掲載されました。
背景
糖鎖は、グルコースのような単糖が複数個連なってできており、タンパク質や脂質などの生体分子に結合し、それら分子の性質を変化させたり、機能を付加するなど生体内で重要な役割を担っています。糖鎖が生体分子に結合することを「糖鎖修飾」と呼び、糖鎖と生体分子の修飾の組み合わせは多数存在します。この糖鎖修飾は、細胞小器官のうちの1つである小胞体の内腔で行われます。糖鎖修飾の代表例として、アスパラギン結合型糖鎖修飾がよく知られています。糖鎖は、タンパク質が合成される過程で、そのタンパク質に含まれる特定のアスパラギン残基に付加されます。修飾される糖鎖の種類などによってタンパク質の品質管理や細胞内輸送、細胞間コミュニケーションなど、重要な生命活動に関与します。
アスパラギン結合型糖鎖修飾は、小胞体内腔に存在する「オリゴ糖転移酵素(OST)」によって触媒され、糖鎖の結合反応が進行します。OSTの構造は、真核生物に属する出芽酵母から哺乳動物に至るまで類似しています。複数のタンパク質(サブユニット)で構成されており、酵素活性を担う触媒サブユニットを1つ含む複合体酵素です。また、OSTは小胞体膜上に存在するドリコール脂質に構築された糖鎖(ドリコール結合型糖鎖)をひとまとめにタンパク質に結合させる非常にユニークな性質を持ちます。
糖鎖修飾された糖タンパク質は、小胞体内腔において立体構造が整えられ、適切な場所に輸送され、機能します。一方、構造が正しく整わなかった異常な糖タンパク質は、細胞質へ輸送され、タンパク質の分解を担うプロテアソームに運ばれることで、異常なタンパク質を排除しています。この時、タンパク質に付加された糖鎖はプロテアソームに運ばれる前に糖鎖を切り離す酵素ペプチド:N-グリカナーゼ(PNGase)によってまるごと取り除かれ、細胞質内に遊離状態の糖鎖(遊離糖鎖)が生成されます。
これまでの研究から、出芽酵母においてPNGaseを合成する遺伝子(PNGase遺伝子)を欠損させると遊離糖鎖の95%程度が消失することが知られています。このことから、出芽酵母のほとんどの遊離糖鎖は、PNGaseによって糖タンパク質から切り離されることで生成されていると考えられます。一方、残りの5%の遊離糖鎖がどのように生成されているのかは全く分かっていませんでした。興味深いことに、哺乳動物の細胞の小胞体内腔において遊離糖鎖が生成されることが知られていましたが、この遊離糖鎖の由来も長年明らかにされていませんでした。また、過去の研究から、小胞体内腔における遊離糖鎖の生成反応の性質がOSTの糖鎖修飾反応に似ていることが知られていましたが、決定的な実験的証拠はありませんでした。
そこで、共同研究グループは、出芽酵母にはPNGaseに依存しないもう1つの遊離糖鎖の生成経路が存在することに着目し、PNGase非依存的な遊離糖鎖がOSTによって生成されるのかどうか、遺伝学および生化学的な手法を用いて検証を行いました。
研究手法と成果
まず、PNGase遺伝子を欠損させた変異酵母において、生成される遊離糖鎖の構造および細胞内の局在を詳細に調べました。その結果、遊離糖鎖は小胞体内腔で生成されることが分かりました。
次に、「小胞体内腔に見いだされる遊離糖鎖はOSTが生成する」という仮説を立て、その検証を行いました。出芽酵母のOSTは、触媒サブユニットを含め8つの膜タンパク質で構成されています。その内、触媒サブユニットを含む5つのタンパク質は酵母の生育に必須ですが、残りの3つのタンパク質は酵母の生育に必須ではないものの、OSTの最適な酵素活性に必要であることが分かっています(図1)。そこで、生育に必須ではないOSTサブユニットの1つとPNGase遺伝子を欠損させた変異酵母を用いて、小胞体内の遊離糖鎖の生成量を比較しました。その結果、OSTの糖鎖修飾活性が低下すると、遊離糖鎖の生成量も減少することが分かりました。
出芽酵母における糖鎖修飾の効率はドリコール結合型糖鎖の構造に大きく左右されます。これは、OSTが成熟型ドリコール結合型糖鎖を優先的に認識するため、未成熟なドリコール結合型糖鎖の場合は、糖鎖修飾効率が低下します。つまり、ドリコール結合型糖鎖の構造を未成熟型にした際に、遊離糖鎖の生成量が減少すれば、OSTがその生成に関わっていることを示す更なる証拠となります。未成熟型ドリコール結合型糖鎖が蓄積する変異酵母において遊離糖鎖を調べたところ、その生成量が減少していました。
また、OSTがドリコール結合型糖鎖を分解して遊離糖鎖を生成するかどうかを検証するため、出芽酵母から精製したOSTとドリコール結合型糖鎖を混合し、試験管内における遊離糖鎖の生成反応を解析しました。その結果、OSTとドリコール結合型糖鎖の両者が存在するときだけ、遊離糖鎖が生成することが分かりました。これらの結果から、OSTはドリコール結合型糖鎖を分解して遊離糖鎖を生成することが明らかとなり、長年不明だった小胞体内腔の遊離糖鎖生成の分子機構を初めて明確に示すことができました。また、この反応は糖鎖修飾反応と競合的であることが分かりました。
OSTの糖鎖修飾反応の触媒機能を担うサブユニットは、Stt3と呼ばれる複数回膜貫通型タンパク質です。共同研究グループは、OSTによるドリコール結合型糖鎖を介した遊離糖鎖の生成がStt3によって触媒されるかどうかを明らかにするため、原虫であるリーシュマニア(Leishmania major)の糖鎖修飾システムに着目しました。リーシュマニアは4種類のStt3(Stt3A~D)だけを持ち、未成熟型ドリコール結合型糖鎖でも糖鎖修飾反応が進行することが知られています。そこで、リーシュマニアのStt3Dを未成熟型ドリコール結合型糖鎖が蓄積する変異酵母に入れたところ、遊離糖鎖が顕著に増加することを見いだしました。この結果は、触媒サブユニットであるStt3が遊離糖鎖の生成を触媒することを示しています(図2)。
今後の期待
OSTの本来の機能はタンパク質の糖鎖修飾を適切に行うことですが、その機能とは逆の分解反応も触媒することが本研究によって明らかになりました。近年、Stt3の遺伝子変異によって糖鎖修飾活性の低下により、先天性糖鎖合成異常症という全身性の重篤な疾患が引き起こされることが明らかになってきています。OSTの糖鎖修飾活性と分解活性を制御する因子の同定を行うことによってOSTの反応制御機構を明らかにできれば、OSTの活性低下が原因で起こる新たな疾患の治療薬創出の一助になるかもしれません。
また、哺乳動物と出芽酵母では遊離糖鎖の生成メカニズムに大きな違いがあり、出芽酵母ではOST由来の糖鎖は全体の5%程度であるのに対し、哺乳動物ではPNGase遺伝子を欠損させても遊離糖鎖の量に変化は見られず、ほとんどの糖鎖はOST由来であると考えられます。なぜ生物種によってこのような制御の違いがあるのか、また特に哺乳動物でOST由来の糖鎖がなぜ大量に作られるのか、その生理的意義を明らかにすることは今後に残された興味深い研究テーマであるといえます。
原論文情報
- Yoichiro Harada, Reto Buser, Elsy M. Ngwa, Hiroto Hirayama, Markus Aebi and Tadashi Suzuki.
"Eukaryotic oligosaccharyltransferase generates free oligosaccharides during N-glycosylation" The Journal of Biological Chemistry, 2013,doi: 10.1074/jbc.M113.486985
発表者
理化学研究所
グローバル研究クラスタ 理研-マックスプランク連携研究センター システム糖鎖生物学研究グループ 糖鎖代謝学研究チーム
チームリーダー 鈴木 匡 (すずき ただし)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ドリコール脂質
糖鎖修飾の際に脂質キャリアとして用いられるポリプレノール類の1種で、小胞体膜に挿入されている( 図2参照)。末端に1級アルコールを持ち、ここにピロリン酸を介して糖鎖が構築される。
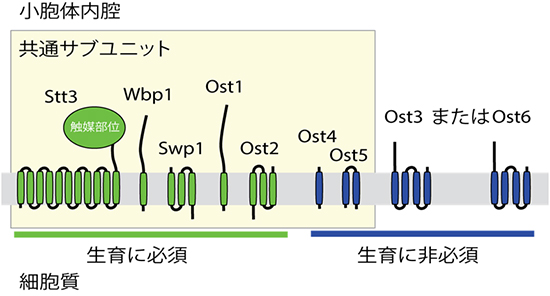
図1 出芽酵母OSTのサブユニットの構造
出芽酵母のOSTは8つの膜タンパク質から構成される。そのうち、5個のタンパク質(Stt3, Wbp1, Swp1, Ost1およびOst2)をつくる遺伝子は生育に必須である。一方、残りの3個のタンパク質(Ost4, Ost5およびOst3またはOst6)をつくる遺伝子は、生育には必須ではないものの、OSTの活性に必要である。OST複合体は2種類存在し、7つの共通サブユニット(黄色枠内)にOst3またはOst6が付加される。これら2種類のOST複合体は、糖鎖修飾を受けるターゲットタンパク質に対して異なる特異性を示す。Stt3タンパク質は全ての生物ドメイン(真核生物、真性細菌および古細菌)において高度に保存されたOSTの触媒サブユニットで、小胞体内腔に触媒部位を持つ。しかし、その他のOSTサブユニットの機能はほとんど分かっていない。

図2 OSTが触媒する糖鎖修飾と分解反応
出芽酵母においてOSTは複数の膜タンパク質から構成され(OST複合体)、Stt3タンパク質が触媒部位を有する。小胞体膜の細胞質表面に結合したリボソームによって翻訳途中の新生ポリペプチド鎖は、チャネルを通って小胞体内腔へ輸送される。その際、特定のアスパラギン残基(Asn)が存在した場合、OSTがドリコール結合型糖鎖からその糖鎖部分をAsn残基にひとまとめに転移する(糖鎖修飾)。一方、OSTはドリコール結合型糖鎖を加水分解する活性も有する(加水分解)。
