ポイント
- 独自に開発した最先端の分光計測法により界面の水構造を直接観察
- 陽イオンのホフマイスター系列は界面の水の水素結合強度の序列と一致
- 陽イオンと陰イオンではホフマイスター系列発現メカニズムが異なる
要旨
理化学研究所(理研、野依良治理事長)は、独自に開発した表面・界面に存在する分子を選択的に計測できる最先端の分光計測法を用いて、広い分野で重要とされているホフマイスター系列[1]の発現メカニズムについてモデル界面を用いて調べました。その結果、陽イオンのホフマイスター系列と陰イオンのホフマイスター系列の発現メカニズムが異なる可能性を示唆しました。これは、理研田原分子分光研究室の二本柳聡史研究員と山口祥一専任研究員、田原太平主任研究員らの研究グループによる成果です。
19世紀末にホフマイスター[1]によって報告された、タンパク質の溶解度に及ぼす塩効果の序列はホフマイスター系列として知られています(図1)。この系列は元々はタンパク質の塩析[2]に対して発見されたものですが、酵素活性のような複雑な生体機能から界面活性剤の相変化のような単純な物性にいたるまで非常に多くの溶質の多様な物性に共通しています。そのため、ホフマイスター系列を理解することは生物物理および物理化学の広範な学問領域において非常に重要であり、世界中で研究されています。しかし、膨大な数の研究がなされてきたにもかかわらず、その分子レベルの詳細なメカニズムについてはほとんど分かっていません。最近では、ミクロレベルではホフマイスター塩効果はタンパク質や単分子膜などの分子系とイオンが溶けた水溶液との間の界面の問題に起因すると考えられています。そのため、この現象の解明には界面の構造を分子レベルで理解することが求められていました。
研究グループは、独自に開発したヘテロダイン検出振動和周波発生分光法[3]を用いて単分子膜/水界面の水分子の振動スペクトル[4]の測定を行いました。その結果、正に帯電した界面における陰イオンの効果はイオンの界面への吸着力で説明できるのに対して、負に帯電した界面における陽イオンの効果は吸着力ではなく界面近くの水の水素結合強度[5]の変化と関連があることを見いだしました。この結果は、水の科学に画期的な知見を与えると同時に、界面の水構造の知見が鍵となる生物物理などの分野にも新しい視点を与えると期待できます。本研究成果は、米国の学術誌『Journal of The American Chemical Society』に近日掲載予定です。
背景
タンパク質の溶解度に及ぼす塩効果の序列はホフマイスター系列として知られています。この系列はタンパク質の塩析のみならず、塩溶液の表面張力のようにタンパク質やその他の巨大分子が存在しない系でも共通してみられるため、広い分野で興味を持たれています。かつてはホフマイスター系列の発現メカニズムは主にイオンと水の相互作用で決定されているという考えが主流でした。しかし研究の進展により、イオンが溶けた時の水の構造(水分子の配列やつながり方)とホフマイスター系列の間には直接的な相関がないことが分かってきました。そして最近では、ホフマイスター塩効果はミクロレベルではタンパク質や単分子膜などの大きな分子または分子系とイオンが溶けた水溶液との間の界面の問題であると考えられるようになっています。したがってホフマイスター系列の発現メカニズムを理解するには、まず、界面の水分子の性質を理解することが重要です。しかし、現在でも界面の分子構造を調べることは容易ではなく、特に水のミクロな構造についてはほとんど分かっていません。
界面の水の構造を調べるほとんど唯一の実験方法が、非線形分光計測の一種である振動和周波発生分光法です。この方法を用いると、液体内部にある圧倒的多数の水分子を“無視”して界面に存在する水分子だけの情報を得ることができます。この方法を用いて過去に行なわれた実験結果は、陰イオンのホフマイスター系列が陰イオンと界面の吸着力と強い相関を示すことを示唆していました。しかし、陽イオンのホフマイスター系列が同様に吸着力で説明できるか、あるいはかつて主流だった水の構造はどのように関係しているかという点については不明なままでした。
研究手法と成果
研究グループは、自ら開発した新しい分光法「ヘテロダイン検出振動和周波発生分光法」と同位体希釈法[6]をこの問題に適用しました。この方法は界面分子だけを選択的に計測可能なため、界面分子の配向と構造を決定できます。研究グループは、この方法を用いて、正および負に帯電したイオン性界面活性剤単分子膜と種々の塩水溶液の界面における水の構造とホフマイスター系列との関係を調べました。その結果、正に帯電した界面での陰イオンのホフマイスター系列は界面の陰イオンの吸着力と非常に良く一致していました。これはこれまでの研究と同じ結果です。その一方で、負に帯電した界面における陽イオンの効果は界面と陽イオンの接触吸着による直接的な相互作用では説明できないことが分かりました。代わりに負に帯電した界面における水の水素結合強度と陽イオンのホフマイスター系列には明確な相関があることが強く示唆されました(図2)。このような結果を元に、ホフマイスター系列は、①界面と対イオンが接触吸着する場合はその吸着力(会合定数)、②界面と対イオンが接触吸着しない場合は、界面の水の水素結合強度というように、2つの因子が複合的に働いて決定されていると結論しました。
今後の期待
今回の成果は、水界面の分子科学研究に対して画期的な新しい知見を与えると同時に、100年以上謎であったホフマイスター系列の発現に関する有力なメカニズムの提案となります。今回調べたのは界面活性剤の界面におけるホフマイスター塩効果ですが、より生体に近いモデル界面を調べることによって、今後、タンパク質のホフマイスター系列の発現メカニズムの全容を解明できる可能性があります。また、今回の研究で界面における水素結合構造の重要性が理解されたことで、生物物理やタンパク質の研究者に対し新しい指針を与えることも期待できます。
原論文情報
- Nihonyanagi, Satoshi; Yamaguchi, Shoichi; Tahara, Tahei. “Counterion Effect on Interfacial Water at Charged Interfaces and Its Relevance to the Hofmeister Series”. Journal of the American Chemical Society, 2014, doi: 10.1021/ja412952y
発表者
理化学研究所
主任研究員研究室 田原分子分光研究室
主任研究員 田原 太平(たはら たへい)
研究員 二本柳 聡史(にほんやなぎ さとし)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ホフマイスター系列、ホフマイスター
ホフマイスター系列とは、1988年にドイツの化学者フランツ・ホフマイスターによって提唱された水溶液系の物理現象に及ぼす各イオンの影響力を並べたもの。詳細は 図1を参照。 - 2.塩析
水に塩MXを加えるとその塩はプラスの電荷を持つ陽イオンM+と負の電荷を持つ陰イオンX-に分離(電離という)して水に溶ける。ある物質Aの水溶液に多量の塩を加えると塩が水に溶けるとともに元々溶けていた物質Aの溶解度が低下し、物質Aが析出する現象を塩析という。 - 3.ヘテロダイン検出振動和周波発生分光法
振動和周波発生分光法は二次非線形分光法の中で最も利用されている分光法。液体や高分子フィルムの界面構造や生体膜の構造解析などに使われている。周波数Aのレーザー光を可視光、周波数Bのレーザー光を赤外光とし、これらを試料に照射して発生する和の周波数(A+B)の持つ光信号を検出する。ほとんどの物質の内部ではA+Bの振動数を持つ信号が生じず、界面でのみ生じるという性質があるため、この方法を用いると物質の界面だけを選択的に調べることができる。従来の方法はホモダイン検出と呼ばれる方式で、信号光の強さのみを測定していた。理研田原分子分光研究室が2009年に開発したヘテロダイン検出の振動和周波発生分光法を用いると、信号光の強度とともにその位相を決定しながら高い質の界面の振動スペクトルを測定できる。これにより、界面の分子についても物質内部と同レベルの詳細な情報が得られるようになった。 - 4.振動スペクトル
分子がどのような振動数で振動しているかを示すグラフ。分子の振動数は、その分子の状態や周りの環境に対して鋭敏に変化するので、このグラフを測定し、解析することで詳細な分子についての情報が得られる。 - 5.水素結合
分子の中で酸素や窒素など電子を引きつけやすい原子と共有結合した水素原子は、電子を引っ張られて弱い正電荷を帯びる。このような水素と、別の分子の弱い負電荷を帯びた原子が近づくと、それらの間に共有結合の10分の1程度の弱い結合が生じる。これを水素結合と呼ぶ。水分子の場合、隣接する水分子と4つの水素結合を作ることができる。 - 6.同位体希釈法
同位体は化学的性質がほぼ同じで、重さだけが異なる原子。普通の水は軽水素原子(H)2つと酸素原子(O)1つから形成されている(H2O)。これに対し、重水は重水素原子(D)2つと酸素原子(O)1つの組み合わせでできている(D2O)。比較的少量のH2OをD2Oで希釈すると、希釈した水の中では軽水素と重水素の交換が起きてHOD分子が生成される。H2Oの分子は1つの分子に2つのOHが存在するために分子内の相互作用によって振動スペクトルが複雑化することがあるが、HODは1つの分子に1つのOHしかないのでそのような相互作用がなくスペクトルが直接的に理解しやすい。このような同位体希釈は振動スペクトルを簡単にして解釈しやすくする目的でよく用いられる。
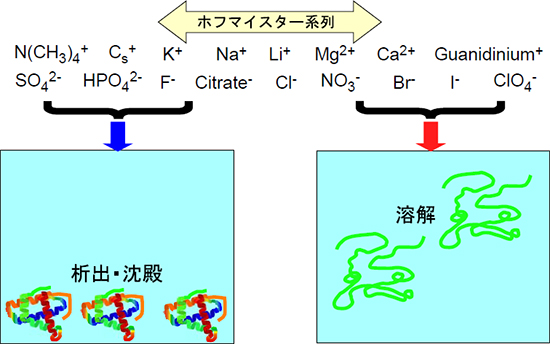
図1 ホフマイスター系列の概念図
上部に示すイオンのうち左側に示すイオンはタンパク質の溶解度を下げる働きをするため水に溶けていたタンパク質を析出・沈殿させる。中央に位置するイオンでは沈殿させる効果が小さくなり、右側のイオンは逆にタンパク質の溶解度を上げる働きをする。このようにイオンを加えた時に水溶液の性質がどれだけ変化するかの序列はホフマイスター系列と呼ばれ、非常に多くの溶質の多様な物性に共通してみられる。
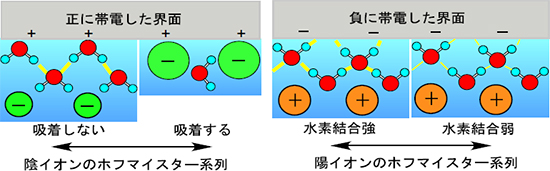
図2 今回の実験から示唆された界面の構造
正に帯電した界面においては静電引力が働くため陰イオンが界面近くに集まる。図1に示すホフマイスター系列の左側のイオンは界面に接触しないのに対して右側のイオンほど界面に接触吸着しやすい。一方、負に帯電した界面においては陽イオンが界面近くに集まるが、いずれの陽イオンも界面に接触吸着はしない。この場合、負に帯電した界面と左側の陽イオンの間にある水分子は充分に強い水素結合をしているのに対して右側の陽イオンの間にある水分子は水素結合が弱まっている。
