ポイント
- 炎症や免疫応答の要分子NF-kappaBには細胞状態を決定するいき値が存在
- 細胞内情報の増幅機構によりいき値が決定される
- 増幅機構は一つひとつのアナログな細胞活性をデジタル(0か1)に変換する
要旨
理化学研究所(理研、野依良治理事長)は、炎症や免疫応答の要となる転写因子「NF-kappaB(NF-κB)[1]」の閾値(いき値)[2]を決定する分子機構を明らかにしました。細胞内情報の増幅機構がアナログな分子情報をデジタル(0か1)に変換し[3]、1細胞ごとのNF-κBのいき値を決定することが分かりました。これは、理研統合生命医科学研究センター(小安重夫センター長代行)統合細胞システム研究チームの篠原久明研究員らと岡田眞里子チームリーダー、理研佐甲細胞情報研究室(佐甲靖志主任研究員)の廣島通夫研究員、理研生命システム研究センター(柳田敏雄センター長)、カリフォルニア大学らの共同研究グループの成果です。
転写因子は細胞や組織の性質、病態を決定するという重要な役割を持ちます。炎症や免疫応答においては、NF-κBが細胞の状態をつかさどっています。NF-κBの活性が十分でない場合は免疫不全、逆に過剰に活性化されると自己免疫疾患やがんを引き起こすことが知られています。このことから、NF-κBには適切な活性の範囲と活性化の有無を決定するいき値があるのではないかと考えられていました。しかし、多くの研究者がこの課題に取り組んだにも関わらず、その分子機構は全く分かっていませんでした。
共同研究グループは、免疫細胞の1つであるB細胞の情報伝達経路「CARMA1-TAK1-IKK[4]」に注目し、この経路について詳細な分子動態の計測を行い、数理モデリングにより解析しました。その結果、経路内に存在する細胞内情報を増幅する正のフィードバック[5]が、B細胞受容体のアナログの分子情報をデジタル(0か1)活性に変換し、1細胞ごとにNF-κBのいき値を決定していることが分かりました。NF-κBの活性化に関わるリン酸化酵素「IKK[4]」の異常と疾病との関連はすでに広く知られていますが、本研究ではアダプター分子「CARMA1[4]」の重要性も明らかになりました。CARMA1の遺伝子異常は、がんやアトピー性皮膚炎の発症にも関与することが臨床データからも明らかであり、本研究成果はこれらの疾病の発症機構を解く鍵になると期待できます。
本研究は、文部科学省 革新的細胞解析研究プログラム(セルイノベーション)プロジェクトおよび内閣府/日本学術振興会 最先端研究開発支援プログラム 合原最先端数理モデルプロジェクトの成果で、米国の科学雑誌『Science』(5月15日号)に掲載されます。
背景
転写因子は細胞や組織の性質、病態を決定するという重要な役割を持ちます。炎症や免疫応答においては、転写因子「NF-kappaB(NF-κB)」が細胞の状態をつかさどっています。NF-κBの活性が十分でない場合は免疫不全、逆に過剰に活性化されると自己免疫疾患やがんを引き起こすことが知られています。このことから、NF-κBには適切な活性の範囲と活性化の有無を決定する「閾値(いき値)」があるのではないかと考えられていました。しかし、多くの研究者がこの課題に取り組んだにも関わらず、その分子機構は全く分かっていませんでした。
研究グループは2007年、リン酸化酵素のIKKに着目し、B細胞(免疫細胞)内の情報伝達経路「CARMA1-TAK1-IKK」がNF-κBの活性化を正にフィードバック制御していることを発見しました(図1)注)。そこで研究グループは、NF-κBの活性化のいき値決定における、このフィードバックの役割を実験解析および数理モデリングを用い詳しく調べることにしました。
- 注)
2007年12月17日プレスリリース
免疫の要「NF-κB」の活性化シグナルを増幅する機構を発見
研究手法と成果
実験では、TAK1遺伝子を欠損したマウス脾臓由来のB細胞を用い、B細胞受容体を刺激して分子の活性を調べました。その結果、TAK1[4]が欠損するとIKKの活性化がほとんど起きず、NF-κBによって誘導されるはずの遺伝子発現活性が低下することが明らかになりました。さらに詳細に調べるため、トリ由来のB細胞株を用いて、B細胞受容体刺激後のTAK1とIKKの活性を90秒間隔で計測したところ、IKKは刺激後6分で活性のピークに達するのに対し、TAK1の活性は1.5分後と6分後の2回、ピークが存在することが分かりました。
次に、この一見矛盾するように見える分子動態の制御メカニズムを理解するために、数理モデリングの手法を用いてTAK1とIKKの活性化機構を解明することにしました。TAK1がリン酸化したCARMA1と複合体を形成しIKKを活性化するステップ、IKKが自己リン酸化するステップ、さらにCARMA1を介した正のフィードバックループなどを数理モデルに組み込むことによって、前述の実験結果を数理モデルで説明することに成功しました。この数理モデルを用いた詳細なコンピュータシミュレーションの結果、TAK1がCARMA1のリン酸化を介してIKK活性を増幅する正のフィードバック制御を行い(図1)、これがNF-κBのいき値を決定していることが示唆されました。
そこで、この機構によるNF-κBのいき値活性制御を1細胞レベルで検証しました。B細胞受容体を刺激したところ、通常のB細胞株では、一定の刺激量以上でNF-κBの核内移行がデジタル(0か1)に制御されている、つまりいき値が存在することが認められました(図2)。しかし、CARMA1のリン酸化部位に変異を導入し、正のフィードバックループを切ると、NF-κBの核内移行は刺激の強さに段階的に反応するアナログな応答に変化することが明らかになりました。
これらから、情報伝達経路であるCARMA1-TAK1-IKKの正のフィードバック機構が、B細胞受容体のアナログの情報をデジタル(0か1)活性に変換し、1細胞ごとにNF-κBのいき値を決定していることが分かりました。
今後の期待
本研究により、NF-κBの活性化のいき値決定にはIKKだけでなくTAK1やCARMA1といった分子も重要であることが分かりました。最近のゲノムワイド関連解析の結果からも、CARMA1の遺伝子異常は、がんやアトピー性皮膚炎のような炎症に関与することが分かっており、本研究で得られた知見はこれらの疾病に対する新しい治療や薬剤の開発に役立つと期待できます。
発表者
理化学研究所
統合生命医科学研究センター 統合細胞システム研究チーム
チームリーダー 岡田 眞里子(おかだ まりこ)
お問い合わせ先
統合生命医科学研究推進室
Tel: 048-503-9117 / Fax: 048-462-4715
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.NF-kappaB(NF-κB)
nuclear factor kappa-light-chain-enhancer of activated B cells。炎症、感染などの免疫応答をつかさどるタンパク質としてデビッド・バルチモアらにより1986年に発見された。NF-κBはもともと免疫細胞のB細胞中に発見されたが、現在はさまざまな細胞や組織に存在することが知られている。また免疫応答だけではなく、その過剰な活性化はがんを引き起こすとされている。 - 2.閾値(いき値)
生体物質を活性化させるために必要な最小限の刺激の値。本研究ではNF-κBを最大に活性化するために必要なB細胞受容体刺激の半量(50%)の濃度(EC50)を閾値の目安に用いた。 - 3.細胞内アナログ分子情報のデジタル変換
通常、細胞内の情報量は連続した値(アナログ)として観察される。しかし、いくつかの分子については連続値ではなく離散値(0と1の2進数:デジタル)で観測されることがある。NF-κBはそのようなデジタルな活性化を示す転写因子である可能性が以前から示唆されていた。細胞の中にはさまざまなノイズが存在しており、離散値のほうが細胞内の情報を正しく伝えることができるという考え方がある。 - 4.CARMA1-TAK1-IKK
CARMA1:B細胞のシグナル伝達を転写因子NF-κBに仲介するアダプター分子。
TAK1:リン酸化酵素セリンスレオニンキナーゼの1つ。さまざまな刺激で活性化されることが知られている。
IKK:リン酸化酵素セリンスレオニンキナーゼの1つ。IKKα、IKKβ、IKKγ複合体として活性化することでNF-κBのインヒビター(IκB)をリン酸化する。NF-κBはIκBと複合体を形成し細胞質に留まっているが、IκBがリン酸化を受け、分解されることで核へ移行し、転写因子として機能を発揮する。
CARMA1-TAK1-IKK:B細胞内の情報伝達経路。CARMA1、TAK1、IKKが連携して細胞内で情報を伝達し、NF-κBを活性化する(図1参照)。これらシグナル伝達物質はB細胞受容体のみでなくT細胞においてもNF-κBの活性に必要な機能要素である。 - 5.正のフィードバック
誘導される反応により生じた活性が誘導した反応に戻って正の影響を持つこと。ここではCARMA1とTAK1により誘導されたIKKの活性がCARMA1とTAK1の活性をさらに増幅する効果を持つことを指す。旧来の実験では正のフィードバックに関わる分子の遺伝子欠損では全ての活性が低下するため、正のフィードバックを証明することは困難だった。数理モデリングの手法を用いることにより理論的な考察が可能となった。さらに本研究では、定量的な細胞実験を同時に行うことで、理論的な考察を実験的に証明することができた。
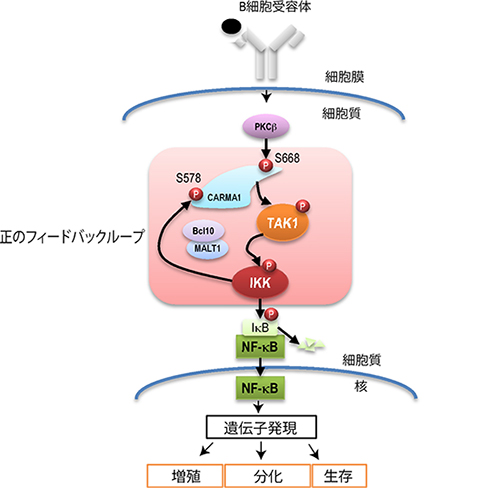
図1 B細胞受容体刺激によりNF-κBが活性化される機構
B細胞受容体が刺激を受け取り、PKCβ がCARMA1のセリン668残基をリン酸化すると、CARMA1はTAK1などの分子(Bcl10・MALT1)と複合体を形成し、さらにIKK複合体とも会合する。これにより活性化したTAK1は、IKKを活性化する。ここで、活性化したIKKは上流のCARMA1の別の部位であるセリン578残基をリン酸化し(正のフィードバック制御)、シグナルを増幅する。これにより十分な活性を得たIKKは下流のIκBをリン酸化し、リン酸化された NF-κBが分解されることで、NF-κBは核内に移行し転写因子として活性化し、増殖、分化、生存に関わる遺伝子群の発現を誘導する。
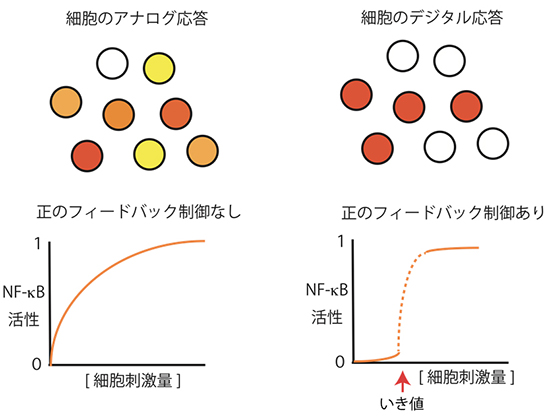
図2 細胞のアナログ応答とデジタル応答
通常、細胞内の情報量は連続した値(アナログ)として観察される(左)。しかし、いくつかの分子については連続値ではなく離散値(0と1の2進数:デジタル)で観測されることがある(右)。正のフィードバックがない細胞の場合、刺激の量に対してNF-κBの活性はアナログ(緩やかに連続した)に反応がおこる。これに対して正のフィードバックによる制御がある細胞では、一定の刺激量以上でNF-κBの活性がデジタル(0か1)に誘導される。このとき活性に必要な刺激の量、つまりいき値を認めることができる。
