要旨
理化学研究所(理研)生命システム研究センター再構成生物学研究ユニットの戎家美紀ユニットリーダー、松田充弘基礎科学特別研究員らの共同研究グループ※は、均一な細胞集団に自発的に違いを生み出す仕組みを再構成することに成功しました。
多細胞生物の体は、たった1個の受精卵が分裂を繰り返し、さまざまな種類の細胞へと分化することで形づくられていきます。同じ種類の細胞から、異なる種類の細胞を安定して作り出す仕組みの1つが、「Delta-Notchシグナル[1]」を使った隣接細胞間のコミュニケーションです。これまでの研究では、阻害剤や遺伝子破壊という方法で隣接細胞間コミュニケーションや細胞が分化する仕組みを「壊す」実験によって、Delta-Notchシグナルの関与や分化する仕組みを解明しようとする試みが主でした。しかし、壊すアプローチだけでは、現在提唱されている仮説で隣接細胞間に違いを生み出すことを十分説明できるのか、その他の要素も必要なのかを調べることは困難でした。そこで、細胞間に違いを生み出す仕組みを壊すのではなく「作る」アプローチをとることにしました。
共同研究グループは、隣接細胞間コミュニケーションの仕組みを持たない細胞の中に、Delta-Notchシグナルを単純化した人工遺伝子ネットワークを作製し導入しました。人工遺伝子ネットワークを導入した細胞は、細胞間で偶然にできる遺伝子発現量の小さな差を細胞間コミュニケーションで増幅していき、隣接細胞間に遺伝子発現状態の非対称性を作り出しました。最終的に、たった4つの遺伝子部品から成る最小限の人工遺伝子ネットワークで、隣り合う細胞を互いに異なる2種類の細胞に変えることができました。また、人工遺伝子ネットワークの一部を改変することで、2種類の細胞の比率をコントロールできることも発見しました。
生物の仕組みを人工的に再構成したことによって、隣接細胞間に違いを生み出すための最小遺伝子ネットワークが明らかになりました。また細胞種の比率を変える仕組みの一端も解明されました。これらの成果は分化の仕組みをさらに詳細に解明していくうえで役立つと期待できます。今後は、空間的パターンを含めた再構成が課題になります。
なお、本研究の一部は科学技術振興機構(JST)・さきがけ、最先端・次世代研究開発支援プログラム、科学振興調整費、新学術領域研究の支援を得て行われました。成果は、英国のオンライン科学雑誌『Nature Communications』(2月5日:日本時間2月5日)に掲載されます。
※共同研究グループ
理化学研究所 生命システム研究センター 細胞動態計測コア 再構成生物学研究ユニット
ユニットリーダー 戎家 美紀(えびすや みき)(兼JSTさきがけ研究者)
基礎科学特別研究員 松田 充弘(まつだ みつひろ)
京都大学 大学院生命科学研究科 シグナル伝達学分野
教授 西田 栄介(にしだ えいすけ)
大学院生(当時) 古賀 牧土(こが まきと)
京都大学 iPS細胞研究所
准教授 Woltjen Knut(ウォルツェン・クヌート)
背景
多細胞生物の体には多くの種類の細胞が存在しますが、元は受精卵というたった1種類の細胞に由来します。つまり、発生過程では、元は同じ種類の細胞が異なる種類の細胞へと変わる「分化」が繰り返し起こります。同じ種類の細胞は遺伝子の発現量などが似ており、対称な状態にあります。そのため、さまざまな種類の細胞を生み出すためには遺伝子の発現量に違いを生み出す仕組みが必要です。
同じ種類の細胞集団から、自発的に安定した違いを作り出す仕組みの1つが、「Delta-Notchシグナル」による隣接細胞間のコミュニケーションです。Delta-Notchシグナルとは、隣接細胞が接触し、リガンド(特定の受容体に特異的に結合する物質)である「Delta」と受容体の「Notch」が結合した時に、Notchが活性化した結果、その下流に起こるシグナル伝達のことです。特に、隣り合う細胞が互いにDelta遺伝子の発現を抑制し合うタイプの細胞間コミュニケーションは側方抑制と呼ばれます。この細胞間コミュニケーションによって、隣接細胞間に偶然起こるDelta遺伝子発現量の小さな差が増幅され、Delta遺伝子を発現する細胞と発現しない細胞が生み出されます。
これまでの研究では、遺伝子機能を阻害する薬剤や遺伝子を破壊する方法を用いて隣接細胞間コミュニケーションや細胞が分化する仕組みを「壊す」実験が主に行われ、Delta-Notchシグナルの関与や細胞分化の仕組みが調べられてきました。しかし、壊すアプローチだけでは、現在提唱されている仮説で隣接細胞間に違いを生み出すことを十分説明できるのか、その他の要素も必要なのかを調べることは困難でした。
そこで、共同研究グループは、細胞間に違いを生み出す仕組みを壊すのではなく「作る」アプローチで、細胞が自発的に分化する仕組みの解明に挑みました。
研究手法と成果
共同研究グループはまず、これまでに提唱されたDelta-Notchシグナルを介した細胞分化の仕組みを模倣し、かつできる限り単純化した人工遺伝子ネットワークを作製しました(図1左)。この人工遺伝子ネットワークは4つの遺伝子(Delta、Notch、tTS、Lfng)部品で構成され、隣接細胞間が人工的な転写抑制因子[2]「tTS」を介してDelta遺伝子の転写を抑え合う仕組みになっています。人工遺伝子ネットワークを導入する細胞には、本来はDeltaやNotchをほとんど発現していない哺乳類培養細胞である、CHO(Chinese Hamster Ovary)細胞を選びました。
人工遺伝子ネットワークを導入した1個の細胞が分裂した場合、2個の娘細胞は最初は似たDelta遺伝子の発現量を示します(蛍光タンパク質を用いて可視化)。しかし、遺伝子発現のゆらぎや細胞の形の違いなどの偶然の影響によって、娘細胞間でDelta-Notchシグナルの状態に小さな差ができ始めます。すると、Delta遺伝子の発現を互いに抑え合う仕組みが細胞間ポジティブフィードバック[3]として働き、その差を増幅します。実際に、2個の娘細胞のうち、片方が赤色の細胞(Delta陽性・Notch不活性)に、もう片方が緑色の細胞(Delta陰性・Notch活性)に変わった様子を観察できました(図1右)。
また、人工遺伝子ネットワークを導入した細胞が増殖すると、自発的に赤色の細胞と緑色の細胞が入り混じった細胞コロニーが形成されました(図2)。黄色の細胞(Delta陽性・Notch活性)や無色の細胞(Delta陰性・Notch不活性)はほとんど存在せず、はっきりした2種類の細胞集団に分かれていることが分かりました。これらの結果から、今回作製した人工遺伝子ネットワークが、均一な細胞集団から異なる2種類の細胞を自発的に生み出すのに十分であることが実証されました。
今回作製した細胞間に違いを生み出す仕組みは、多くの組織や生物種で普遍的に観察されます。また、Delta陽性細胞とNotch活性細胞の比率が異なることも知られていました。そこで、どういった条件が2種類の細胞の比率に影響するかについて調べました。
作製した人工遺伝子ネットワークは、2つのサブ回路(A回路とB回路)に分けて考えられます(図3)。A回路はtTSを介する転写抑制回路で、B回路はLfngを介してDelta-Notchシグナルの活性を制御する回路です。実験の結果、A回路のみを細胞に導入すると、赤色の細胞(Delta陽性細胞)の比率が高くなり、A回路とB回路の両方を導入すると、緑色の細胞(Notch活性細胞)の比率が高くなりました(図3)。これらの結果からA、Bのサブ回路の組み合わせを変えて人工遺伝子ネットワークを改変することにより、細胞種の比率をコントロールできることが分かりました。
今後の期待
今回、共同研究グループは、均一な細胞集団に自発的に違いを生み出すための最小遺伝子ネットワークを作製し、2種類の細胞の比率をコントロールすることに成功しました。生物の仕組みを人工的に再構成することで、均一な細胞集団から性質の異なる細胞を生み出すための条件の検証や、新たな発見が得られました。これらの成果は分化の仕組みをさらに詳細に解明していくうえで役立つと期待できます。
実際の生物の発生過程では、異なる種類の細胞が適切な比率で自発的に生まれるだけでなく、各細胞種の空間的な配置も決まっていきます。今後は、空間的パターンも含めた再構成が課題になります。
原論文情報
- Matsuda M, Koga M, Woltjen K, Nishida E and Ebisuya M, "Synthetic lateral inhibition governs cell-type bifurcation with robust ratios", Nature Communications, doi: 10.1038/ncomms7195
発表者
理化学研究所
生命システム研究センター 細胞動態計測コア 再構成生物学研究ユニット
ユニットリーダー 戎家 美紀 (えびすや みき)
基礎科学特別研究員 松田 充弘 (まつだ みつひろ)
お問い合わせ先
理化学研究所 生命システム研究センター
広報担当 川野 武弘 (かわの たけひろ)
Tel: 06-6155-0113 / Fax: 06-6155-0112
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.Delta-Notchシグナル
多細胞生物の発生過程で使われる最も重要なシグナル伝達経路の1つ。シグナルを送るリガンドであるDeltaとシグナルを受ける受容体のNotchの両方が膜タンパク質という特徴がある。隣接細胞間が接触しDeltaとNotchが結合した時に、Notchが活性化され下流のシグナル伝達が起こる。 - 2.転写抑制因子
遺伝子発現を負に制御する因子。転写抑制因子がプロモーター上に結合することで、転写が抑制される。 - 3.ポジティブフィードバック
ある方向の変化が起こった時に、回りまわってその変化を増幅、促進するような制御形態。例えば、遺伝子Aが遺伝子Bを誘導し、BもAを誘導する場合、AとBはポジティブフィードバックを形成している。このとき、Aが誘導されると、Bを介してAがさらに誘導される。
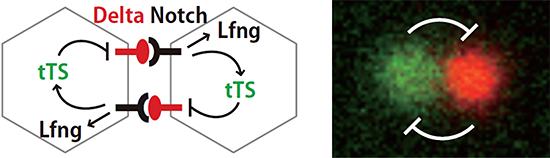
図1 人工遺伝子ネットワークの模式図(左)と隣接細胞間の非対称化(右)
Delta(リガンド)が隣の細胞のNotch(受容体)を活性化すると、tTS(人工的な転写抑制因子)とLfng(Delta-Notchシグナルの調節因子)の発現が誘導される。tTSはDelta遺伝子の転写を抑制するので、隣り合う細胞が互いにDelta遺伝子の発現を抑え合う形になっている。右の写真は、人工遺伝子ネットワークを導入したCHO細胞。2個の娘細胞間でDelta遺伝子の発現を互いに抑え合う仕組みが細胞間ポジティブフィードバックとして働き、片方が赤色の細胞(Delta陽性・Notch不活性)ともう片方が緑色の細胞(Delta陰性・Notch活性)に自発的に分かれた。
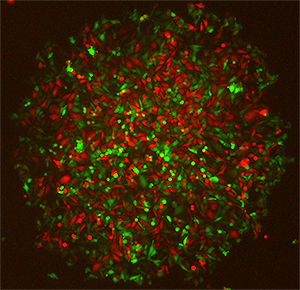
図2 人工遺伝子ネットワークを導入した細胞が増殖して形成された細胞コロニー
人工遺伝子ネットワークを導入したCHO細胞が増殖していくにつれ、赤色の細胞(Delta陽性・Notch不活性)と緑色の細胞(Delta陰性・Notch活性)が入り混じった細胞コロニーが形成された。
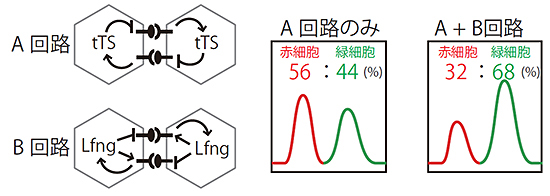
図3 人工遺伝子ネットワークのサブ回路の組み合わせ(左)と細胞種比率の関係(右)
図1の人工遺伝子ネットワークは、2つのサブ回路の組み合わせでできている。A回路は人工的な転写抑制因子tTSを介する転写抑制回路。B回路はLfngを介するが、本研究で詳しく調べた結果、LfngがNotchとDeltaの両方に対してフィードバック機構を持っていることが分かった。A回路のみを細胞に導入すると赤色の細胞(Delta陽性細胞)の比率が高くなり、A回路とB回路の両方を細胞に導入すると緑色の細胞(Notch活性細胞)の比率が高くなった。
