要旨
理化学研究所(理研)石井分子遺伝学研究室の吉田圭介特別研究員、石井俊輔上席研究員らの共同研究チーム*は、自然免疫[1]に記憶[2]が存在し、病原体感染によるエピゲノム変化[3]の持続がその記憶メカニズムであることを明らかにしました。
ヒトの免疫系には、先天的に備わった「自然免疫」と生後獲得していく「獲得免疫[1]」があります。自然免疫はマクロファージなどにより病原体に対して初期防御を行います。一方、獲得免疫はB細胞やT細胞などのリンパ球により一度侵入した抗原を認識し、排除します。これまで、病原体に感染したことを記憶するのは獲得免疫だけとされていましたが、いくつかの現象から自然免疫にも記憶が存在することが示唆されていました。しかし、その記憶メカニズムが不明なため、自然免疫の記憶の存在を疑問視する声もありました。
共同研究チームは、グラム陰性菌[4]の細胞壁外膜成分のリポ多糖(LPS)をマウスに投与すると、ストレス応答性転写因子ATF7を介して免疫系遺伝子のエピゲノム変化が誘導され、その状態が長期間持続すること、そして、これによりグラム陽性の黄色ブドウ球菌に対する抵抗性が上昇することを明らかにしました。したがって、自然免疫の記憶は特定の抗原の情報を特異的に認識する獲得免疫の記憶と異なり特異性がない、という特徴を持つことが分かりました。
今回の研究により自然免疫の記憶メカニズムが明らかになり、自然免疫にも記憶が存在することが示されました。自然免疫に記憶が存在するかどうかは、免疫学の根本的な重要課題であると共に、衛生仮説[5]やワクチンに必要なアジュバント[6]の性質にも関わっています。このため、今回の成果はアレルギー発症機構の解明や、効率的なワクチンの開発にも役立つことが期待できます。
本研究は、科学技術振興機構CREST(エピゲノム研究に基づく診断・治療へ向けた新技術の創出)、および文部科学省科学研究費新学術領域研究「ゲノムアダプテーションのシステム的理解」の助成を受け、米国の科学雑誌『Nature Immunology』に掲載されるのに先立ち、オンライン版(8月31日付け:日本時間9月1日)に掲載されます。
※共同研究チーム
理化学研究所
石井分子遺伝学研究室
上席研究員 石井 俊輔(いしい しゅんすけ)
特別研究員 吉田 圭介(よしだ けいすけ)
協力研究員 前川 利男(まえかわ としお)
研修生 ユジュアン・ズー(Yujuan Zhu)
統合生命医科学研究センター 統合細胞システム研究チーム
チームリーダー 岡田 眞里子(おかだ まりこ)
特別研究員 井上 健太郎(いのうえ けんたろう)
東京大学 分子細胞生物学研究所
教授 白鬚 克彦(しらひげ かつひこ)
特任研究員 クレア・ルナール・ギレ(Claire Renard-Guillet)
ストラスブール大
教授 ブルーノ・シャトン(Bruno Chatton)
東京工業大学大学院 生命理工学研究科
講師 山田 拓司(やまだ たくじ)
大学院生 内山 健(うちやま たける)
東京薬科大学 薬学部
教授 大野 尚仁(おおの なおひと)
助教 石橋 健一(いしばし けんいち)
背景
ヒトの免疫系には、先天的に備わった「自然免疫」と生後獲得していく「獲得免疫」があります(図1)。自然免疫は、マクロファージなどにより病原体に対して初期防御を行います。一方、獲得免疫は、B細胞やT細胞などのリンパ球により一度侵入した病原体を認識し、排除します。このようにヒトの体は、一度侵入した病原体が再度侵入した時、より早くその病原体を認識し排除するため、「免疫記憶」と呼ばれる病原体を記憶するメカ二ズムを持っています。これまで記憶は獲得免疫のみに存在するとされていましたが、自然免疫しか持たない植物や昆虫にも記憶が存在することや、脊椎動物でヘルペスウイルス感染がバクテリアに対する抵抗性を上昇させることなどから、自然免疫にも記憶が存在するのではないかと議論されていました。しかし、その記憶メカニズムが不明なため、自然免疫系の記憶の存在を疑問視する声もありました。
これまで、石井分子遺伝学研究室では、ストレスによる遺伝子発現変化を調べるために、マウスやショウジョウバエを用いて、ストレス応答性転写因子ATF7を含むATF2ファミリー転写因子について研究してきました。さまざまなストレスはDNA配列に変異を生じさせる可能性は低いことから、DNA配列の変化を伴わずに遺伝するメカニズム(エピジェネティックス)に着目し調べたところ、熱ショックストレスや精神ストレスなどの環境要因により、ATF2ファミリー転写因子を介してエピゲノム変化が誘導され、それにより基底発現レベルの高い状態が長期間持続することを報告していました注)。エピゲノムは、DNAやヒストン[7]が化学修飾された遺伝子配列情報で、環境要因により変化し、それが様々な疾患の発症に影響することが示唆されています。
注)2011年6月24日 プレスリリース「親の受けたストレスは、DNA配列の変化を伴わずに子供に遺伝」
研究手法と成果
共同研究チームは、これまでの研究で用いてきた転写因子ATF7の変異マウスのマクロファージが活性化されていることに気づき、マクロファージにおいて病原体感染によりエピゲノム変化が誘導されるのではないかと考えました。一連の解析の結果、マクロファージでは一群の免疫系遺伝子にATF7が結合し、ヒストンのメチル化酵素G9aを運び、ヒストンをメチル化することにより発現を抑制していることが分かりました(図2左)。そしてグラム陰性菌細胞壁外膜の構成成分であるリポ多糖(LPS)をマウスに投与し病原体に感染した状態を再現すると、Toll様受容体(TLR)からのシグナルによりリン酸化されたATF7がこれらの免疫系遺伝子から外れ、ヒストンのメチル化が低下し、転写が誘導されました(図2中)。LPSを投与して3週間後でもこれらの遺伝子のヒストンメチル化レベルは低い状態で維持され、基底発現レベルの高い状態が継続していました(図2右)。さらに、グラム陽性の黄色ブドウ球菌に対する抵抗性も継続して持っていることが分かりました。これは病原体の防御に非特異的に作用する自然免疫系遺伝子の発現レベルが高く維持されるためであり、記憶を獲得していると言えます。
今後の期待
今回の研究により、自然免疫に記憶が存在し、病原体感染によるエピゲノム変化の持続がそのメカニズムであることを明らかにしました(図3)。
乳幼児期までの感染や非衛生的環境が、その後のアレルギー疾患の発症を低下させるということが判明しています(衛生仮説)。しかし、バクテリア感染などの影響が長期間記憶されるメカニズムは不明でした。今回、特定の遺伝子のエピゲノム変化が長期間維持されることが分かったことから、これらの遺伝子をアレルギーの予測に使える可能性が示唆されました。また、効率的なワクチンには自然免疫を活性化するアジュバントが必要です。従来アジュバントの効果は数日で終了すると考えられていましたが、本研究により長期間記憶される事が分かりました。これはアジュバントの選択法にも影響し、より効率的なワクチンの開発に繋がることが期待されます。
原論文情報
- Yoshida K, Maekawa T, Zhu Y, Renard-Guillet C, Chatton B, Inoue K, Uchiyama T, Ishibashi K, Yamada T, Ohno N, Shirahige K, Okada-Hatakeyama M, and Ishii S., "The transcription factor ATF7 mediates lipopolysaccharide-induced epigenetic changes in macrophages involved in innate immunological memory", Nature Immunology, doi: 10.1038/ni.3257
発表者
理化学研究所
上席研究員研究室 石井分子遺伝学研究室
特別研究員 吉田 圭介(よしだ けいすけ)
上席研究員 石井 俊輔(いしい しゅんすけ)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.自然免疫と獲得免疫
免疫はマクロファージなどが関与する「自然免疫」と、T細胞やB細胞が関与する「獲得免疫」の連携によって成り立っている。2011年ノーベル医学生理学賞は、自然免疫のメカニズムが解明されたことに授与された。病原体が感染するとマクロファージ上のToll様受容体(TLR)が病原体細胞表面上の分子を認識し、シグナルが細胞内に伝わり、病原体を攻撃する物質(サイトカインなど)を産生する。これが自然免疫である。また、マクロファージはT細胞を活性化する物質を産生し、B細胞による抗体産生を促し、T細胞とB細胞による獲得免疫を活性化する。獲得免疫は抗原を認識する反応で特異性が高いが、自然免疫はTLRによる認識であり、特異性が低い。 - 2.免疫の記憶
私達の体は、一度感染した病原体が再感染した時には、より早くその病原体を殺す仕組みを持っている。これが免疫記憶で、ワクチンなどに応用されている。病原体が感染すると、それに特異的に反応するT細胞やB細胞が増えるが、病原体が無くなっても、記憶T細胞、記憶B細胞と呼ばれるごく一部の細胞が残る。これらは長い寿命を持ち、同じ病原体が再感染した時には、素早く増えて、病原体に対抗する。これが獲得免疫の記憶メカニズムである。一方これまで、自然免疫には記憶がないとされて来た。 - 3.エピゲノム
接頭辞「エピ(付加した、の意)」と「ゲノム」を繋いだ言葉で、DNAやDNAが巻き付くヒストンが化学修飾(メチル化など)された遺伝子配列情報。このような化学修飾情報のいくつかのものは、細胞分裂を超えて伝わる。またこのような情報は環境要因により変化し、それが様々な疾患の発症に影響することが示唆されている。 - 4.グラム陰性菌
細菌類はグラム染色と呼ばれる方法により、大きく2種類に大別される。これは細胞壁の構造の違いによるもので、染まるものをグラム陽性、染まらないものをグラム陰性という。 - 5.衛生仮説
疫学調査により乳幼児期までの感染,非衛生的環境が,その後のアレルギー疾患の発症を低下させるということが判明しており、衛生仮説と呼ばれている。 - 6.アジュバント
アジュバントは、ワクチンの効果を高める目的で、抗原とともに投与される物質。自然免疫を活性化するものが多い。 - 7.ヒストン
真核生物のクロマチンを構成する一群のタンパク質。ヒストンは5種類(H1, H2A, H2B, H3, H4)に分けられ、そのうち、H2A、H2B、H3、H4の4種はコアヒストンと呼ばれ、それぞれ2分子が集まり八量体(オクタマー)を形成する。オクタマーには、約146bpのDNAが左巻きに約1.65回巻き付く。この構造はヌクレオソームと呼ばれ、クロマチン構造の最小単位である。このように、ヒストンは非常に長い分子であるDNAを核内に収納する役割を担う。
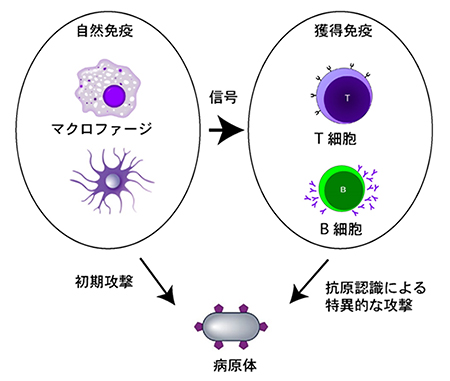
図1 自然免疫と獲得免疫
自然免疫は、マクロファージなどにより、病原体に対して初期防御を行う。一方、獲得免疫は、B細胞やT細胞などのリンパ球により、一度侵入した病原体を認識し、排除する。
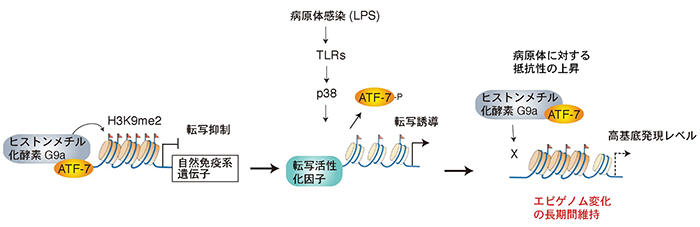
図2 ATF7を介した、病原体感染によるエピゲノム変化と自然免疫記憶
マクロファージでは一群の免疫系遺伝子にATF7が結合し、ヒストンのメチル化酵素G9aをリクルートし、ヒストンをメチル化することにより発現を抑制する。そしてグラム陰性菌細胞壁外膜の構成成分であるリポ多糖(LPS)をマウスに投与すると、Toll様受容体(TLR)からのシグナルによりATF7がリン酸化され、これらの免疫系遺伝子からはずれ、ヒストンのメチル化が低下し、転写が誘導される。LPSを投与して3週間後でもこれらの遺伝子のヒストンメチル化レベルは低い状態で維持され、基底発現レベルの高い状態が継続する。
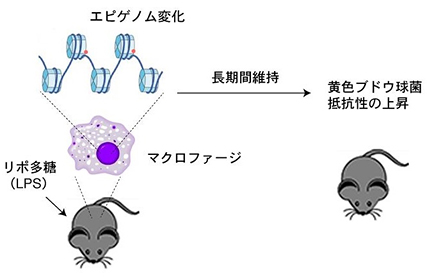
図3 本研究成果のまとめ
自然免疫に記憶が存在し、病原体感染によるエピゲノム変化の持続がそのメカニズムである。
