要旨
理化学研究所(理研)吉田化学遺伝学研究室の吉田稔主任研究員、伊藤昭博専任研究員らの共同研究グループ※は、酸化ストレス[1]応答転写因子[2]Nrf2の負の制御因子であるKeap1の新しい機能を発見し、がん細胞の運動を制御する新しい仕組みを発見しました。
アクチン[3]結合タンパク質であるコータクチンは、がん細胞の浸潤、転移[4]に関わる重要な因子で、多くの浸潤がんに高発現していることから、がん転移治療の標的分子として着目されています。コータクチンの活性は、アセチル化などの翻訳後修飾により制御されていることが知られていましたが、その詳細なメカニズムは明らかになっていませんでした。
共同研究グループは、コータクチンのアセチル化修飾酵素を調べている過程で、コータクチンが核と細胞質を行き来するシャトルタンパク質であることを見出しました。さらに、コータクチンの新しい結合パートナーとして酸化ストレス応答転写因子Nrf2の負の制御因子であるKeap1を発見しました。Keap1はコータクチンを細胞質にとどめおき、さらに外部シグナルに応答して細胞辺縁部へ運ぶことにより、細胞の運動を増進するという新しい機能を持つことが明らかになりました。このときコータクチンがアセチル化されているとKeap1との結合が弱くなるため、がん細胞の運動性が著しく低下することも分かりました。
これらの研究成果により、これまで酸化ストレス応答の制御因子であると考えられていたKeap1による新しいがん細胞運動性制御メカニズムを明らかにすることができました。この成果は、新しいがん転移治療法の開発につながると期待できます。
本研究は、米国の科学雑誌『Science Signaling』(11月24日号)にオンライン掲載されました。
※共同研究グループ
理化学研究所
吉田化学遺伝学研究室
主任研究員 吉田 稔 (よしだ みのる)(環境資源科学研究センター ケミカルゲノミクス研究グループ グループディレクター)
専任研究員 伊藤 昭博 (いとう あきひろ)
統合生命医科学研究センター 医科学数理研究グループ
グループディレクター 角田 達彦(つのだ たつひこ)
産業技術総合研究所 創薬分子プロファイリング研究センター
センター長 夏目 徹(なつめ とおる)
東北大学大学院医学系研究科 医化学分野
教授 山本 雅之(やまもと まさゆき)
背景
悪性腫瘍(がん)は無限に増殖するだけでなく、正常な組織との境界を越えて侵入したり(浸潤)、あるいは転移することにより、身体の各所で増大し、その結果宿主の生命を脅かします。従って、がん細胞の浸潤、転移の分子メカニズムを知ることは、新しいがん治療法の開発に有益です。
がん細胞の運動や浸潤に重要な働きをするアクチン結合タンパク質としてコータクチンが知られています。実際、コータクチンは多くの浸潤がんで高発現しており、がん転移治療の標的分子として注目されています。
コータクチンのがん細胞の運動を活性化する働きは、リジンアセチル化[5]などの翻訳後修飾により制御されています。これまでコータクチンの脱アセチル化酵素については比較的詳しく研究されていましたが、アセチル化酵素についてはよく分かっていませんでした。
研究手法と成果
共同研究グループは、コータクチンのリジンアセチル化を特異的に認識する抗体を作製し、コータクチンのアセチル化酵素を探索しました。その結果、ヒストン[6]アセチル化酵素であるCBPが主要なアセチル化酵素であることを発見しました。
コータクチンは細胞質に存在するタンパク質ですが、ヒストンアセチル化酵素であるCBPは主に核内に存在します。この一見矛盾した知見から共同研究グループは、コータクチンは細胞質と核を行き来しているのではないかと考えました。そこで核外移行の阻害剤であるレプトマイシンBを用いた実験を行ったところ、コータクチンが核から細胞質へ移行できず、核内に蓄積してしまうことが分かりました。つまり、コータクチンが核と細胞質を行き来するシャトルタンパク質であることが明らかになりました。
次に、コータクチンの細胞内局在を調節するタンパク質を同定する目的で、コータクチンの複合体解析を行ったところ、酸化ストレス応答転写因子Nrf2の負の制御因子として知られるKeap1を新しいコータクチンの結合タンパク質として発見しました。RNA干渉法によりKeap1をノックダウン[7]させたところ、コータクチンは核にも顕著に観察されるようになったことから、Keap1はコータクチンを細胞質にとどめおく機能があることが分かりました。
コータクチンは外部シグナル(増殖刺激[8])により細胞の辺縁部、特に細胞運動の際に形成される仮足[9]部分に移行します。そしてコータクチンはアクチン重合を促進することにより、がん細胞の運動を増進させます。そこで共同研究グループは、コータクチンによる細胞の運動増進におけるKeap1の役割についても検討しました。その結果、増殖刺激に応答してKeap1はコータクチンとともに細胞辺縁部に移行すること、Keap1がないとコータクチンは辺縁部に移行できないことが分かりました(図1)。さらにKeap1を欠損させるとがん細胞および正常線維芽細胞[10]の運動性が低下することが分かり、Keap1が細胞運動に重要な働きを持つことが明らかになりました。
コータクチン内の7カ所のリジン残基のアセチル化は、細胞の運動性を低下させることが知られています。そのメカニズムの一端として、コータクチンのアセチル化は、Keap1との結合を阻害することにより、細胞辺縁部への移行を阻害することを見出しました。つまり、コータクチンの脱アセチル化を止め、アセチル化を増やすとがん細胞の動きが止まることが分かりました。
これらの研究成果により、Keap1はこれまで知られていた酸化ストレス応答調節因子としての機能に加えて、コータクチンの細胞内局在を調節することにより細胞運動性を制御する因子として機能することが明らかになりました(図2)。Keap1はアクチンと結合することが知られていましたが、長らくその理由は不明でした。本研究成果はこの謎に1つの答えを与えるものです。
今後の期待
本研究成果により、Keap1・コータクチン・システムによる新しいがん細胞の運動制御メカニズムの存在が明らかになりました。本研究成果から、Keap1とコータクチンの相互作用の阻害は、がん細胞の浸潤や転移を抑えることを示します。また、コータクチンのアセチル化はKeap1との結合を弱めるため、コータクチン脱アセチル化酵素の阻害剤はがん転移の治療薬になる可能性があります。コータクチン脱アセチル化酵素を標的とした創薬開発が今後期待できます。
原論文情報
- Akihiro Ito, Tadahiro Shimazu, Satoko Maeda, Asad Ali Shah, Tatsuhiko Tsunoda, Shun-ichiro Iemura, Toru Natsume, Takafumi Suzuki, Hozumi Motohashi, Masayuki Yamamoto, Minoru Yoshida, "The subcellular localization and activity of cortactin is regulated by acetylation and interaction with Keap1", Science Signaling, doi: 10.1126/scisignal.aad0667
発表者
理化学研究所
主任研究員研究室 吉田化学遺伝学研究室
主任研究員 吉田 稔 (よしだ みのる)
専任研究員 伊藤 昭博 (いとう あきひろ)
 伊藤 昭博
伊藤 昭博
 吉田 稔
吉田 稔
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.酸化ストレス
生体内で、活性酸素(化学反応が起こりやすくなった酸素)などによる酸化作用が抗酸化作用を上回り、細胞などに有害な作用を及ぼすこと。ヒトの場合、酸化ストレスは狭心症、心筋梗塞、パーキンソン症候群、アルツハイマー病、統合失調症などさまざまな病気を引き起こす。 - 2.転写因子
ゲノムから遺伝子を発現させるときに機能するタンパク質。 - 3.アクチン
細胞骨格タンパク質の1つ。単量体のG-アクチンが重合して繊維状アクチン(F-アクチン)を形成する。F-アクチンから成るアクチンフィラメントは、細胞の形態や運動に深く関わる。 - 4.がん細胞の転移
がん細胞が発生した場所から他の臓器に移動して、そこで再び増殖して腫瘍を形成すること。 - 5.リジンアセチル化
リジン残基上で起こる可逆的な翻訳後修飾の1つ。アセチル-CoAを基質にし、ヒストンアセチル化転移酵素によりリジン残基のε-アミノ基がアセチル化される。 - 6.ヒストン
真核生物の染色体を構成する主要なタンパク質。 - 7.ノックダウン
特定の遺伝子の転写量を減少させることにより、遺伝子の機能を阻害する方法。 - 8.増殖刺激
成長因子など、外部シグナルにより細胞の増殖が引き起こされること。 - 9.仮足
真核細胞に見られる細胞質の一時的な突出のことで、仮足による運動をアメーバ運動と呼ぶ。 - 10.繊維芽細胞
結合組織を構成する細胞の1つで、皮膚の真皮の成分であるコラーゲン、ヒアルロン酸、エラスチンなどを作り出す。
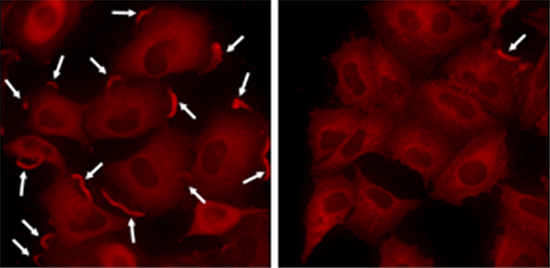
図1 Keap1ノックダウンによるコータクチンの細胞辺縁部への局在阻害
左はコントロール細胞。右はKeap1ノックダウン細胞。矢印は細胞辺縁部に局在するコータクチン。Keap1ノックダウン細胞では、細胞辺縁部に局在するコータクチンがほとんど存在しないことが分かる。
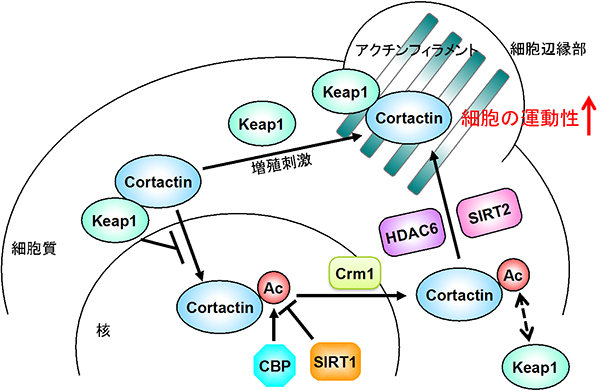
図2 Keap1とアセチル化によるコータクチンの活性制御機構の模式図
Keap1はコータクチン(Cortactin)を細胞質にとどめ、増殖刺激依存的にコータクチンを細胞辺縁部へ移行させることにより、がん細胞の運動性を増加させる。加えて、コータクチンのCBP(ヒストンアセチル化酵素)によるアセチル化は、Keap1との結合を阻害することにより、細胞の運動性を低下させる。
