要旨
理化学研究所(理研)ライフサイエンス技術基盤研究センター機能性ゲノム解析部門核酸技術診断開発ユニットの木村恭将客員研究員、相馬崇裕研究員、臼井健悟ユニットリーダーおよび同部門のマティアス・ハーバス客員研究員らの研究チームは、DNAの定量分析や病原体の遺伝子型決定、ヒト遺伝子多型(DNAの個体差)の検出に最適化したリアルタイムPCR[1]用のプローブとプライマーを設計するソフトウェア「Edesign(イーデザイン)」を開発・公開しました。
PCR法は、微量のDNAやRNAを酵素反応で増幅する方法です。リアルタイムPCR法では、この増幅産物をリアルタイムに検出することで、試料中の遺伝子発現量の定量や、遺伝子型の判別ができます。ただし、増幅に用いるプライマーと、増幅産物の検出に用いる蛍光プローブの配列が実験結果に大きな影響をもたらすため、これらの設計には細心の検討が必要でした。研究チームは2013年に、配列特異性(ある特定の配列にだけ反応する性質)が高く、かつ高感度な検出を可能にする蛍光プローブ「Eprobe(イープローブ)®」[2]を開発しました注1)。しかしEprobeには、最適な配列を見つけるための設計上の課題が残されました。
今回、研究チームは、Eprobeにおける蛍光色素標識塩基の挿入場所や、ミスマッチ塩基対[3]の位置、1本鎖のEprobeが形成する2次構造などの条件について、それぞれの要素がリアルタイムPCR法の実験結果に与える影響を詳しく調べました。その結果を踏まえて、最適なプライマー配列とプローブ配列を合わせて設計できるアルゴリズムの開発を行いました。これにEprobeの特性データを組み込むことで、新たな配列設計ソフトウェア、Edesignを開発しました。既存の設計ソフトと比較したところ、Edesignを用いればEprobe配列とプライマー配列のセットを高い精度でデザインできることが実験的に示されました。
今後、EprobeとEdesignの併用により、従来に比べて、より正確かつ高感度なDNA分析が可能になります。またEdesignは、Eprobe以外のプローブにも適用可能で、さまざまなタイプのプローブに対して幅広く利用されることが期待できます。なお、EdesignのWebインターフェイス(英語)はダナフォーム社から公開されています。
本研究は、米国のオンライン科学雑誌『PLOS ONE』(2月10日付;日本時間2月11日)に掲載されます。
注1)2013年8月8日プレスリリース「蛍光プローブ「Eprobe」のリアルタイムPCRへの応用」
背景
リアルタイムPCR法の登場により、生体から得た試料中にある微量のDNAやRNAを分析し、遺伝子発現の検出やDNA量の定量、遺伝子型の判別などが簡便に行えるようになりました。リアルタイムPCR法は、生物学実験ではもちろん、ヒトの遺伝子多型(DNAの個体差)の検出や感染症の診断に欠かせないツールとなっています。この技術の進展には、増幅産物を検出するための蛍光プローブの開発が大きく貢献しています。
研究チームは2013年に、蛍光色素として励起子相互作用を持つ人工核酸[4]をプローブ配列の途中に組み込むことで、蛍光のスイッチングを行なう新しい蛍光プローブ「Eprobe(イープローブ)」を開発しました(図1)。Eprobeを用いたリアルタイムPCR法は、検出対象となる鋳型核酸を特異的に定量検出でき、1塩基単位での遺伝子型判別を同時に行うことができます。これは、他の蛍光プローブにはない特徴です。
一方、リアルタイムPCR法には、最適なプローブ配列とプライマー配列の決定が難しいという課題があります。特にプローブの設計には、検出する標的配列との適合性だけではなく、プライマー配列との相補性や位置との兼ね合いも考慮することが必要です。しかし、複雑な複数の要素を考慮して、手法に応じた最適な配列を簡便に設計することのできるソフトウェアがありませんでした。
研究手法と成果
Eprobeを用いたPCR法を利用するためには、その増幅領域を決めるPCRプライマーの配列と、増幅産物を検出する蛍光色素の特性を考慮したEprobeの配列を最適化して設計する必要があります(図2)。
研究チームはまず、プローブとなる配列のモデルとして20塩基の長さのDNAを設計し、配列中の蛍光色素標識塩基の位置が異なるEprobeを10パターン合成しました。このEprobeが検出する標的DNAのモデルとして、Eprobeと完全に一致する相補的な20塩基のDNA配列を持つフルマッチ配列(1種類)と、1個ずつ元と違う塩基を持つ相補的なDNA配列(1カ所ミスマッチ塩基対、60種類)をデザインしました。これらの10パターンのEprobeと61種類の標的DNAの組み合わせ(610組)において、Eprobeと標的DNAとの融解曲線解析[5]を行い、それぞれにおける熱力学的パラメータを詳しく調べました。
その結果、蛍光色素標識塩基が末端にあると蛍光強度が下がることが分かりました。また、蛍光色素標識塩基と1カ所ミスマッチ塩基対が3塩基以上離れている場合に、ミスマッチ検出感度が著しく向上することなど、さまざまな特性を数値化することができました。そして、プローブと標的DNAの配列特異性や、プローブの2次構造予測、PCRプライマー配列との相補性や位置との兼ね合い、およびEprobeの特性など複数の要素を考慮した上で、プローブ配列を簡便に設計できる新しいソフトウェア「Edesign(イーデザイン)」を開発しました。このEdesignは、複数の遺伝子型を検出する目的に適したプローブを設計する機能も併せ持っています。
研究チームはEdesignを、オープンソースのプライマー設計ソフトウェアであるPrimer3[6]を基に開発しました。そこで、オリジナルのPrimer3に既知のEprobe融解温度計算のみを組み込んで設計したEprobeと、Edesignで設計したEprobeの比較を試みました。インフルエンザウイルスの遺伝子型の検出性能で比較した結果、Edesignで設計したEprobe・プライマーのセットは、遺伝子型の違いを正確かつ高感度に検出できました(図3)。このことから、Edesignは高い精度でプライマー配列とEprobe配列のセットを設計できることが実験的に示されました。
さらにEdesignの汎用性を高めるために、熱力学的パラメータがEprobeとは異なる修飾塩基を持つプローブにも適用するための拡張機能も追加しました。この機能により、さまざまなタイプのプローブに対してEdesignが利用できます。通常のDNAプローブから、Eprobeで複数の蛍光標識を同時に検出する場合の新規蛍光色素、Eprobeとは熱力学特性が異なるプローブまで、幅広く利用可能なプローブ・プライマー設計ソフトウェアとなっています。
※ダナフォーム社はEdesign Webインターフェイス(英語)を公開しました。
今後の期待
個別化医療の普及や感染症の病原体検出において、遺伝子検査に関連する市場は飛躍的に成長しています。遺伝子検査をさらに普及させるには、技術開発スピードの向上が必要になってきます。Edesignは、Eprobeを用いたリアルタイムPCR法のデザインを高精度かつ簡便にできます。そのため、ウイルスなどの病原体の定量に必要な少量のDNAやRNAの検出、がん治療における分子標的薬投薬前の遺伝子変異検査など、医療をはじめ産業・研究などにおいて、今後、幅広く利用されることが期待できます。
なお、EdesignのWebインターフェイス(英語)がダナフォーム社から公開されています。
原論文情報
- Yasumasa Kimura, Takahiro Soma, Naoko Kasahara, Diane Delobel, Takeshi Hanami, Yuki Tanaka, Michiel J. L. de Hoon, Yoshihide Hayashizaki, Kengo Usui, Matthias Harbers, "Edesign: Primer and enhanced internal probe design tool for quantitative PCR experiments and genotyping assays", PLOS ONE, doi: 10.1371/journal.pone.0146950
発表者
理化学研究所
ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 オミックス応用技術研究グループ 核酸診断技術開発ユニット
客員研究員 木村 恭将(きむら やすまさ)
研究員 相馬 崇裕(そうま たかひろ)
ユニットリーダー 臼井 健悟(うすい けんご)
ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門
客員研究員 マティアス・ハーバス(Matthias Harbers)
 木村恭将
木村恭将
 相馬崇裕
相馬崇裕
 臼井健悟
臼井健悟
 マティアス・ハーバス
マティアス・ハーバス
お問い合わせ先
理化学研究所 ライフサイエンス技術基盤研究センター
広報・サイエンスコミュニケーション担当 山岸 敦(やまぎし あつし)
Tel: 078-304-7138 / Fax: 078-304-7112
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.リアルタイムPCR
PCR法では最初に、増幅対象(テンプレート)のDNA、DNA合成酵素(DNAポリメラーゼ)、大量のプライマーと呼ばれるオリゴヌクレオチドを混合して、反応液を作る。反応液を加熱(94℃程度)すると、2本鎖DNAが変性して1本鎖DNAになる。次に急速冷却する(60℃程度)と、結合(アニーリング)したプライマーの3’端を起点としてDNAポリメラーゼが働き、1本鎖部分と相補的な2本鎖DNAが合成される。これで2倍量のDNAができたことになる。再び高温にしてDNA変性から繰り返す。このように、PCR法は、DNA鎖長の違いによる変性とアニーリングの違いを利用して、温度の上下を繰り返すだけでDNA合成を繰り返し、DNAを2倍、4倍、8倍、16倍…と増幅する(増やす)技術である。リアルタイムPCR法では蛍光プローブを共存させ、反応の進行を蛍光シグナルの増減によって、リアルタイムで確認することができる。 - 2.Eprobe(イープローブ)
リアルタイムPCR法の反応過程で特定の鋳型配列への結合と解離を繰り返し、その際に生じる蛍光の発光と消失を測定することで、増幅された鋳型DNAの定量や遺伝子の変異検出を行う新しいタイプの蛍光プローブ。他の人工核酸型の蛍光プローブと比べて、構造が簡単で合成が容易であり、従来のリアルタイムPCR法と同じ手法で遺伝子検査システムを構築できる利点がある。 - 3.ミスマッチ塩基対
DNAは、アデニン(A)-チミン(T)とグアニン(G)-シトシン(C)が、それぞれ水素結合で結ばれた2種類の塩基対から構成されている。これらの塩基対をワトソン-クリック塩基対と呼ぶ。これに対し、他の塩基の組み合わせとしてはA-A、A-G、A-C、T-T、T-G、T-C、G-G、C-Cの8種類がある。これらの塩基対は水素の位置がマッチせず水素結合していない(相補的でない)ことから、ミスマッチ塩基対と呼ばれる。 - 4.励起子相互作用を持つ人工核酸
標的核酸への結合の有無に応じて、可逆的な蛍光のオン・オフを行う人工核酸のこと。理化学研究所の岡本晃充博士(現:東京大学教授)が2008年に開発した注2、3)。いくつかの蛍光色素が集合して平行型会合体(H会合体)を形成すると消光を示す、励起子相互作用を利用している。これは、色素の双極子の配向に基づく励起軌道の分裂に起因する。H会合体の場合は、分裂した励起軌道のうち上位が許容遷移、下位が禁制遷移になる。色素は、上位軌道へのみ励起されるので、吸収スペクトルの短波長移動が観察される。その励起状態は、エネルギー的に安定な下位軌道へ速やかに遷移した後、そこから基底状態へ戻ろうとする。しかし、その過程は蛍光を伴わない放熱系であるので、蛍光発光は生じない。
注2)Ikeda, S., and Okamoto, A. (2008) Hybridization-sensitive on-off DNA probe: Application of the exciton coupling effect to effective fluorescence quenching. Chem.-Asian J. 3, 958−96
注3)Ikeda, S., Kubota, T., Kino, K., and Okamoto, A. (2008) Sequence dependence of fluorescence emission and quenching of doubly thiazole orange labeled DNA: Effective design of a hybridization-sensitive probe. Bioconjugate Chem. 19, 1719−1725.
- 5.融解曲線解析
リアルタイムPCR法で得られた増幅産物は、反応液中で2本鎖DNAの状態となっている。溶液の温度を徐々に上げていくと、ある温度以上で2本鎖DNAが分離し、急激に蛍光強度が低下する。温度上昇と蛍光強度の関係は、蛍光プローブがどの程度の強さで標的DNAに結合しているかを反映している。本研究では、プローブの配列デザインを評価するためにこの解析を用いた。 - 6.Primer3
PCR用プライマー設計ツール。PCRの用途に合わせた単純な条件を入力してプライマー配列を設計できるソフトウェア。PCRプライマーに対しては十分な計算が行われているが、プローブに対してはPCRプライマーと合わせたプローブ設計に必要な複雑な条件を考慮するものではなかった。詳細は、 Primer3のホームページ(英語)。
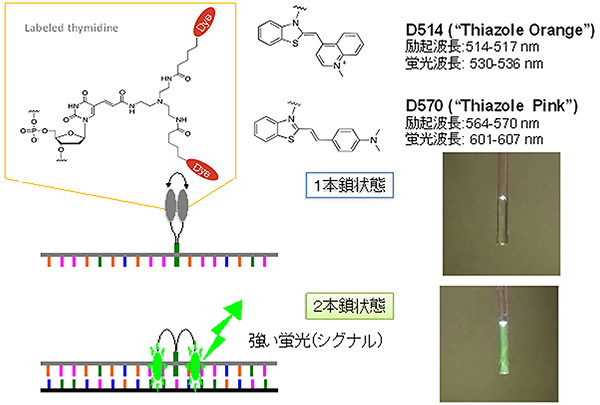
図1 Eprobeの発光の仕組み
図上:Eprobeは、DNAの部品であるチミン塩基に蛍光色素(Dye)を2つ(D514とD570)持つ構造をしている。これらの蛍光色素は、ターゲットとなるDNA配列と結合していない1本鎖の状態では、励起子相互作用が働いて蛍光発光が抑制されている。
図下:EprobeがターゲットのDNA配列と結合し2本鎖を形成すると、2つの色素が分かれてDNAの2本鎖構造に入り込み、色素間の励起子相互作用が解除され蛍光を発する。
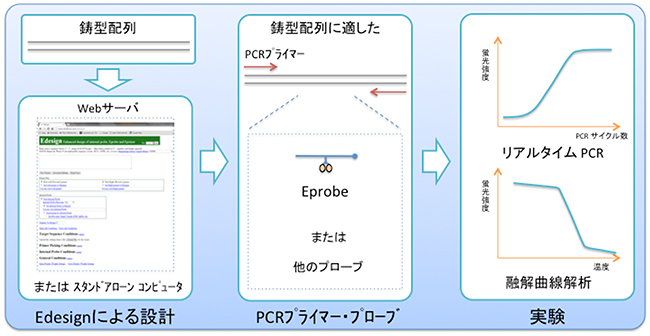
図2 Edesignによる設計からリアルタイムPCR実験まで
調べたいDNA(もしくはRNA)配列をEdesignに入力すると、最適なプライマー配列とプローブ配列の候補が表示される(左)。この情報をもとにプライマーとEprobe(または他のプローブ)を合成し(中央)、実際にリアルタイムPCR実験を行う(右)。
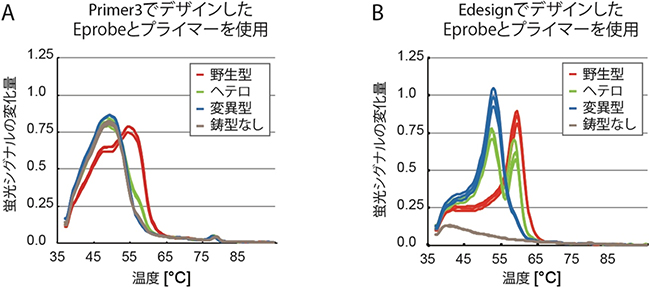
図3 Primer3およびEdesignで設計したEprobeによるミスマッチ配列の検出感度の比較
Primer3に既知のEprobe融解温度計算のみを組み込んで設計したEprobe(A)と、EdesignでデザインしたEprobe(B)を用い、インフルエンザウイルスの遺伝子型の検出性能を比較した。(B)では、野生型(赤)、変異型・野生型ヘテロ(緑)、変異型(青)の蛍光シグナルの変化量に温度による鋭いピークがみられ、それぞれのミスマッチ配列を正確に検出することができた。また、(A)では対照実験の「鋳型なし」でもシグナルの増加がみられたが、(B)では誤ったシグナルのピークは検出されなかった。
