要旨
理化学研究所(理研)環境資源科学研究センター先進機能触媒研究グループの侯召民(コウ・ショウミン)グループディレクター、張亮(チャン・リャン)研究員、西浦正芳専任研究員、侯有機金属化学研究室のビアトリース・キャリー国際プログラム・アソシエイトらの研究チームは、銅触媒を用いて、二酸化炭素(CO2)やホウ素化合物など入手容易な原料から、新奇な構造を持つ「リチウムホウ素化合物[1]」を簡便に合成する手法を開発しました。
CO2は入手が容易で再生可能な炭素資源であると同時に、温室効果ガスとして環境に悪影響を及ぼすことから、CO2削減につながる有効な利用法の開発が期待されています。例えば、CO2を利用した合成反応による有用物質の開発が考えられますが、CO2は化学的に安定であるため、効率的かつ実用的に変換する方法は限られています。一方で、リチウムホウ素化合物は、スマートフォンやノートパソコンなどで使われる「リチウムイオン電池[2]」の電解質として利用されています。しかし、実用化に耐えうる、高純度のリチウムホウ素化合物を得るには、複雑な多段階反応を用いる必要があります。また、従来法では合成できる構造や組成も限られています。そのため、入手が容易な原料から、多様な組成や構造を持つリチウムホウ素化合物を効率的に合成する手法の開発が求められていました。
研究チームはこれまで、CO2を利用する有機合成反応について研究を進めてきました。今回、銅触媒を用いることにより、CO2、ホウ素化合物、アルデヒド類、リチウムアルコキシド[3]といった複数の入手容易な原料から、1段階で多様なリチウムホウ素化合物を合成する新しい手法の開発に成功しました。この手法を用いることで、従来のリチウムイオン電池の電解質とそれを溶かす溶媒が一体化した、新奇なリチウムホウ素化合物を合成することができます。
本研究は今後、溶媒を必要としない、新しいリチウムイオン電池の電解質の開発へ展開することが期待できます。また、これまで合成困難であったリチウムホウ素化合物を合成できることから、CO2の新たな有効利用法の開発にもつながると考えます。
成果は、ドイツの科学雑誌『Angewandte Chemie International Edition』のオンライン版(4月9日)に掲載されました。
背景
二酸化炭素(CO2)は、温室効果ガスとして地球環境への悪影響が懸念されることから、排出量の削減が急がれています。一方で、化学合成の観点からは、入手容易で再生可能なC1炭素資源[4]として捉えることができるため、有用物質の合成にCO2を利用することが非常に重要です。しかし、CO2は化学的に安定であるため、効率的かつ実用的な化学変換を実現するには、新しい反応の開発が必要でした。
一方「リチウムホウ素化合物」は、スマートフォンやノートパソコンなどの充電池として需要が大きい「リチウムイオン電池」の電解質として利用されています。リチウムイオン電池の電解液は、電解質を有機溶媒に溶かして使用します。そのため、電池として利用するためには高純度のリチウムホウ素化合物が必要です。しかし、従来法では、複雑な多段階反応を行う必要があり、合成できる生成物の組成や構造も限られていました。
研究チームはこれまで、安価な銅触媒を用いてCO2を利用する有機合成反応について研究を進めてきました。そこで今回、CO2を含む入手容易な原料から多様なリチウムホウ素化合物を効率的に合成する新しい手法の開発に挑みました。
研究手法と成果
研究チームは以前、銅触媒存在下で、CO2、ホウ素化合物、リチウムアルコキシド、アルキン類[5]などを反応させて、アルキン類のカルボキシル化反応[6]の開発を進めていました注)。この研究過程で、今回、アルキン類をアルデヒド類に変えて、同様な反応を行ったところ、分子内に5員環構造[7]を持つ新奇なリチウムホウ素化合物が選択的に生成されることを発見しました(図1)。
さらに詳しく検討したところ、さまざまな官能基を持つアルデヒド類から、多様なリチウムホウ素化合物を効率的に合成できることが明らかになりました。従来のリチウムホウ素化合物は、環状カーボネートなどの有機溶媒と組み合わせて、リチウムイオン電池の電解質として利用されています(図2)。今回合成した新奇なリチウムホウ素化合物は、ホウ素原子が環状カーボネートに組み込まれているため、従来のリチウムホウ素化合物とそれを溶かす有機溶媒が“一体化した物質”と見なすことができます。そのため、有機溶媒を必要としない、新しいリチウムイオン電池の電解質の開発へ展開することが期待できます。
注)L. Zhang, J. Cheng, B. Carry and Z. Hou, "Catalytic Boracarboxylation of Alkynes with Diborane and Carbon Dioxide by an N-Heterocyclic Carbene Copper Catalyst ", J. Am. Chem. Soc., 2012, 134, 14314-14317.
今後の期待
研究チームは銅触媒を用いて、CO2など、入手が容易な原料から多様なリチウムホウ素化合物を1段階で合成できる、効率的な新手法の開発に成功しました。これまでの手法では合成が困難だった、さまざまなリチウムホウ素化合物を手に入れることができるようになり、新しいCO2の有効利用法の開発につながる可能性があります。例えば、有機溶媒を必要としない、新しいリチウムイオン電池の電解質の開発へ展開することが期待できます。
原論文情報
- Beatrice Carry, Liang Zhang, Masayoshi Nishiura, Zhaomin Hou, "Synthesis of Lithium Boracarbonate Ion Pairs by Copper-Catalyzed Multi-Component Coupling of Carbon Dioxide, Diboron, and Aldehydes", Angewandte Chemie International Edition, doi: 10.1002/anie.201602278
発表者
理化学研究所
環境資源科学研究センター 先進機能触媒研究グループ
グループディレクター 侯 召民(コウ・ショウミン)
研究員 張 亮(チャン・リャン)
専任研究員 西浦 正芳(にしうら まさよし)
主任研究員研究室 侯有機金属化学研究室
国際プログラム・アソシエイト ビアトリース・キャリー(Beatrice Carry)
 左から侯 召民、ビアトリース・キャリー、張 亮、西浦 正芳
左から侯 召民、ビアトリース・キャリー、張 亮、西浦 正芳
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.リチウムホウ素化合物
リチウムとホウ素原子を持つ化合物群。例えば、リチウムビス(オキサラ-ト)ボレート(LiBOB)はリチウムイオン電池の代表的な電解質として用いられている。 - 2.リチウムイオン電池
充電式の電池の1種。正極と負極の間をリチウムイオンが行き来することで、充電・放電を行う。正極にリチウム酸化物、負極に炭素化合物を用いる。電解液には有機溶媒にリチウム塩を溶解した非水溶液が使われるのが一般的である。ニッケルカドミウム電池やニッケル水素電池よりも、小型化・軽量化がしやすく、電力が大きい。スマートフォンやノートパソコン、デジタルカメラなどの電源として普及している。 - 3.リチウムアルコキシド
アルコキシドは、アルコール類の水酸基(-OH)のHを金属で置換した化合物の総称。その金属がリチウムのものが、リチウムアルコキシドである。 - 4.C1炭素資源
原料として利用できる炭素数が1の化合物群。一酸化炭素やメタンなどもC1炭素資源である。 - 5.アルキン類
分子内に炭素-炭素間の三重結合を1個持つ、鎖式炭化水素群。 - 6.カルボキシル化反応
有機化合物にカルボキシル基(-COOH)を導入する反応。 - 7.5員環構造
有機化合物の分子内で、五個の原子が環状に結合した構造。
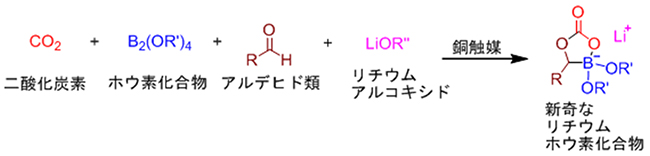
図1 銅触媒を用いた多成分カップリング反応によるリチウムホウ素化合物の合成
多様なリチウムホウ素化合物を、銅触媒存在下であればCO2を含む4種類の入手容易な原料から、1段階で簡便に合成できる。これは、多様なアルデヒド類に適用する新しい二酸化炭素固定化反応である。
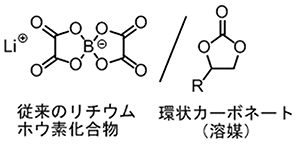
図2 従来のリチウムホウ素化合物と環状カーボネートとの組み合わせ
リチウムイオン電池の電解質として利用されている従来のリチウムホウ素化合物(左、リチウムビス(オキサラ-ト)ボレート)は、溶媒の環状カーボネート(右)と組み合わせることで高い性能を発揮する。図1の今回合成したリチウムホウ素化合物は、1分子内にリチウムホウ素と環状カーボネートの両方を併せ持ち、上記の2物質が“一体化された物質”と見なすことができる。
