要旨
理化学研究所(理研)小林脂質生物学研究室の森島信裕専任研究員(研究当時)と中西慶子協力研究員(研究当時)の研究チームは、血小板[1]の形成には、巨核球[2]細胞内の小胞体[3]が「小胞体ストレス[4]」状態となることが必要であることを発見しました。小胞体ストレスとは、立体構造がうまく形成されなかったり、構造が壊れたりしたタンパク質が小胞体内に蓄積した状態のことです。
血小板は、傷口の止血にとって欠かせない血液成分です。血小板は骨髄中に存在する前駆細胞の巨核球細胞がばらばらになり、核を含まない数千個の細胞質断片になることで作られます。細胞が変形したり、ばらばらになったりする現象は、細胞の自死現象の1つであるアポトーシス[5]にも共通することから、血小板が作られる際の巨核球細胞においても、アポトーシスと似た仕組みである「カスパーゼ族[6]」と呼ばれるタンパク質分解酵素が働くのではないかと考えられていました。2000年代初頭にはカスパーゼ3が血小板形成に関わっているという説が発表されましたが、その仕組みは不明でした。
カスパーゼ族は、生細胞中では余分な部分を含む前駆体として存在していて、不活性な状態にあります。カスパーゼ3が活性化するためには、イニシエーター[7]タイプと呼ばれるカスパーゼによって、カスパーゼ3前駆体が切断されなくてはなりません。一方、イニシエーターカスパーゼにはいくつか種類があり、細胞の状況に応じて異なる種類のカスパーゼが自己活性化[8]を起こします。
研究チームは、血小板形成の仕組みをイニシエーターカスパーゼ活性化の観点から調べようと考え、培養した巨核球細胞株から血小板ができる過程を調べました。その結果、カスパーゼ3の他にカスパーゼ4が活性化していることが分かりました。カスパーゼ4は小胞体ストレスによって自己活性化し、カスパーゼ3などを活性化させてアポトーシスを起こすことが知られています。研究チームは、血小板が作られるときにも小胞体ストレスが起きている実験的証拠を得ました。また、小胞体ストレスを解消する薬剤やカスパーゼ4の阻害剤があると血小板が形成されにくくなりました。一方、小胞体ストレスを増強する薬剤によって血小板形成効率を上げることに成功しました。これらの結果により、血小板形成のためには小胞体ストレスとカスパーゼ4の活性化が重要であることが分かりました。
本研究は、今後、培養細胞から血小板を大量生産するための技術開発に貢献すると期待できます。
成果は、日本分子生物学会と米国の出版社が発行する科学雑誌『Genes to Cells』(6月14日付け)に掲載されます。
背景
ヒトのようにさまざまな組織、臓器を持つ体ができるためには、幹細胞由来の未分化細胞の性質が変わり、特別な機能を果たすようになる細胞分化という過程が必要です。細胞機能が変化する原動力となるのは遺伝子発現パターンの変化で、これによって細胞内にあるタンパク質の量や種類が変わり、細胞が特別な機能を発揮できるようになります。
機能的な変化に加えて、細胞分化には細胞形態や核の大きな変化を伴うものがあります。血小板は血液中の細胞成分の一種ですが、細胞そのものではなく、前駆細胞である巨核球細胞が断片化し、核を失うとともに細胞質だけからなる小片へと分化することで形成されます。これとは逆に、骨格筋細胞は多数の核を持つ細胞で、前駆細胞である筋芽細胞が融合して形成されます。細胞の自死現象の1つであるアポトーシスも、生細胞がプログラムされた道筋を通って死細胞に変化する点で細胞分化に関連した現象であり、形態の大きな変化を伴います。このように細胞が自らの力で大きな形態変化をするとき、細胞内の構造にも大きな変化が生じます。
研究チームは、血小板形成とアポトーシスの間の類似性に着目しました。両者に共通して「カスパーゼ」と呼ばれるタンパク質分解酵素が働き、細胞形態変化を起こすのではないかと考え、どのようにしてカスパーゼが機能するようになるかを探ることにしました。
研究手法と成果
血小板が作られる過程において、巨核球細胞は大きな形態変化を起こして多数の突起を持つ細胞(胞体突起細胞)になり、さらに細胞質の断片化と脱核が起こります(図1)。巨核球細胞株を培養すると、培養フラスコ中でこの一連の過程が低頻度ながらも生じ、最終的に作られる細胞質断片は血液中の血小板と同じ凝集能を示すことが知られていました。そこで、研究チームはヒトの巨核球細胞株を用い、巨核球細胞、胞体突起細胞、血小板の中でカスパーゼ族のメンバーがどのような状態にあるか調べました。
巨核球細胞株が外径20~50マイクロメートル程度(μm、1μmは1,000分の1mm)の球形の比較的大きな細胞であるのに対し、胞体突起細胞は凹凸を持ち形は不定形です。また、血小板のサイズは2~3μmで、巨核球細胞に比べてはるかに小さいです。そこで、研究チームは細胞培養液中に混在するこれらの細胞や細胞断片を遠心分離し、巨核球細胞と分化が進んだ細胞とを分ける条件を見つけました(図2)。分離後、胞体突起細胞と血小板がほぼ同数形成されていることが分かりました。
次に巨核球細胞と分化の進んだ細胞とで、カスパーゼ族の活性化が起きているかどうかを詳しく調べました。カスパーゼ族は、カスパーゼ前駆体が切断されることによって活性化します。それぞれのメンバーについてウエスタンブロット解析[9]を行い、特異的な切断が起こっているかどうかを調べました。その結果、胞体突起細胞と血小板とを合わせた試料中で、カスパーゼ3とカスパーゼ4の活性化が検出されました。他のイニシエーターカスパーゼ(カスパーゼ5, 8, 9など)は前駆体のままでいるか、あるいは低レベルの活性化に留まっていました。
カスパーゼ4は小胞体ストレスに応答して起動し、カスパーゼ3を活性化させてアポトーシスを起こすことが知られています。小胞体ストレスは、立体構造がうまく形成されなかったり、構造が壊れたりしたタンパク質が小胞体内に蓄積した状態です。小胞体ストレスが起こると、細胞防御タンパク質が働きます。胞体突起細胞、血小板試料中では、ストレスセンサータンパク質が活性化して、タンパク質フォールディング(タンパク質の折りたたみ)を手助けするタンパク質が著しく増加していました。試料中の胞体突起細胞と血小板がほぼ同数で、それぞれのサイズは大きく異なることを考慮すると、解析した試料中にあるタンパク質はほとんど胞体突起細胞内にあったものと考えられます。そのため実験データは、胞体突起細胞の状態をよく反映している可能性が高いといえます。おそらく、胞体突起細胞が形成されるときか血小板になる前の段階で、小胞体ストレスの発生とカスパーゼ4の活性化が起きると考えられます。
それでは、小胞体ストレスやカスパーゼ4の活性化は、血小板形成にとってどれくらい大事なのでしょうか。小胞体ストレスは、タンパク質の立体構造形成の不具合によって生じますが、タンパク質立体構造形成を助ける低分子が既にいくつか開発されています。その1つである4-フェニル酪酸(4-PBA)を巨核球細胞の培養液に加えておくと、血小板形成は有意に阻害されました。また、カスパーゼ4のタンパク質分解活性を不可逆的に抑える低分子阻害剤を加えたときも、同様に血小板形成が阻害されました(図3左)。
一方、小胞体ストレスは、小胞体に備わっている特定のタンパク質の機能を抑えると人為的に生じさせることができます。代表的な例は小胞体にカルシウムイオン(Ca2+)を送り込むポンプタンパク質の機能阻害です。その阻害剤を添加すると、血小板形成が10倍程度まで上昇しました(図3右)。これらの結果は、巨核球細胞の分化にとって、小胞体ストレスとカスパーゼ4の活性化が重要であることを示しています。
今回の結果は、細胞がばらばらになり、しかも生きたままでいる分化過程の進行にとって、小胞体ストレスが役に立っていることを示しています。逆に細胞同士がくっついて融合する過程(骨格筋形成)においても、小胞体ストレスが重要な働きをしています(図4)注1)。これらは小胞体ストレスが善玉、悪玉の“二面性”を持っていることを示すとともに、小胞体という細胞小器官が細胞分化を制御する高い機能を進化の過程で獲得してきたことを示している可能性があります。
注1)2005年5月23日プレスリリース「筋肉組織の構築に細胞ストレスが必要なことを発見」
2007年4月16日プレスリリース「細胞内ストレスを利用して収縮する筋細胞を作る」
今後の期待
小胞体ストレスが1980年代後半に見つかって以来、この現象は細胞に対するダメージや負荷として捉えられることが多く、医学的な見地からは小胞体ストレスをいかに抑制するかに注目した研究も多くなされています。しかし、今回発見したように、小胞体ストレスは健康な個体内で起こっている細胞分化の調節に役立っている可能性があります。
研究チームは以前、骨格筋組織の形成において小胞体ストレスが筋前駆細胞を筋細胞に変える原動力の1つになっていることを示しました。また、筋前駆細胞において小胞体からカルシウムイオンが放出されることがこのストレスの原因であることを明らかにしました注2)。このように、個体の形成や健康にとって役に立つ小胞体ストレスの原因が明らかになってくると、その仕組みを利用して健康維持や病気の治療に役立てる道が開けてきます。同様に血小板形成において小胞体ストレスを生じさせる原因が究明されれば、生体内あるいは培養細胞系において血小板形成を人為的にコントロールする手法や薬剤の発展が促進されることが期待できます。
注2)2015年2月17日プレスリリース「筋肉を動かすカルシウムは筋肉を作る指令役も担う」
原論文情報
- N.Morishima and K. Nakanishi, "Proplatelet formation in megakaryocytes is associated with endoplasmic reticulum stress", Genes to Cells, doi: 10.1111/gtc.12384
発表者
理化学研究所
小林脂質生物学研究室
専任研究員(研究当時) 森島 信裕(もりしま のぶひろ)
(現:理研伊藤ナノ医工学研究室 専任研究員)
協力研究員(研究当時) 中西 慶子(なかにし けいこ)
(現:理研脳科学総合研究センター神経膜機能研究チーム 研究員)
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.血小板
血液成分の1つであり、血管が損傷して出血が起こったときに止血役として働く重要な細胞成分。凝固反応を起こして傷口を塞ぐ役割を果たしている。巨核球細胞から作られるときに核が失われるため、細胞質のみを含む細胞断片となっていて増殖することはできない。外科手術時や抗がん治療による血小板減少の対策として、血小板を体外から補充することが行われるが、現時点では血小板の供給は献血に頼っているため、保存可能期間が数日しかない点が問題となっている。 - 2.巨核球
骨髄中に存在している血小板の前駆細胞。造血幹細胞が分化して巨核球になり、さらに分化が進んで血小板となる。巨核球ができる過程では細胞分裂を伴わない特殊な染色体複製が複数回起こる(回数は一定していない)。そのため、個体内の他の多くの細胞がゲノムを2セットずつ持つ二倍体であるのと異なり、多倍体(ゲノムのセット数が4, 8, 16, 32, 64など多くなっている)である。細胞の大きさも均一ではない。 - 3.小胞体
細胞小器官の1つで、膜タンパク質、分泌タンパク質、脂質が合成される場。合成されたタンパク質は特異的な立体構造(三次構造、四次構造)を形成した後、脂質膜でできた袋に包まれて細胞膜や他の細胞小器官に運ばれる。 - 4.小胞体ストレス
小胞体内で作られたタンパク質の立体構造がうまく形成されなかったり(ミスフォールディング)、構造が壊れたりする(アンフォールディング)場合がある。このようなタンパク質が小胞体内に蓄積した状態を小胞体ストレスと呼ぶ。立体構造形成不全を起こしたタンパク質は凝集しやすく、また、立体構造形成を手助けするタンパク質群を動員するため、細胞にとって負担になるとされている。 - 5.アポトーシス
細胞が自己破壊を起こして自ら死ぬ現象。発生過程での組織作り、古くなった細胞の消失、がん化する可能性のある細胞の除去など、発生や健康の維持にとって重要である。異なる組織間や動物種間でも、アポトーシスの形態には共通性がある。共通性が生まれるのは[6]で説明するカスパーゼ族が共通して存在しており、同じような種類のタンパク質が同じように分解されるためだと考えられている。 - 6.カスパーゼ族
タンパク質中のペプチド結合を切断するタンパク質分解酵素の一種。ほ乳類では13種類が見つかっており、そのうち約3分の2がイニシエータータイプに分類されている。カスパーゼ3は数百種類以上のタンパク質を切断し、細胞の自己破壊において中心的な役割を果たす。 - 7.イニシエーター
生体内のシステム(シグナル系などの分子群や発がんなどの現象)を起動したり、きっかけとなるものを指し、その多くは分子である。 - 8.自己活性化
カスパーゼ族における自己活性化とは、イニシエーターカスパーゼ前駆体が持つ低いタンパク質分解活性によって同種(例えばカスパーゼ4同士)のカスパーゼ前駆体を切断し、活性化(分解能力の上昇)を起こすことを指す。細胞内の状況変化に応じて前駆体同士が集合し、分子間で切り合うことによって余分なアミノ酸配列が取り除かれると活性化が誘導される。 - 9.ウエスタンブロット解析
細胞試料など、多種類のタンパク質を含む試料の中にある特定のタンパク質の量や切断状態などを解析する手法。多くの場合、タンパク質をそれぞれのサイズに従って分布させた状態で、ニトロセルロースなどの膜に移してブロット(染み)を作る。特定タンパク質を認識する抗体がブロット上にどれくらい結合するかを量り、特定タンパク質の定量を行う。ウエスタンという呼び方はDNAのブロット解析法を開発したサザン博士の名前をもじったもの。
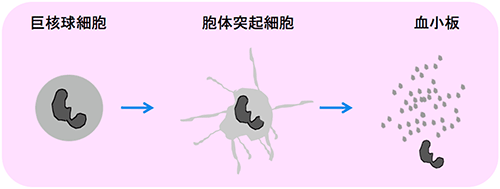
図1 血小板形成の過程
巨核球細胞は胞体突起細胞に分化し、その後細胞質の断片化と脱核が起こって多数の血小板が形成される。細胞質の断片化は、アポトーシスにおいても共通してみられる。

図2 血小板前駆細胞と分化過程にある細胞の分離
遠心分離によって前駆細胞(上図、巨核球細胞)と分化細胞(下図、胞体突起細胞、血小板および分裂途中の細胞断片)を分けることができる。100 倍の対物レンズを使用して撮った顕微鏡像。
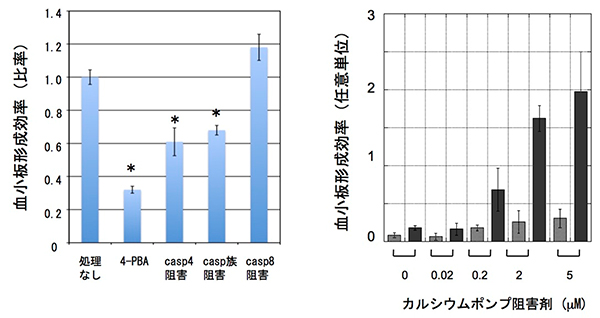
図3 血小板形成効率に与える影響
左:小胞体ストレスの解消(4-フェニル酪酸、4-PBA)や小胞体ストレスによって起動するカスパーゼ(casp)4の活性阻害によって、血小板形成効率は低下した。同様にカスパーゼ族全体を阻害すると、効率は低下したが、カスパーゼ8の阻害による低下はみられなかった。これらのデータは、血小板形成には小胞体ストレスとカスパーゼ4が必要だということを支持している。*は「処理なし」試料との差が統計学的にどの程度有意かを表す(P < 0.05)。
右:小胞体ストレスは、小胞体にあるカルシウムイオンを送り込むポンプタンパク質を阻害することによって、人為的に起こすことができる。このポンプタンパク質を一時的に阻害して、小胞体カルシウムイオン濃度を低下させた。すると、阻害剤の濃度に依存して血小板形成効率が上がった。灰色の棒は阻害後24時間経過時点、黒は48時間経過後の値を表す。5μMのカルシウムポンプ阻害剤では、阻害しない場合(0μM)に比べて、48時間後の効率を比較すると効率が10倍程度まで上昇していることが分かる。
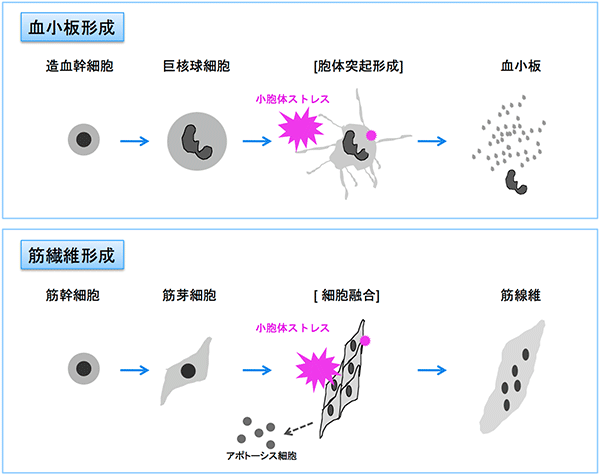
図4 細胞がばらばらになるときも、くっつくときも役立つ小胞体ストレス
(上図)血小板ができるために細胞がばらばらになる。(下図)筋肉細胞の前駆細胞が融合する直前に、小胞体ストレスが生じる。一部の細胞はストレスによってアポトーシスを起こす。
