要旨
理化学研究所(理研)グローバル研究クラスタ疾患糖鎖研究チームの木塚康彦研究員、谷口直之チームリーダーらの国際共同研究チーム※は、細胞が作る糖鎖[1]を高感度に検出する新たな手法を開発しました。
単糖が鎖状、もしくは分岐状につながってタンパク質などに結合したものを糖鎖と呼びます。糖鎖は体の中でさまざまな役割を果たしており、糖鎖の構造や量の変化が、がん、糖尿病、アルツハイマー病などの疾患の原因の一つとなることが分かっています。
国際共同研究チームは今回、フコース糖鎖(フコシル化糖鎖)[2]と呼ばれる糖鎖に注目しました。フコース糖鎖は免疫機能や肺の機能に重要な糖鎖で、フコース糖鎖の発現異常は、肺がん、肝がん、膵臓がんなどの多くのがんや、慢性閉塞性肺疾患[3]などの疾患でみられます。実際にフコース糖鎖の量の増加を指標にしたAFP-L3、CA19-9といったバイオマーカー[4]が、がんの診断に用いられています。ところが、フコース糖鎖を検出する現状の方法は、特異性(特定の糖鎖を見分ける性質)や感度が十分ではありません。糖鎖が関連する疾患をより正確に診断し、また疾患の原因をより詳しく探るには、フコース糖鎖の検出方法の改善が必要であると考えられます。
国際共同研究チームは今回、代謝ラベル法[5]という近年発展してきた糖鎖の検出法を利用し、フコース糖鎖を高感度に検出できる「7-アルキニルフコース」と呼ばれる新しい化合物を開発しました。この化合物は、フコース糖鎖の構成成分であるフコース[6]と類似した構造を持っており、細胞に添加するとフコースと同じようにフコース糖鎖の中に取り込まれ、容易に検出することができます。この方法を用いると、従来法よりも細胞毒性が生じにくく、高い感度で細胞のフコース糖鎖を特異的に検出し、顕微鏡下で観察することができます。
今後、この技術は、がんなどの疾患の新しいバイオマーカーの開発やがんのライブイメージング[7]などへの応用が期待できます。
本研究は、米国の科学雑誌『Cell Chemical Biology』オンライン版(7月21日付け:日本時間7月22日)に掲載されます。
※共同研究チーム
理化学研究所 グローバル研究クラスタ 理研-マックスプランク連携研究センター
システム糖鎖生物学研究グループ 疾患糖鎖研究チーム
研究員 木塚 康彦(きづか やすひこ)
チームリーダー 谷口 直之(たにぐち なおゆき)
大阪大学 産業科学研究所 疾患糖鎖(生化学工業)寄附研究部門
受託研究員 舩山 奨(ふなやま しょう)
受託研究員 庄籠 秀彦(しょうごもり ひでひこ)
台湾中央研究院 ゲノム研究センター
Distinguished Research Fellow チーフゥイ ウォン(Chi-Huey Wong)
背景
糖鎖の付加はタンパク質が受ける修飾の中で最も量が多く、哺乳動物に存在する半数以上のタンパク質には糖鎖が結合しています。このように糖鎖が結合したタンパク質は糖タンパク質と呼ばれています。糖鎖には構造の異なる多くの種類があり、私たちの体の中でさまざまな役割を果たしています。そして、がん、糖尿病、アルツハイマー病など多くの疾患で、糖鎖の構造や量の変化が原因の一つであることが分かっています。一方で、糖鎖の変化は、疾患を診断するためのバイオマーカーにもなります。特にがんでは、AFP-L3、CA19-9といった糖鎖の変化を指標とした診断マーカーが実際に臨床の場で使われています。中でも、フコースと呼ばれる糖を含むフコース糖鎖(フコシル化糖鎖)は、多くのがんでその量が増加し、がんの増殖や転移などに関わっていることが知られています。AFP-L3やCA19-9もフコース糖鎖の一種です。
診断マーカーとして糖鎖を利用するには、標的とする糖鎖を特異的・高感度・簡便に検出することが重要です。現在、糖鎖の簡便な検出には主に、①抗体、②レクチン[8]、③代謝ラベル法が用いられています。抗体は、特異性(特定の糖鎖を見分ける性質)が高い反面、多くの糖鎖に関して、それを認識する抗体の作製が技術上非常に困難です。植物や動物が持っている糖鎖認識タンパク質のレクチンは、種類は豊富ですが個々のレクチンの結合特異性が低く、しばしば非特異的なシグナルが問題になります。
代謝ラベル法は、検出したい糖に類似した構造を持つ糖類似体(糖アナログ[9])を用いる方法です。糖アナログを細胞に添加すると、細胞内の糖の代謝経路を利用して、糖鎖の中の糖の一部が糖アナログと置き換わります(図1)。検出のための目印を化学的に工夫して糖アナログに付けておけば、糖鎖中に含まれる糖アナログを容易に検出することができます。しかしこの方法は、特異性は高い一方、検出感度が低く細胞毒性を生じる場合があるなどの問題点があります。国際共同研究チームはこの代謝ラベル法に着目し、新しい糖アナログを開発することによって、より高感度に、低毒性で簡便にフコース糖鎖を検出できる方法の開発に取り組みました。
研究手法と成果
代謝ラベル法による糖鎖検出に用いられるフコースの既存の糖アナログとして、6-アルキニルフコースと6-アジドフコースが知られており、6-アルキニルフコースは糖鎖を検出する試薬として市販されています。最初に国際共同研究チームは、新しい糖アナログとしてアルキニル-(O)n-フコース(nは1~3)と7-アルキニルフコースを有機合成によって作製し、糖鎖検出の際の感度や細胞毒性について既存の糖アナログと比較しました。
まず、哺乳動物において最も主要なフコース糖鎖の合成酵素であるFUT8を用い、合成した糖アナログがこの酵素にどれだけ基質として利用されるかを調べました。その結果、既存の糖アナログは、天然のフコースに比べてFUT8の基質としてあまり利用されないのに対し、7-アルキニルフコースは、効率よくFUT8の基質として利用されることが分かりました(図2)。また同様の結果が、その他のフコース糖鎖合成酵素(Fut1, 2, 4, 9)を用いた実験でも得られました。このことから、7-アルキニルフコースは、既存の糖アナログに比べて効率よくフコース糖鎖中に取り込まれ、糖鎖の検出感度が上昇すると考えられます。
次に、実際に7-アルキニルフコースをヒト細胞に添加し、この糖アナログを取り込んだ糖タンパク質のフコース糖鎖を検出したところ、既存の6-アルキニルフコースに比べ、高感度に糖鎖を検出できることが分かりました(図3左)。また、6-アジドフコースは強い細胞毒性を示すことが知られていますが、7-アルキニルフコースはそのような毒性は示さないことが分かりました(図3右)。
さらに国際共同研究チームは、マウス細胞に添加した7-アルキニルフコースが糖鎖中のどの位置に取り込まれているかを確認するため、糖タンパク質が持つ糖鎖の構造を質量分析(LC-MS)[10]で決定しました。その結果、N型糖鎖の根元の「コアフコース」の位置に7-アルキニルフコースを取り込んだ糖鎖が検出されました(図4)。これは、7-アルキニルフコースが予想通りフコース糖鎖の一部に取り込まれ、主にコアフコースの位置に入ることを示しています。このことから、7-アルキニルフコースは細胞中のフコース糖鎖を検出する高感度のプローブとして有用であり、特にコアフコースを強く検出できることが分かりました。
今後の期待
本研究により、細胞の作り出すフコース糖鎖を高感度、低毒性かつ簡便に検出することが可能になりました。特にがんなど、細胞や血中のフコース糖鎖の量が増加することが知られている疾患の新しいバイオマーカーとなる糖鎖や糖タンパク質の同定に応用できます。将来的には、がんのライブイメージングなどへの応用も期待できます。なお、理研はすでにこの技術の特許を申請しました。
また、7-アルキニルフコースを用いれば、糖鎖を分析する専門的な機器や技術を必要とせずにフコース糖鎖が検出、可視化できるため、今後の基礎研究においてフコース糖鎖の機能や量、代謝経路、細胞内動態について調べることが容易になります。さらに、フコース糖鎖合成酵素の活性測定系への応用など、基礎研究においても幅広い用途での応用も期待できます。
原論文情報
- Yasuhiko Kizuka, Sho Funayama, Hidehiko Shogomori, Miyako Nakano, Kazuki Nakajima, Ritsuko Oka, Shinobu Kitazume, Yoshiki Yamaguchi, Masahiro Sano, Hiroaki Korekane, Tsui-Ling Hsu, Hsiu-Yu Lee, Chi-Huey Wong, Naoyuki Taniguchi, "High sensitivity and low toxicity fucose probe for glycan imaging and biomarker discovery", Cell Chemical Biology
発表者
理化学研究所
グローバル研究クラスタ 理研-マックスプランク連携研究センター システム糖鎖生物学研究グループ 疾患糖鎖研究チーム
チームリーダー 谷口 直之(たにぐち なおゆき)
研究員 木塚 康彦(きづか やすひこ)
 左:谷口 直之、右:木塚 康彦
左:谷口 直之、右:木塚 康彦
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.糖鎖
グルコース(ブドウ糖)などの糖が鎖状につながった物質。遊離の状態で存在するものもあれば、タンパク質や脂質に結合した状態のものもある。 - 2.フコース糖鎖(フコシル化糖鎖)
フコースと呼ばれる糖を構成成分の一つに持つ糖鎖。がんなどで血中や細胞中での量が増え、がんの増殖、転移に関わることが知られている。また炎症や慢性閉塞性肺疾患の発症にも深く関わっている。 - 3.慢性閉塞性肺疾患
肺気腫と慢性気管支炎の総称で、気道の閉塞による呼吸困難を引き起こす。WHOによれば、2030年までに世界の死亡原因の3位を占めるといわれている。 - 4.バイオマーカー
体液中などにおける存在量が疾患の有無や進行度の指標となるような生体物質。糖鎖も、がんなどのバイオマーカーとして用いられる。 - 5.代謝ラベル法
細胞内の糖の代謝経路を利用して、糖鎖をラベルし検出する方法。通常の糖と区別するために、ラベルに用いる糖には検出のための目印となるような化学修飾が施されている。ラベルされた糖鎖は、目印となる化学修飾を利用して検出される。 - 6.フコース
糖鎖を構成する糖の一種。ほ乳類では、10種類程度の糖から糖鎖は構成される。 - 7.ライブイメージング
生きた細胞のさまざまな活動を経時観察すること。本研究では今後、フコース糖鎖の発現が周囲の組織に比べて異常に増えているがん細胞を選択的に画像化する用途を想定している。 - 8.レクチン
糖もしくは糖鎖と結合する性質を持つタンパク質。植物や動物の体内に存在している。 - 9.糖アナログ
糖と構造が非常に類似した化合物。糖アナログのうち、検出のための目印となるような化学修飾を施したものが代謝ラベル法による糖鎖の検出に用いられる。7-アルキニルフコースも糖アナログの一つ。 - 10.質量分析(LC-MS)
分子をイオン化し、質量によって分離することで分子の質量を知る分析法。目的とする分子をさらに断片化させた質量も得ることができ、これらの情報から、含まれる分子の構造や種類の同定にも用いられる。液体クロマトグラム(LC)と接続することにより、より詳細な分子の情報が得られる。LC-MSは糖鎖の正確な構造決定に用いられる方法の一つ。
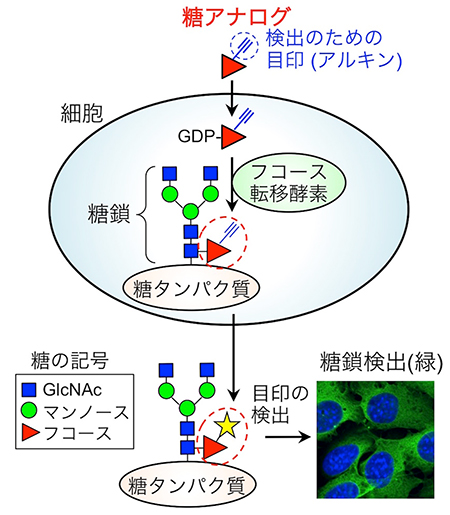
図1 代謝ラベル法による糖鎖の検出
検出のための目印(この場合はアルキン)を持った糖アナログを細胞に添加すると、細胞の中で活性化され、糖を合成する酵素(フコース転移酵素など)によって糖鎖の中に取り込まれる。糖アナログを取り込んだ糖鎖は、目印によって簡便に検出することができる。写真は細胞のフコース糖鎖を検出したもので、緑色の部分が糖鎖で、青色の丸い部分が細胞核である。
なお、アルキンとは分子内に炭素-炭素三重結合を持つ炭化水素のことである。GlcNAcはN-アセチルグルコサミンのことで、マンノースと同じく単糖である。GDPはグアノシンニリン酸で、ヌクレオチドの一種である。
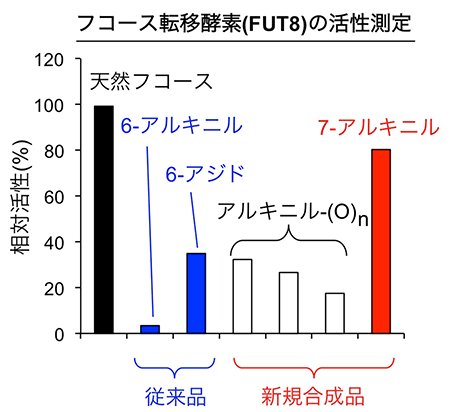
図2 フコース糖鎖合成酵素(FUT8)の活性測定
哺乳動物において主要なフコース糖鎖合成酵素であるFUT8の活性を、天然フコース、既存のフコースアナログ(6-アルキニルフコース、6-アジドフコース)、新たに合成したフコースアナログ(アルキニル-(O)n-フコース、7-アルキニルフコース)を用いて測定した。天然フコースに比べ、6-アルキニルフコース、6-アジドフコース、アルキニル-(O)n-フコースはFUT8に基質としてあまり利用されないのに対し、7-アルキニルフコースは効率よく基質として利用された。実験には、フコースもしくはフコースアナログのGDP体(グアノシンニリン酸体)を用いた。
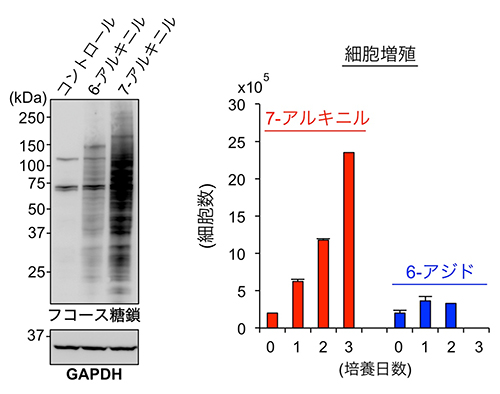
図3 7-アルキニルフコースを用いたフコース糖鎖の検出感度と細胞毒性
左:HEK293細胞(ヒト胎児腎細胞)に、6-アルキニルフコースもしくは7-アルキニルフコースを添加し、48時間後に細胞のタンパク質を溶解し、糖アナログを取り込んだフコース糖鎖を電気泳動法で検出した。縦軸はタンパク質の分子量を表す。GAPDHはサンプル間で同量のタンパク質を使用したことを示すための図。7-アルキニルフコースは、広い範囲の分子量のタンパク質で検出されていることが分かる。
右:Jurkat細胞(ヒトT細胞性白血病由来細胞)に、7-アルキニルフコースもしくは6-アジドフコースを添加し、24時間ごとに細胞数を計測した結果。7-アルキニルフコースは6-アジドフコースに比べて、増殖した細胞数がかなり多く、細胞毒性が低いことを示している。
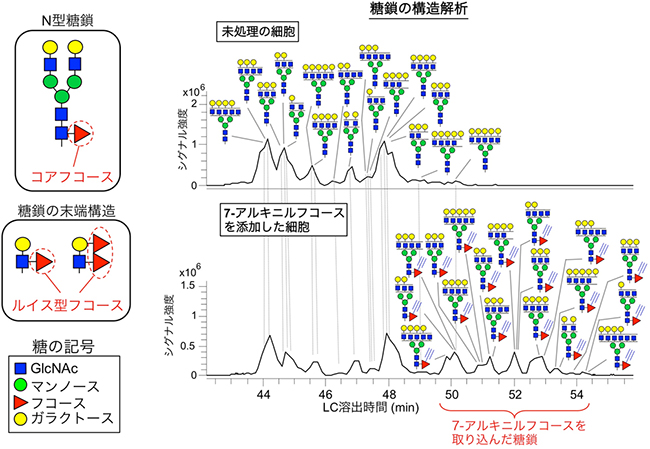
図4 糖鎖中の主なフコースの位置と7-アルキニルフコースが主に取り込まれる位置
左:哺乳動物における糖鎖中の主なフコースの位置。N型糖鎖の根元に結合したフコースをコアフコースと呼ぶ。その他、さまざまな糖鎖の末端のガラクトースやGlcNAc(N-アセチルグルコサミン)に結合したフコースをルイス型フコースと呼ぶ。
右:Neuro2A細胞(マウス神経芽腫細胞)に7-アルキニルフコースを添加し、糖タンパク質から糖鎖を切り出して質量分析(LC-MS)で構造を決定した。7-アルキニルフコースがコアフコースの位置に取り込まれた糖鎖構造が多く検出された。
