要旨
理化学研究所(理研)環境資源科学研究センター生体機能触媒研究チームの中村龍平チームリーダー、林徹研修生とソウル大学校工科大学のナム・キテ准教授、ジン・キョンソク博士研究員らの国際共同研究グループは、非貴金属系の水分解触媒において高い活性を示す人工マンガン触媒[1]が、「中性の水から電子を引き抜き分解する経路」の可視化に成功しました。
水は自然界に最も豊富に存在する電子源[2]であり、水素ガス製造や二酸化炭素の液体燃料(アルコールなど)への変換を担う重要な資源です。自然界で水資源の利活用を最も効率的に行っているのは植物などの光合成生物です。植物は四つのマンガン原子(Mn)を含む酵素(生体マンガン4核酵素)を用いて、水から電子と水素イオン(プロトン)を引き抜いて利用することで、二酸化炭素からデンプンを作り出しています。
しかし、人工的に合成したマンガン水分解触媒(人工マンガン触媒)の多くは、水素イオン濃度(pH)の中性領域において活性が著しく低いという問題がありました。また、これまでの水分解触媒開発は、明確な設計指針がないまま試行錯誤的に行われてきました。
そこで、国際共同研究グループは、水分解の反応経路の特定が重要と考え、人工マンガン触媒によって進む水分解反応機構の可視化を試みました。マンガン原子中の電子数とスピン[3]の状態、およびマンガン-酸素間の化学結合の変化を分子分光法[4]で包括的に解析したところ、ナノ粒子表面における化学種の変化や、人工マンガン触媒が中性の水から電子を引き抜き分解する経路の可視化に成功しました。その結果、酸化マンガンの直径を10nm程度(1nmは10億分の1メートル)まで粒子化すると、表面の3価のマンガン(Mn3+)が特異的に安定化し、中性環境での水分解活性が大きく向上することが分かりました。
本成果は、ナノ粒子化による「Mn3+の安定化」が、水分解触媒の高活性化に向けた設計指針になることを示しています。また、生体マンガン4核酵素においてもMn3+が安定に存在していることから、生体酵素を模倣した水分解触媒の合理的デザインにもつながると期待できます。
本研究は、米国の科学雑誌『Journal of the American Chemical Society』に掲載されるのに先立ち、オンライン版(1月17日付け:日本時間1月18日)に掲載されました。
背景
近年注目を集めている水素ガス製造や二酸化炭素の液体燃料(アルコールなど)への変換には電子源が必要です。海水や雨水などの水素イオン濃度(pH)が中性の水は、自然界に豊富に存在するため、水素ガスなどを製造するための電子源として期待されています。
自然界で電子源としての水の利活用を最も効率的に行っているのは植物などの光合成生物です。植物は四つのマンガン原子(Mn)を含む酵素(生体マンガン4核酵素)を用いて、水分子から電子(e-)と水素イオン(H+、プロトン)を引き抜いて利用することで、二酸化炭素からデンプンなどの栄養分を作り出しています。水分解反応は、「2H2O→4H++O2+4e-」で表されます。水を分解する生体マンガン4核酵素の構造は、原核生物のシアノバクテリアから藻類、種子、シダ植物とほぼ全ての光合成生物において共通すると考えられています。そのため植物の仕組みに学んでマンガン材料を用いて水分解触媒を設計し、高効率な水分解触媒を開発することは、太陽光と二酸化炭素から燃料を作り出す人工光合成デバイスの創出にもつながる重要な課題です。
しかし、人工的に合成したマンガン水分解触媒(人工マンガン触媒)の多くは、pHの中性領域において活性が著しく低下するという問題があります。また、これまでの水分解触媒開発は、反応効率を高めるための明確な材料設計の指針がないまま試行錯誤的に行われてきました。そこで国際共同研究グループは、試行錯誤的な開発から脱却するには、水分解の反応経路を特定することが鍵になると考え、人工マンガン触媒によって進行する水分解反応の可視化を試みました。
研究手法と成果
本研究では、直径が従来の人工マンガン触媒より小さな10nm程度のナノ粒子酸化マンガンを用いました。直径10nm程度のナノ粒子酸化マンガンは、非貴金属系の触媒において世界最高レベルの活性で中性の水を分解できることが、ソウル大学校ナム准教授らによって報告されています注1)(図1)。しかし、マンガン触媒をナノ粒子化することで触媒活性が飛躍的に向上する理由は分かっていませんでした。
まず、ナノ粒子酸化マンガンを導電性基板に塗布し、水電解の電極としました。次に、水電解のために電圧をかけた状態で、ナノ粒子酸化マンガン表面における化学種(マンガン原子中の電子数とスピンの状態、マンガン-酸素間の結合)がどのように変化するかを分子分光法(電子スピン共鳴[5]、紫外・可視光吸収、X線吸収、ラマン散乱)を用いて測定しました(図2)。
電子スピン共鳴でマンガン原子中の電子数とスピンの状態を調べたところ、水電解開始より低いエネルギーをかけた状態でも3価のマンガン(Mn3+)が多く生じることが分かりました。同様の結果は、ナノ粒子が吸収するX線のエネルギーの変化や、紫外・可視光に対する吸収の変化からも確認できました。また、光散乱の一種であるラマン散乱の測定からは、Mn3+の生成に伴うマンガン-酸素間結合の変化を確認できました。
続いて、比較として直径100nm以上の大きな酸化マンガンを用いて同様の測定を行いました。しかし、Mn3+の安定な存在は確認できませんでした。中村龍平チームリーダーらは過去に、酸化マンガン上でのMn3+の生成には高いエネルギーが必要で、このことが酸化マンガンの水分解活性の低さの原因となっていることを見いだしています注2)。つまり、「酸化マンガン触媒を直径10nm程度まで粒子化するとMn3+が安定化し、その結果、水分解活性が飛躍的に向上すること」が明らかになりました。
さらに、電子と水素イオン(プロトン)が移動するタイミングを、電流のpH依存性や、電圧変化に応答した電流増加の速さを測定することにより検討しました。その結果、マンガン原子から一つずつの電子が奪われて2価(Mn2+)から3価(Mn3+)、3価から4価(Mn4+)へと変化するそれぞれの段階で、プロトンも同時に一つずつ移動することが分かりました。これによって、ナノ粒子酸化マンガン表面で進行する水分解反応経路、つまり人工マンガン触媒が中性の水から電子を水から電子を引き抜き分解する経路を図3のように可視化できました。
注1)K. Jin, A. Chu, J. Park, D. Jeong, S. E. Jerng, U. Sim, H.-Y. Jeong, C. W. Lee, Y-S. Park, K. D. Yang, G. K. Pradhan, D. Kim, N.-E. Sung, S. H. Kim, K. T. Nam, “Partially Oxidized Sub-10nm MnO Nanocrystals with High Activity for Water Oxidation Catalysis”, Scientific Reports, 2015, 5, 10279.
注2)2014年6月30日「中性の水から電子を取り出す「人工マンガン触媒」を開発」
今後の期待
本成果は、酸化マンガン触媒を直径10nm程度まで粒子化するとMn3+が安定化し、その結果、水分解活性が飛躍的に向上することを示しています。すなわち、試行錯誤的だった触媒開発に対して、「Mn3+の安定化が鍵」という明確な設計指針を提供するものです。
また、生体マンガン4核酵素においてもMn3+が安定に存在していることから、人工光合成システムの構築に向けて鍵となる生体酵素を模倣した水分解触媒の合理的デザインにもつながると期待できます。
原論文情報
- Kyoungsuk Jin,† Hongmin Seo,† Toru Hayashi,† Mani Balamurugan, Donghyuk Jeong, Yoo Kyung Go, Jung Sug Hong, Kang Hee Cho, Hirotaka Kakizaki, Nadège Bonnet-Mercier, Min Gyu Kim, Sun Hee Kim, Ryuhei Nakamura,* Ki Tae Nam*, "Mechanistic Investigation of Water Oxidation Catalyzed by Uniform, Assembled MnO Nanoparticles", Journal of the American Chemical Society, doi: 10.1021/jacs.6b10657
†These authors contributed equally.
発表者
理化学研究所
環境資源科学研究センター 生体機能触媒研究チーム
チームリーダー 中村 龍平(なかむら りゅうへい)
研修生 林 徹(はやし とおる)
ソウル大学校 工科大学
准教授 Ki Tae Nam(ナム・キテ)
博士研究員 Kyoungsuk Jin(ジン・キョンソク)
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
産業利用に関するお問い合わせ
理化学研究所 産業連携本部 連携推進部お問い合わせフォーム
補足説明
- 1.人工マンガン触媒
光合成生物が行う、水から電子を引き抜き酸素とプロトンを作り出す水分解反応を人工的に行うための触媒。光合成生物が四つのマンガン原子(Mn)を含む酵素(生体マンガン4核酵素)を用いていることから、マンガンを含む金属酸化物や金属錯体が触媒として検討されている。 - 2.電子源
化学物質に電子を与える反応(還元反応)を行うために、電子を引き抜く(酸化する)ことができる化学物質。 - 3.スピン
粒子の持つ量子力学的な内部自由度(粒子を区別する性質)の一つで、しばしば粒子の自転として解釈される。マンガン原子中における電子のスピンの状態は、マンガンが何価であるかによって異なる。そのため本研究では、電子のスピンの状態を測定することで、2価(Mn2+)と3価(Mn3+)のマンガンの増減を測定できた。 - 4.分光法
測定した観測量と、測定に用いたエネルギーや周波数などとの相関を解析することで、測定対象物の構造や性質を調べる方法。本研究では、電子スピン共鳴、紫外・可視光吸収、X線吸収、ラマン散乱の4種類の分光法を利用した。 - 5.電子スピン共鳴
磁場中に置かれた物質は、ある条件(共鳴条件)を満たすマイクロ波(電磁波の一種)を強く吸収する。この現象を用いて、物質中の電子の状態を測定する手法。

図1 ナノ粒子酸化マンガンの電子顕微鏡像
酸化マンガン(II) (MnO)に酸化マンガン(II, III) (Mn3O4)が一部混ざった構造をした、ナノ粒子酸化マンガンの電子顕微鏡像。スケールバーはどちらも100nm。左画像をさらに拡大した右画像から、酸化マンガンの粒径が10nm程度にそろっていることが分かる。
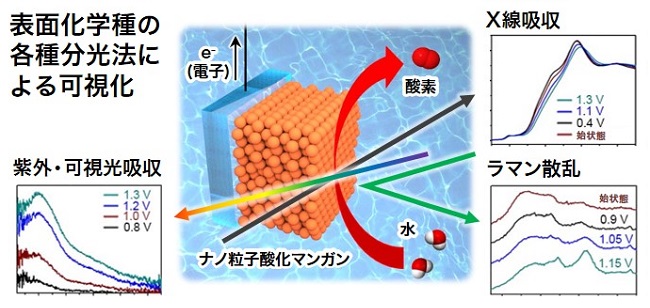
図2 ナノ粒子酸化マンガン表面における化学種の変化や反応経路の測定
ナノ粒子酸化マンガンを導電性基板に塗布し、水電解の電極とした。次に、分子分光法(紫外・可視光吸収、X線吸収、ラマン散乱)を包括的に用いることで、かけた電圧に応じたナノ粒子酸化マンガン表面における化学種の変化(マンガン原子中の電子数とスピンの状態、マンガン-酸素間の化学結合)を測定した。図に示したもののほかに、電子スピン共鳴も測定した。
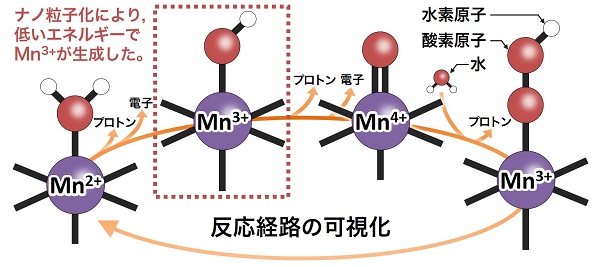
図3 ナノ粒子酸化マンガンにおける表面化学種の反応経路の可視化
電気化学測定と分光法により、ナノ粒子酸化マンガン表面における分子レベルでの情報を可視化した。Mn2+-H2O→Mn3+-OH→Mn4+=Oというように触媒表面の化学種が変化した後に、水から電子が引き抜かれる。ナノ粒子化により、Mn3+が特異的に安定化するとともに、プロトン移動を伴う電子移動(プロトン共役電子移動)が誘起されることが分かった。
