要旨
理化学研究所(理研)脳科学総合研究センターの内匠透シニアチームリーダー、日本医科大学大学院医学研究科の鈴木秀典教授らの共同研究グループ※は、モデルマウスを使った実験で、発達期のセロトニン[1]が自閉症発症メカニズムに関与する可能性を明らかにしました。
自閉症(自閉スペクトラム症)は、社会的コミュニケーション能力の欠如や繰り返し行動が特徴的な発達障害の一つです。症状は対処療法によって和らぐ場合もありますが、生涯にわたり表出します。家族は自閉症患者の保護や介護に多くの時間と労力を費やすため、社会的・経済的困難を抱えます。そのため自閉症の症状を緩和させる療法の発見に向けた原因解明が社会的に強く求められていますが、自閉症の発症メカニズムはほとんど分かっていません。自閉症患者の中にはゲノム異常を持つ人が見つかっており、なかでも15番染色体において重複異常が頻出することが知られています。また過去の研究で、自閉症患者の脳内において神経伝達物質のセロトニンが減少していることが示されていました注1)。しかし、ゲノム異常やセロトニン異常がどのように自閉症につながるのかは分かっていませんでした。
今回、共同研究グループはヒトの15番染色体重複と同じゲノム異常を持つモデルマウス(15番染色体重複モデルマウス)を解析したところ、脳内セロトニンの減少に関連して、セロトニンの供給元である中脳の縫線核の働きが低下していることや、セロトニン神経の投射先である大脳皮質(体性感覚皮質バレル野)での感覚刺激の応答異常を発見しました。また、発達期に重点をおいた薬理学的なアプローチでモデルマウスの脳内セロトニン量を回復させることにより、縫線核と大脳皮質の電気生理学的異常を改善させることに成功しました。さらに、15番染色体重複モデルマウスの成長後にセロトニン量を回復させることで、社会性行動異常も改善することが分かりました。
本成果は、発達期におけるセロトニンの重要性を示しているだけでなく、バイオマーカーとしての脳内セロトニンの役割や自閉症治療に関わる新たな知見をもたらすものと期待できます。
本研究は、米国のオンライン科学雑誌『Science Advances』の(6月21日付け:日本時間6月22日)に掲載されます。
本研究は日本学術振興会科学研究費補助金基盤研究(S)「自閉症の生物学的統合研究」と科学技術振興機構(JST)戦略的総合研究推進事業(CREST)「精神の表出系としての行動異常の統合的研究」(研究代表:内匠透)の支援を受けて行われました。
注1)Chandana et.al. J. Dev. Neurosci (2005)
※共同研究グループ
理化学研究所
脳科学総合研究センター
精神生物学研究チーム
シニアチームリーダー 内匠 透(たくみ とおる)(研究当時:広島大学 大学院医歯薬保健学研究院 統合バイオ研究室教授)
リサーチアソシエイト 中井 信裕(なかい のぶひろ)
研究員 玉田 絋太(たまだ こうた)
神経グリア回路研究チーム
チームリーダー 平瀬 肇(ひらせ はじめ)
研究員 毛内 拡(もうない ひろむ)
ライフサイエンス技術基盤研究センター
センター長 渡辺 恭良(わたなべ やすよし)
生体機能評価研究チーム
チームリーダー 尾上 浩隆(おのえ ひろたか)
研究員 水間 広(みずま ひろし)
日本医科大学 大学院医学研究科
薬理学分野
教授 鈴木 秀典(すずき ひでのり)
准教授 齋藤 文仁(さいとう ふみひと)
講師 永野 昌俊(ながの まさとし)
衛生学公衆衛生学分野
教授 川田 智之(かわだ ともゆき)
講師 稲垣 弘文(いながき ひろふみ)
広島大学 大学院医歯薬保健学研究院
統合バイオ研究室
助教(研究当時) 渡辺 康仁(わたなべ やすひと)
大学院生(研究当時) 川本 明子(かわもと あきこ)
神経生理学研究室
教授 橋本 浩一(はしもと こういち)
特任助教(研究当時)河村 吉信(かわむら よしのぶ)
東京大学 大学院医学系研究科
神経生理学分野
教授 狩野 方伸(かのう まさのぶ)
准教授(研究当時)喜多村 和郎(きたむら かずお)
神経細胞生物学分野
教授 岡部 繁男(おかべ しげお)
技術職員 佐藤 由佳(さとう ゆか)
北海道大学 大学院医学研究院
解剖学分野
教授 渡辺 雅彦(わたなべ まさひこ)
助教 宮崎 太輔(みやざき たいすけ)
背景
自閉症(自閉スペクトラム症)は、社会的コミュニケーション能力の欠如(対人関係を築くことが苦手、視線を合わせない、人の話したことをオウム返しするなど)や、繰り返し行動(毎日決まった行動をし、予定外の行動は取れないなど)が特徴的な発達障害の一つです。また、音や光、触られることに対して過敏に反応するなどの感覚異常の症状を持ちます。症状は対処療法によって和らぐ場合もありますが、生涯にわたり表出します。家族は自閉症患者の保護や介護に多くの時間と労力を費やすため、社会的・経済的困難を抱えます。また、自閉症の罹患率は年々増加しており、2010年のアメリカの調査では約68人に1人が自閉症だといわれています注2)。そのため自閉症の症状を緩和させる療法の発見に向けて、原因解明が社会的に強く求められていますが、自閉症の発症メカニズムはほとんど分かっていません。
近年の遺伝学的研究により自閉症患者では、単一遺伝子変異やゲノム変異であるコピー数多型[2](重複や欠失によってゲノムの一部領域の数が変化すること)が見つかっています。このような遺伝的な異常は、親から受け継いだ変異だけではなく、新しく発生した変異(精子や卵子が形成されるときにランダムに生じるもの)にも由来します。その種類は非常に多く、自閉症の原因究明が困難な理由の一つとなっています(図1A)。
内匠シニアチームリーダーらの研究チームは2009年に、染色体工学の手法を用いて、ヒトのコピー数多型(15番染色体重複)と同じゲノム異常を持つモデルマウス(15番染色体重複モデルマウス)を作製し、このマウスがヒトの自閉症のような行動を示すことを報告しました注3)。さらに、15番染色体重複モデルマウスの脳内神経伝達物質を定量的に調査し、発達期においてセロトニン量が減少していることを明らかにしました(図1B)。また、セロトニンの異常は自閉症患者でも確認されているため、このモデルマウスを詳細に解析することで自閉症の発症メカニズム解明に近づくことができると考えられます。
注2)Investigators DDMNSYP, (CDC) CfDCaP. Prevalence of autism spectrum disorder among children aged 8 years - autism and developmental disabilities monitoring network, 11 sites, United States, 2010. MMWR Surveill Summ. 2014;63(2):1-21.
注3)Nakatani J et al."Abnormal behavior in a chromosome-engineering mouse model for human 15q11-13 duplication seen in autism." Cell 137: 1235-1246,(2009).
研究手法と成果
ヒトでもマウスでもセロトニンは、中脳にある神経核の一つである縫線核のセロトニン神経細胞から放出されます。共同研究グループはまず、PETイメージング[3]を用いて、15番染色体重複モデルマウスの脳活動を測定しました。その結果、モデルマウスでは縫線核の活動が低下していました(図2A)。また、セロトニン神経細胞に対する電気活動を調べたところ、興奮性の入力が低下していました。これらは脳内セロトニン減少を示す有力な手がかりとなります。
セロトニン神経は脳全体に投射しており、神経発達の重要な因子として知られています。大脳皮質の中でも体性感覚皮質は、セロトニン神経の投射を強く受けており、また体からの触覚情報の入力を受けている脳領域です。マウスの体性感覚皮質にあるバレル野と呼ばれる領域はひげ感覚入力の受け手で、発達期のセロトニン異常はバレル野構造を変化させることが知られています。また、自閉症患者では感覚異常を示すことが多いことが特徴です。そこで、モデルマウスの感覚刺激応答を調べたところ、ひげ刺激に反応するバレル野の応答異常が認められました(図2B)。これは、感覚刺激の入力に対するバレルの応答(シグナル)に対して、その周辺エリアの応答(ノイズ)が高くなる現象です。このようにシグナルノイズ比(S/N比)[4]が悪化する応答異常は、自閉症患者の機能的核磁気共鳴画像法(f-MRI)[5]研究でも報告されています。
また、体性感覚皮質を組織学的に解析したところ、15番染色体重複モデルマウスでは抑制シナプスが減少していました。さらに、モデルマウスの体性感覚皮質の電気活動を調べたところ、抑制性入力が減少していました。抑制機能が低下していると周辺エリアの応答が高くなります。抑制性入力の減少が、シグナルノイズ比を悪化させ、感覚情報のチューニング機能に障害を与える原因と考えられます。
このモデルマウスは、生後間もない時期からセロトニンが減少しています。共同研究チームは発達期のセロトニン量を増やすことで、これらのモデルマウスでみられる異常が改善するのではないかと考えました。そこで、発達期のセロトニンを増やす方法として、SSRI(選択的セロトニン再取り込み阻害剤)[6]を生後3日齢から離乳(生後21日齢)まで長期間投与するアプローチを使用しました。SSRIにはセロトニンの効果を高める役割があります。その結果、SSRI投与マウスでは体性感覚皮質の抑制性入力および、縫線核のセロトニン神経への興奮性入力が改善し、脳内セロトニン量が回復しました(図2C)。
最後に、15番染色体重複モデルマウスにみられる社会性行動異常が、セロトニンを増やす療法によって改善するかどうかを行動試験[7]で調べました。SSRIを投与した仔マウスでは、鳴き方の発達の遅れ(コミュニケーション障害)が改善しました。また、空間学習に基づく繰り返し行動異常は改善しなかったものの、社会性の行動指標(社会性相互作用)は改善しました(図2D、E)。
本研究によって、15番染色体重複モデルマウスの生体内におけるセロトニン神経系の異常を起因として脳内セロトニンが減少し、それに伴って大脳皮質の感覚応答異常が引き起こされることが明らかとなりました。さらに、セロトニン神経系を亢進させることで自閉症様症状の一部が緩和できることが分かりました。
今後の期待
本研究成果は、セロトニン療法が自閉症に効果的である可能性を示すものであります。抗うつ薬として使用されているSSRIは、過去にも自閉症患者に対して投与されてきた実績がありますが、その効果は報告ごとに肯定的であったり否定的であったりとさまざまで結論が出ていません。
また、セロトニンは過剰になっても欠乏しても悪影響が出るため適切な量の調節が必要です。そのため、セロトニン療法はセロトニンが減少している自閉症患者に選択的にアプローチすることが重要だと考えられます。また、セロトニン量は食事や運動によって増えると考えられています。本研究の知見は今後、自閉症の適切な治療法の開発にも貢献するものと期待できます。
原論文情報
- Nobuhiro Nakai*, Masatoshi Nagano*, Fumihito Saitow*, Yasuhito Watanabe§, Yoshinobu Kawamura, Akiko Kawamoto, Kota Tamada, Hiroshi Mizuma, Hirotaka Onoe, Yasuyoshi Watanabe, Hiromu Monai, Hajime Hirase, Jin Nakatani, Hirofumi Inagaki, Tomoyuki Kawada, Taisuke Miyazaki, Masahiko Watanabe, Yuka Sato, Shigeo Okabe, Kazuo Kitamura, Masanobu Kano, Kouichi Hashimoto, Hidenori Suzuki§, Toru Takumi§(*Equal contribution to this work, §Corresponding authors), "Serotonin Rebalances Cortical Tuning and Behavior Linked to Autism Symptoms in 15q11-13 CNV Mice", Science Advances, doi: 10.1126/sciadv.1603001
発表者
理化学研究所
脳科学総合研究センター 精神生物学研究チーム
チームリーダー 内匠 透(たくみ とおる)
日本医科大学 大学院医学研究科 薬理学分野
教授 鈴木 秀典(すずき ひでのり)
 鈴木、斎藤、永野、中井、内匠(左から)
鈴木、斎藤、永野、中井、内匠(左から)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
学校法人日本医科大学 総務部 広報課
Tel: 03-5814-6242 / Fax: 03-3824-2822
kouhouka [at] nms.ac.jp(※[at]は@に置き換えてください。)
産業利用に関するお問い合わせ
理化学研究所 産業連携本部 連携推進部
お問い合わせフォーム
補足説明
- 1.セロトニン
神経伝達物質の一つ。セロトニンは神経発達における重要な調節因子であり、社会性行動だけでなく攻撃性行動や性行動との関係性も示唆されている。セロトニンの受容体は脳内に(マウス脳では)13種類あり、その機能はさまざまで、発現している受容体の種類特異的に神経細胞を興奮させたり抑制させたりする。セロトニンは、食事から摂取したアミノ酸のトリプトファンから脳内で合成される。日光を浴びることやリズミカルな運動をすることで、体内のセロトニン量が増加することが知られている。また、睡眠ホルモンであるメラトニンの前駆体でもある。 - 2.コピー数多型
染色体の一部領域が重複したり欠失することによって、ゲノムに含まれる遺伝子数が変化すること。ダウン症の原因である21番染色体トリソミー(21番染色体が三つになること)も、コピー数多型の一つである。今回の自閉症モデルマウスは、ヒト15番染色体の一部に相当する領域が重複するコピー数多型を持っている。 - 3.PETイメージング(陽電子放射断層撮影法)
陽電子を放出する陽電子放出核種(放射性同位体の一種)をプローブとして、生体内のプローブ分布を画像化する手法。人体に害のない微量のPETプローブを体内に注入し、その集積を非侵襲的に(生体を傷つけずに)3次元画像化し定量することができる。今回の実験ではグルコース代謝量を測定するために、18F-FDG(フルオロデオキシグルコース)をプローブに用いた。活動が盛んな部位ではより多くグルコースを取り込むため、18F-FDGが集積される。PETはPositron Emission Tomographyの略。 - 4.シグナルノイズ比(S/N比)
一般的には、測定時のシグナル(信号)とノイズ(雑音)の比率を示す。シグナルノイズ比が大きいほど、精度の高い測定データが得られる。 - 5.機能的核磁気共鳴画像法(f-MRI)
核磁気共鳴画像法(MRI)を利用して、ヒトの脳活動における神経活動の高まりを血流動態反応で視覚化する方法の一つ。 - 6.SSRI(選択的セロトニン再取り込み阻害剤)
セロトニンの効果を増強させる薬。セロトニンは、シナプスから放出された後に回収されて再利用される。その回収作業を担うトランスポーターの働きを阻害する。主に抗うつ薬としてうつ病患者に投与される。 - 7.行動試験
マウスは社会性の高い動物である。集団で飼育すると、互いにコミュニケーションをとり、社会的ヒエラルキーを形成する。マウスでは、自閉症様症状に関係する行動試験がいくつも開発されている。仔マウスの鳴き声を測定することで、鳴き方の発達の遅れ(コミュニケーション障害)を調べることができる。空間学習試験では、一度覚えさせた経路を別の経路に変更することで、前に覚えた記憶から新しい記憶へ置き換える能力(繰り返し行動)を調べることができる。社会性行動試験では、マウス同士の接触時間(社会的相互作用)を測定することで、社会性指標を測定することができる。
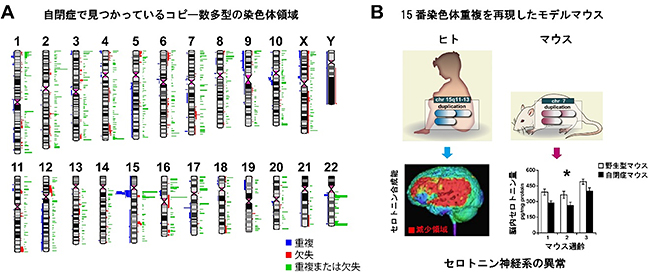
図1 コピー数多型の染色体領域と15番染色体重複モデルマウス
A:青・赤・緑の色棒の横の長さは、ヒト染色体領域における重複および欠失の報告数(患者数ではなく論文の数)を表している。15番染色体の一部の領域(15q11-13領域)に、重複異常が集中して見つかっている。米国のシモン財団が開設している自閉症研究サイトSFARI(英語)の登録情報をもとに作成した。また、2016年現在、コピー数多型は2172領域が見つかっている。
B:ヒトの染色体15q11-13重複と同じゲノム異常を持つモデルマウスでは、脳内セロトニンが減少している(玉田らの報告、2010年PLoS One)。また、自閉症患者で脳内セロトニン合成能が低下していることが報告されている。セロトニン神経系の異常が自閉症症状に関係している可能性が示唆されていた。
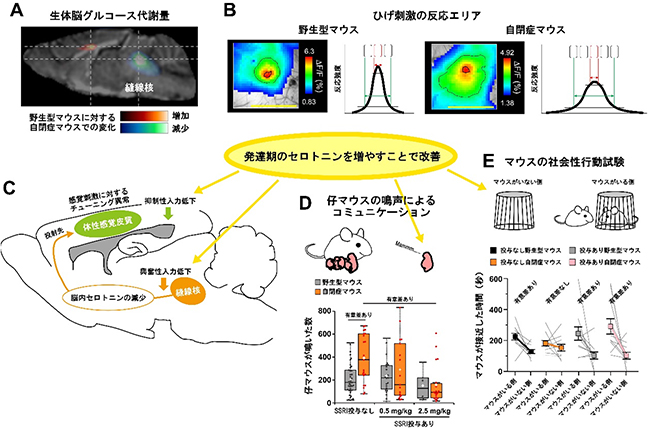
図2 今回の研究で明らかとなった15番染色体重複マウスの表現型
A:PETイメージングによって、モデルマウスでは中脳にある縫線核の活動が低下していることが明らかとなった。活動が増加している領域は前帯状皮質領域(不安を感じるときに活動が増加することが知られている領域)であるが、今回の研究では詳細に解析されていない。
B:ひげ刺激に対する体性感覚皮質バレル野の解析結果。経頭蓋(けいとうがい)カルシウムイメージングで測定したモデルマウスのひげ刺激反応エリアは、野生型マウスに比べて拡大している。野生型マウスは周辺バレルの応答が低く抑えられていて、ひげ刺激の入力シグナルがシャープに出るのに対し、モデルマウスでは周辺バレル応答が高くなり、シグナルノイズ比が低下する。
C:電気生理学実験では、縫線核のセロトニン神経に対する興奮性入力が低下しており、体性感覚皮質の錐体細胞に対する抑制性入力が低下していた。これらはSSRI(選択的セロトニン再取り込み阻害剤)の投与により、発達期のセロトニンを増やすことで改善した。
D:モデルマウスでは、離乳前の仔マウスの鳴声によるコミュニケーションに異常が認められる。コミュニケーション異常は、SSRI投与によりセロトニンを増やすことで改善した。
E:発達期にセロトニンを増やしたマウスを用いて、成長後に社会性行動試験を行った。SSRI投与なしのモデルマウスでは社会性が低下しているのに対して、SSRI投与ありの自閉症マウスでは社会性が改善した。
