要旨
理化学研究所(理研)横山構造生物学研究室の横山茂之上席研究員とライフサイエンス技術基盤研究センター非天然型アミノ酸技術研究チームの坂本健作チームリーダーらの共同研究グループ※は、人工アミノ酸を用いて抗体医薬[1]の化学修飾に有用な部位を特定し、多様な機能性を持つ抗体「Variabody」の作製に成功しました。
抗体医薬は、疾患の原因となる標的分子に特異的に結合して薬効を発揮するため、副作用が少なく毒性が低いというメリットがあります。近年、抗体に薬剤を結合した武装抗体[2]や、一つの抗体で二つの標的分子に結合する二重特異性抗体[3]など、化学修飾技術を応用して抗体を高機能化する医薬開発が進められています。横山上席研究員と坂本チームリーダーらはこれまでに、天然アミノ酸にはない機能を持つ人工アミノ酸をタンパク質に導入する技術開発を進め、2010年に遺伝暗号[4]を人為的に書き換えた大腸菌RFゼロ株[5]の開発に成功しています注1)。これにより、RFゼロ株を用いてタンパク質の複数の部位に人工アミノ酸をデザイン通りに導入する技術を確立しました。しかし、この技術の抗体への応用については検証していませんでした。
今回、共同研究グループは、大腸菌RFゼロ株で生産したTra-Fab抗体[6]に人工アミノ酸の「o-Az-Z-Lys[7]」を導入することで、化学修飾に適した部位を多数特定しました。また、これらの部位を利用して、Tra-Fab抗体に抗がん剤を結合させた武装抗体や、二つのTra-Fab抗体をさまざまな組み合わせで連結した二量体Tra-Fab抗体[6]を作製できることを示しました。さらに、その連結部位をうまく選ぶことにより、抗体をアンタゴニスト[8](拮抗作用)からアゴニスト[8](作動作用)に変えられることを確認しました。これは、2分子の抗体が連結の仕方によって新しい機能を獲得できることを示しています。共同研究グループは、この連結技術および作製された抗体を「Variabody」と名付けました。
今後、Variabodyは抗体の医療・産業応用をより広げる新しい形式として、抗体医薬の開発に貢献するものと期待できます。なお、理研および協和発酵キリン株式会社は、Variabodyに関する特許を共同出願しています。
本研究成果は、米国の科学雑誌『Bioconjugate Chemistry』掲載に先立ち、オンライン版(7月20日付け:日本時間7月21日)に掲載されます。
注1)Mukai T, Hayashi A, Iraha F, Sato A, Ohtake K, Yokoyama S, Sakamoto K. "Codon reassignment in the Escherichia coli genetic code." Nucleic Acids Res.2010 38(22): 8188-8195
※共同研究グループ
理化学研究所
横山構造生物学研究室
上席研究員 横山 茂之(よこやま しげゆき)
研究員 倉谷 光央(くらたに みつお)
研究員 柳沢 達男(やなぎさわ たつお)
ライフサイエンス技術基盤研究センター 構造・合成生物学部門
生命分子制御研究グループ 非天然型アミノ酸技術研究チーム
チームリーダー 坂本 健作(さかもと けんさく)
研究員 大竹 和正(おおたけ かずまさ)
上級技師 松元 明子(まつもと あきこ)
テクニカルスタッフⅠ 天野 芳美(あまの よしみ)
協和発酵キリン株式会社
マネジャー 白石 泰久(しらいし やすひさ)
研究員 加藤 明文(かとう あきふみ)
研究員 木村 要(きむら かなめ)
背景
抗体医薬は、疾患の原因となる標的分子に特異的に結合して薬効を発揮するため、副作用が少なく毒性が低いというメリットがあります。このため、これまで重い副作用が知られていたがんをはじめ、関節リウマチなどの自己免疫疾患やアルツハイマー病といった有効な治療法が確立されていない病気の治療薬として大きな期待が寄せられています。
近年、抗体に薬剤を結合した武装抗体や、一つの抗体で二つの標的分子に結合する二重特異性抗体など、化学修飾技術を応用して抗体を高機能化する医薬開発が行われています。人工アミノ酸を用いる化学修飾技術の開発では、これまでタンパク質への人工アミノ酸の適切な導入部位を見いだすことが難しく、抗体を自由にデザインし高機能化する上での障害になっていました。
横山上席研究員と坂本チームリーダーらは2002年に、哺乳類培養細胞において人工アミノ酸のチロシン誘導体をタンパク質へ部位特異的に導入する技術注2)を、2008年にピロリシルトランスファーRNA(tRNA)合成酵素の立体構造情報を活用し、人工アミノ酸のピロリシン誘導体を導入する技術注3)を、2010年には遺伝暗号を人為的に書き換えた大腸菌RFゼロ株の作製技術など、人工アミノ酸をタンパク質に導入する技術の開発を行ってきました。またこれらの技術を用いて、ポリペプチドや酵素などをモデルとして、複数の部位に人工アミノ酸をデザイン通りに導入してタンパク質を高機能化させる技術を確立しましたが、抗体への応用については検証していませんでした。
そこで今回は、抗体医薬に関する知見を持つ協和発酵キリン株式会社と共同研究グループを立ち上げ、人工アミノ酸導入技術を実際の抗体への応用研究に生かすべく研究に取り組みました。
注2)Nucleic Acids Res.2002 Nov 1;30(21):4692-9
注3)Chem. Biol. 2008 15:1187–1197.
研究手法と成果
トラスツズマブ(Trastuzumab)[9]は乳がんの抗体医薬で、乳がん細胞の表面に高発現しているタンパク質HER2[10]に特異的に結合して攻撃します。抗体(全長抗体)はY字の形をしていて、上に突き出した二つの腕の部分のそれぞれをFabと呼びます。このFab部分が抗原を認識するため、Fab部分だけ切り離したFab抗体[6]の開発が行われています。トラスツズマブを断片化したFab抗体を、共同研究グループは便宜的にTra-Fab抗体と呼んでいまます。
共同研究グループはまず、大腸菌W3110株をRFゼロ株化し、このRFゼロ株からTra-Fab抗体を効率よく発現させました。続いて、このTra-Fab抗体のFab定常領域[11]のさまざまな部位に、化学修飾における反応性に優れる人工アミノ酸の「o-Az-Z-Lys」を導入し、それぞれのo-Az-Z-Lysに蛍光基を結合させました。そして、蛍光の強度から人工アミノ酸が結合しやすい部位を多数特定しました。
次に、Tra-Fab抗体で特定された人工アミノ酸が結合しやすい部位の中から、o-Az-Z-Lys導入によって立体構造に最も影響を及ぼしにくいと考えられる領域にある六つの部位(CLκ-197、CLκ-155、CLκ-191、CH1-177、CH1-199、CH1-131)を選び出しました(図1)。これら六つの部位がどれくらい化学修飾に適しているかを調べたところ、全ての部位においてo-Az-Z-Lys導入に対して90%以上の反応性が確認されました。
また、o-Az-Z-LysをTra-Fab抗体に導入した機能抗体の有効性を確認するため、六つの部位のうち、特に反応性の高いCLκ-155またはCH1-177にo-Az-Z-Lysを導入し、それぞれのo-Az-Z-Lysに抗がん剤(DM1)を結合させて2種類の武装抗体(Tra-Fab—DM1)を作製しました。これらの武装抗体を、標的となるHER2が細胞表面に高発現している乳がん細胞(SK-BR-3)に加えたところ、両方の武装抗体において高い細胞傷害性がみられました(図2左)。一方、HER2の発現が低い乳がん細胞(MCF-7)に対しては、ほとんど細胞傷害活性がみられませんでした(図2右)。これらの結果から、作製した武装抗体が標的分子のHER2が高発現している乳がん細胞のみを特異的に攻撃することが明らかとなり、その有効性が確認できました。
さらに、選び出した六つの部位にそれぞれo-Az-Z-Lysを導入した6種類のTra-Fab抗体を二つずつリンカーで連結させ、二量体Tra-Fab抗体を作製しました。この連結させるTra-Fab抗体の組み合わせは、全部で21種類(6+5+4+3+2+1)となります。
次に、連結させた全ての二量体Tra-Fab抗体の機能を、HER2が高発現している乳がん細胞(BT-474)を用いて評価しました(図3上)。その結果、21種類のうち2種類(CL1-199/CLκ-197とCL1-199/CL1-177)では、濃度の上昇に伴いBT-474細胞の増殖率が増加することを見いだしました。これにより、二量体ではないTra-Fab抗体をアンタゴニスト(拮抗作用)からアゴニスト(作動作用)に変化させることができました(図3下)。これは、2分子の抗体が連結の仕方によって新しい機能を獲得できることを示しています。
本研究では、Tra-Fab抗体において、上述の六つの部位以外にも多数の化学修飾に適した部位を新たに見つけています。これらの部位をうまく組み合わせて連結させることにより、多様なデザインと機能性を持たせた二量体Fab抗体を作製できることから、この連結技術および作製された抗体を「Variabody」と名付けました。Variabodyという名称は“a novel antibody format allowing various connections”に由来しています。作製方法の詳細を図4に示しますが、手間のかかる従来法に比べてかなり簡便になりました。
なお、理研と協和発酵キリン株式会社は、Variabodyに関する特許を共同出願しています。
今後の期待
Tra-Fab抗体の化学修飾に適した人工アミノ酸導入部位を複数同定したことにより、武装抗体をデザインすることが容易になると考えられます。また、この部位を利用して2分子の抗体を連結させる「Variabody」は今後、抗体の医療・産業応用を広げる新しい抗体の形式として、抗体医薬の開発に貢献するものと期待できます。
原論文情報
- Kato, A. Kuratani,M. Yanagisawa T. Ohtake, K. Hayashi,A. Amano,Y. Kimura, K. Yokoyama,S. Sakamoto,K. and Shiraishi, Y., "An extensive survey of antibody invariant positions for efficient chemical conjugation using expanded genetic codes", Bioconjugate Chemistry, doi: 10.1021/acs.bioconjchem.7b00265
発表者
理化学研究所
上席研究員研究室 横山構造生物学研究室
上席研究員 横山 茂之(よこやま しげゆき)
ライフサイエンス技術基盤研究センター 構造・合成生物学部門 生命分子制御研究グループ 非天然型アミノ酸技術研究チーム
チームリーダー 坂本 健作(さかもと けんさく)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
産業利用に関するお問い合わせ
理化学研究所 産業連携本部 連携推進部
お問い合わせフォーム
補足説明
- 1.抗体医薬
免疫反応における、抗体が抗原を認識する仕組みを利用した医薬品。抗体医薬はがん細胞などの標的のみを認識して狙い撃ちするため、薬効が高く副作用が少ないというメリットがある。 - 2.武装抗体
標的の細胞を認識する抗体と活性本体である薬剤(抗がん剤)を適切なリンカーで連結した抗体医薬のこと。その多くはがん治療を目的として開発が進められている。 - 3.二重特異性抗体
通常、抗体は1種類の抗原を認識して結合するが、二重特異性抗体は2種類の異なる抗原を認識して結合する性質を持つため、相乗効果を発揮し、治療効果を高めることが期待されている。 - 4.遺伝暗号
タンパク質を構成するアミノ酸の並び方は、そのタンパク質の遺伝子(DNA)の中の塩基配列に対応している。三つの塩基がひとまとまりになって一つのアミノ酸に対応しており、この3塩基の並びを「コドン」と呼ぶ。全部で64通りのコドンが存在するが、そのうちの61種類のコドンがアミノ酸を意味しており、例えばUUUはフェニルアラニンである。残り3つのコドン(UAA、UGA、UAG)はタンパク質合成終了を意味する「終止コドン」であり、遺伝子の最後に現れる。このようなコドンとアミノ酸などの対応関係を「遺伝暗号」と呼び、この対応関係に基づいて遺伝子の塩基配列をタンパク質中のアミノ酸の配列に変換することができる。 - 5.RFゼロ株
「終止コドン」の一つのUAGコドンにはアミノ酸が対応していないため、このUAGコドンの位置に人工アミノ酸を導入する方法が一般的に用いられている。UAGコドンは元々「ストップ」の意味を持つことから、タンパク質合成をストップさせるための翻訳終結因子(RF-1)が結合する。このため、UAGコドンと人工アミノ酸の遺伝暗号としての対応関係は不完全であり、これまで人工アミノ酸の導入効率は低かった。遺伝暗号の変更は致死的な結果をもたらすが、理研らの研究チームはRF-1をコードする遺伝子を除去する条件を大腸菌で見いだし、UAGコドンが人工アミノ酸の意味を持つ遺伝暗号への変更に成功した。この大腸菌株をRFゼロ株と名付けた。 - 6.Tra-Fab抗体、二量体Tra-Fab抗体、Fab抗体
抗体(全長抗体)はY字の形をしていて、上に突き出した二つの腕の部分のそれぞれをFabと呼ぶ。このFab部分が抗原を認識するため、Fab部分だけ切り離したFab抗体の医薬開発が行われている。二量体Fab抗体は、二つのFab部分をリンカーで連結した抗体のこと。共同研究グループは、トラスツズマブを断片化し、Fab部分だけにしたFab抗体を便宜的にTra-Fab抗体と呼んでいる。この二量体Fab抗体が二量体Tra-Fab抗体である。

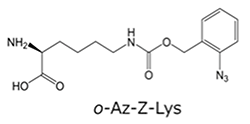
- 7.o-Az-Z-Lys
人工アミノ酸の一つ。メタン生成古細菌由来の「22番目のアミノ酸」として知られるピロリシンを認識する酵素を改変して開発された。タンパク質への部位特異的な導入技術に使用される。
- 8.アンタゴニスト、アゴニスト
生体内の受容体分子に結合して生理活性物質と同様の機能を持つ分子のこと。アンタゴニストは標的のタンパク質に結合するが活性を示さず、生理活性物質と拮抗的に働く。アゴニストは、生理活性物質と同じ、または類似の作用を示す。 - 9.トラスツズマブ(Trastuzumab)
トラスツズマブ(Trastuzumab)は、1998年に米国で認可された乳がんの抗体医薬。乳がんの中でも細胞表面にHER2が高発現するタイプは、治療が難しいとされていたが、トラスツズマブはHER2と結合することによりがん細胞のみを特異的に攻撃する。さらに、トラスツズマブが結合したがん細胞は、他の免疫細胞の攻撃も受け増殖が止まる。トラスツズマブによって、乳がんの効率的な治療の道が拓かれた。 - 10.HER2
細胞の表面に存在するタンパク質で、正常細胞においては細胞の増殖・分化などの制御に関わっている。HER2遺伝子に変異が起こると、HER2遺伝子はがん遺伝子として働く。HER2は、乳がん、胃がん、卵巣がんなど、多くのがん細胞の表面に発現している。ハーツーと読む。 - 11.Fab定常領域
抗体は、どの抗体でもほぼ一定の構造を持つ定常領域と、多様な異物に結合できるよう変化に富んだ構造を持つ可変領域とから構成されている。すなわち、抗原抗体反応において、Fab抗体の可変領域が特定の抗原を認識し結合する。
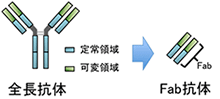
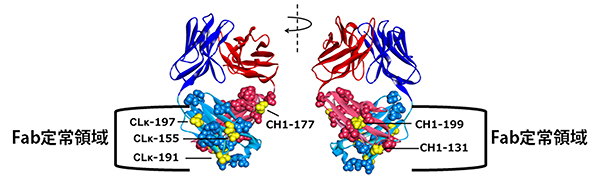
図1 Tra-Fab抗体の化学修飾に適した部位の位置
Tra-Fab抗体のFab定常領域において、黄色で示した6カ所が人工アミノ酸o-Az-Z-Lysの化学修飾に適している。なお、Fab定常領域の上の部分がFab可変領域で、Fab可変領域が抗原を認識する。
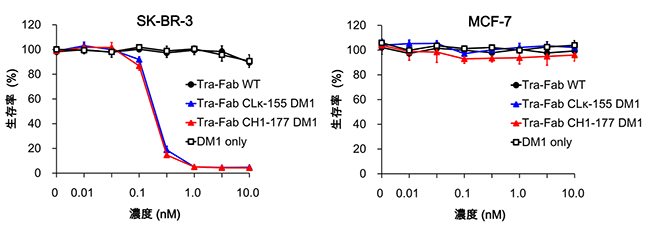
図2 乳がん細胞における武装抗体(Tra-Fab—DM1)の細胞傷害活性
左)HER2が細胞表面に高発現している乳がん細胞(SK-BR-3)に、作製した2種類の武装抗体を加えた場合。Tra-Fab抗体単体(●)と比較して、抗がん剤のDM1をTra-Fab抗体のCLκ-155部位に結合させたTra-Fab CLκ-155 DM1(青)およびCH1-177部位に結合させたTra-Fab CH1-177 DM1(赤)の濃度を上げると、SK-BR-3細胞の生存率が急激に下がった。一方、DM1のみ(□)ではSK-BR-3細胞の生存率にほとんど影響を与えなかった。DM1単独では細胞膜透過性が低く細胞内に取り込まれにくいため、細胞傷害活性を発揮しなかったと考えられる。
右)HER2の発現が低い乳がん細胞(MCF-7)に作製した武装抗体を加えた場合。MCF-7細胞の生存率に対しては、どちらの武装抗体もほとんど影響を与えなかった。すなわち、武装抗体はHER2に特異的に結合することが分かった。
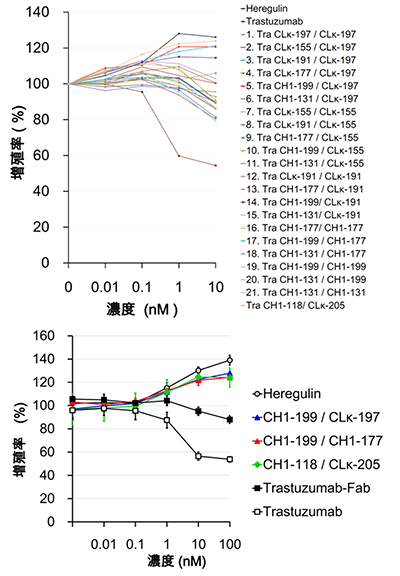
図3 高機能性抗体Variabodyの乳がん細胞(BT-474)増殖率への効果
上)六つの部位の全ての組み合わせ(6+5+4+3+2+1=21)で、二つのTra-Fab抗体を連結させることにより、合計21種類の抗体Variabodyを作製した。それら全ての機能評価(アンタゴニスト=拮抗作用、アゴニスト=動作作用の活性評価)を、HER2が高発現している乳がん細胞(BT-474)の増殖率をみることで行った。
下)Tra-Fab抗体(■)とTrastuzumab(□)はBT-474細胞に対して毒性があるため、濃度上昇に応じて増殖率は低下している。一方で、Tra-Fab抗体の連結の仕方によっては、逆に増殖率が上昇している。CH1-199/CLκ-197(青)、CH1-199/CH1-177(赤)の2種類について、アンタゴニスト(拮抗作用)からアゴニスト(作動作用)に変化させることに成功した。Heregulin(ヘリギュリン)はアゴニスト活性の指標として用いている。
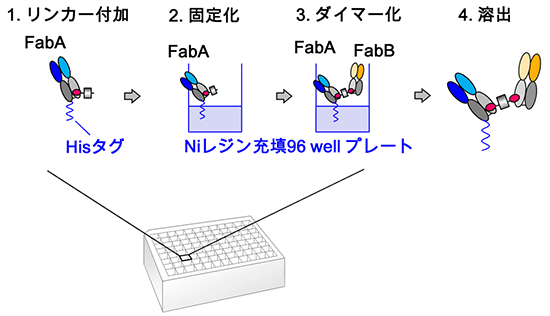
図4 高機能性抗体Variabodyの作製方法
96穴プレート上でニつのFab(FabAとFabB)をリンカーで連結させることにより、二量体Fab抗体を作製することができる。多数の化学修飾に最適な部位を使えるため、バリエーション豊富な二量体Fab抗体を容易に作製できる。この連結技術および作製された抗体を「Variabody」と名付けた。
