理化学研究所(理研)生命機能科学研究センター合成生物学研究チームの上田泰己チームリーダー(東京大学大学院医学系研究科機能生物学専攻システムズ薬理学教授)、丹羽康貴基礎科学特別研究員(研究当時)、神田元紀研究員、山田陸裕上級研究員らの国際共同研究グループ※は、レム睡眠に必須なニつの遺伝子を発見し、レム睡眠がほぼなくなっても生存するマウスの作製に初めて成功しました。
本研究成果は、レム睡眠の誘導や睡眠覚醒における神経伝達物質アセチルコリン[1]の役割の理解と、その異常により引き起こされる睡眠障害の病態解明や治療法の開発に貢献すると期待できます。
レム睡眠は、身体は寝ているのに脳は起きているという、覚醒とノンレム睡眠の中間の状態と考えられています。アセチルコリンはレム睡眠を誘導する分子として知られていますが、本当にレム睡眠に不可欠なものであるかはこれまで不明でした。今回、国際共同研究グループは、脳・神経系49部位のマイクロアレイ[2]による網羅的遺伝子解析、新しいマウス遺伝学ツール「tTR[3]」の開発、トリプルCRISPR法[4]などの個体レベルの遺伝学的手法を駆使することで、アセチルコリンの受容体遺伝子であるChrm1とChrm3が睡眠量の制御に重要な働きをしていることを明らかにしました。特に、その両方の遺伝子を同時に欠失させたマウスでは、レム睡眠がほとんど検出されないことを発見しました。
本研究は、米国のオンライン科学雑誌『Cell Reports』(8月28日付け:日本時間8月29日)に掲載されます。
※国際共同研究グループ
理化学研究所
生命機能科学研究センター
合成生物学研究チーム
チームリーダー 上田 泰己(うえだ ひろき)
(東京大学大学院 医学系研究科 機能生物学専攻 システムズ薬理学 教授)
基礎科学特別研究員(研究当時) 丹羽 康貴(にわ やすたか)
(現 客員研究員、筑波大学 国際統合睡眠医科学研究機構 助教)
研究員(研究当時) 神田 元紀(かんだ げんき)
(現 生命機能科学研究センター 網膜再生医療研究開発プロジェクト 研究員)
上級研究員 山田 陸裕(やまだ りくひろ)
研究員(研究当時) 砂川 玄志郎(すながわ げんしろう)
(現 生命機能科学研究センター 網膜再生医療研究開発プロジェクト 基礎科学特別研究員)
客員研究員 鵜飼 英樹(うかい ひでき)
客員技師 鵜飼(蓼沼) 磨貴(うかい(たでぬま) まき)
テクニカルスタッフI 藤島 博史(ふじしま ひろし)
高速ゲノム変異マウス作製支援ユニット
ユニットリーダー 隅山 健太(すみやま けんた)
テクニカルスタッフI(研究当時) 松本 直実(まつもと なおみ)
生体モデル開発ユニット
ユニットリーダー 清成 寛(きよなり ひろし)
生命医科学研究センター 大容量データ管理技術開発ユニット
ユニットリーダー 粕川 雄也(かすかわ たけや)
東京大学大学院 医学系研究科 機能生物学専攻 システムズ薬理学教室
助教 史 蕭逸(し しょうい)
クイーンズランド工科大学(オーストラリア)
講師 ディミトリ・ペリン(Dimitri Perrin)
大学院生 ジェイムズ・ギャロウェイ(James Galloway)
山口大学大学院 医学系研究科 神経解剖学講座
講師 升本 宏平(ますもと こうへい)
近畿大学 医学部 解剖学教室
教授 重吉 康史(しげよし やすふみ)
准教 授長 野護(ながの まもる)
※研究支援
本研究は、日本医療研究開発機構(AMED)「革新的先端研究開発支援事業(AMED-CREST)」の研究開発領域「生体恒常性維持・変容・破綻機構のネットワーク的理解に基づく最適医療実現のための技術創出」(研究開発総括:永井良三)(※)における研究課題「睡眠・覚醒リズムをモデルとした生体の一日の動的恒常性の解明」(研究代表者:上田泰己)、「革新的バイオ医薬品創出基盤技術開発事業」、日本学術振興会(JSPS)科学研究費補助金基盤研究S「哺乳類概日振動体の構成的な理解(研究代表者:上田泰己)」をはじめ基盤研究B、新学術領域研究、挑戦的萌芽研究、特別研究員奨励費およびクイーンズランド工科大学ECARD(Early Career Academic Recruitment and Development)grantの支援を受けて行われました。
(※)当該開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、科学技術振興機構(JST)より移管されたものです。
背景
動物の状態は覚醒、レム睡眠、ノンレム睡眠の三つに分類されます。この三つの状態は、脳波と筋電図で定義されます。その中でもレム睡眠は、筋電図上では寝ている(ノンレム睡眠時と似ている)のに脳波は起きている(覚醒時と似ている)という中間の状態です(図1)。「夢を見る」、「記憶が固定化される」などは、レム睡眠時に多く起こるイベントとして知られており、レム睡眠は動物にとって重要な状態だといわれています。一方で、レム睡眠がどのように作られるのかについては、神経回路レベルでは少しずつ詳細が明らかになってきましたが、分子・遺伝子レベルではほとんど分かっておらず、レム睡眠のない個体やレム睡眠がなくなっても生きられる個体の存在は、これまで全く知られていませんでした。
レム睡眠を制御する分子の候補としては、神経伝達物質のアセチルコリンがよく研究されており、いくつかの薬理学的な証拠が得られています。例えば、脳幹にアセチルコリン受容体作動薬を注射すると、レム睡眠様の状態が誘導されます。また、レム睡眠中の脳幹注2)や、レム睡眠および覚醒時の大脳皮質注3)において、アセチルコリンが豊富に放出されていることが報告されています。しかし、アセチルコリンを放出するコリン作動性神経[1]は脳内に広く投射しており、他の多くの神経に対してもさまざまな影響を与えると予想されています。さらに、脳内のアセチルコリン受容体には11種類のニコチン型受容体[5]と5種類のムスカリン型受容体[5]が存在し、一つ一つ調べるためには膨大な時間と労力がかかります。このため、アセチルコリンがレム睡眠に本当に不可欠であるかどうかはこれまで不明でした。
そこで、国際共同研究グループは、マウスにおけるアセチルコリンの役割を、個体レベルの包括的な遺伝学的手法を駆使して、評価することを試みました。
- 注2) Tohru Kodama, Yasuro Takahashi and YoshikoHonda."Enhancement of acetylcholine release during paradoxical sleep in the dorsal tegmental field of the cat brain stem". Neuroscience Letters, 1990.
- 注3) Leonor M. Teles-Grilo Ruivo, Keeley L. Baker, Michael W. Conway, Peter J. Kinsley, Gary Gilmour, Keith G. Phillips, John T.R. Isaac, John P. Lowry and Jack R. Mellor. "oordinated Acetylcholine Release in Prefrontal Cortex and Hippocampus Is Associated with Arousal and Reward on Distinct Timescales". Cell Reports, 2017
研究手法と成果
国際共同研究グループはまず、マイクロアレイによる脳・神経系49部位の網羅的遺伝子発現解析を行い、睡眠中枢と考えられている領域(視索前野/基底前脳部位)の特徴として、「TrkA」という遺伝子が特異的に発現していることを見いだしました。
次に、TrkA遺伝子を発現している神経細胞が睡眠中枢においてどのような働きをしているかを調べるため、他の神経細胞は無傷のままTrkA遺伝子発現細胞のみの働きを破傷風毒素(Tetanus toxin、以下TeNT)で阻害できる「TrkA-TeNTマウス」を樹立しました。TeNTが発現している細胞はシナプス放出が阻害されるため、その神経細胞から次の神経細胞への情報伝達が行われなくなります。このTrkA-TeNTマウスの睡眠状態を評価したところ、総睡眠量が対照マウスよりも大幅に減少したことから、TrkA遺伝子が発現している神経細胞が睡眠量の制御にとって重要であることが示されました(図2)。
TrkA遺伝子を発現する神経細胞は、コリン作動性神経とそれ以外の神経を含む多様な細胞集団です。そこで、どの種類のTrkA遺伝子発現細胞が睡眠量の制御に重要かを確かめるために、「tTR」と名付けた遺伝学ツールを新たに開発し、細胞の絞り込みを行いました。tTRを発現させた細胞では、TeNTの発現が抑えられます。TrkA-TeNTマウスのコリン作動性神経(コリンアセチルトランスフェラーゼ[1]をコードするChAT遺伝子を発現する細胞)にのみtTRを発現させた「TrkA-TeNT/ChAT-tTRマウス[6]」では、TrkA-TeNTマウスで減少した睡眠量の回復が観察されました。このことから、TrkA遺伝子発現する神経細胞のうち、コリン作動性神経が睡眠量の制御に重要であることが分かりました(図3)。
さらに、アセチルコリン受容体の遺伝子を欠失させたマウスの睡眠状態を評価することで、どの受容体が睡眠量の制御に重要かを調べました。まず、1次スクリーニングとして、トリプルCRISPR法でアセチルコリン受容体遺伝子を一つずつ欠失させたマウスを作製し、高速に睡眠表現型を解析することができるSSS法[7]により睡眠量を測定しました。その結果、ニつのムスカリン型アセチルコリン受容体(Chrm1またはChrm3)を欠失したマウスにおいて、TrkA-TeNTマウスで見られたような睡眠量の著しい減少が観察されました(図4上)。
次に、Chrm1またはChrm3遺伝子の欠失マウスの睡眠量を、脳波・筋電図測定[8]を用いてより詳しく解析したところ、Chrm1遺伝子欠失マウスはレム睡眠とノンレム睡眠の時間が共に減少(それぞれ約34分と117分短縮)していました。一方、Chrm3遺伝子欠失マウスではノンレム睡眠量のみが著しく減少(約153分短縮)し、レム睡眠は1回の持続時間が短くなり頻度が増える影響が見られたものの、総量に変化はありませんでした(図4中)。これらの違いからレム睡眠、ノンレム睡眠の制御にChrm1、Chrm3がそれぞれ違った役割を持つことが示されました。すなわち、Chrm1遺伝子はレム睡眠、Chrm3遺伝子はノンレム睡眠を主に制御していると考えられます(図4下)。
そこで、Chrm1とChrm3の相乗的な機能を探るために、両方の遺伝子を同時に欠失させたマウスを作製し、睡眠量を解析しました。この両遺伝子欠失マウスは、レム睡眠量がほとんど検出不可能なレベルにまで減少するという、単独の遺伝子欠失マウスにはない表現型が現れました(図5)。この結果により、ムスカリン性アセチルコリン受容体遺伝子Chrm1とChrm3の両方が、睡眠量調節、特にレム睡眠を引き起こすために不可欠であることが分かりました。
今後の期待
本研究により、レム睡眠の有無を決定する遺伝子を初めて同定しました。本成果を利用して、レム睡眠を特異的に操作する技術や薬剤が開発され、さらなる睡眠研究ならびに睡眠障害に対する効果的な治療薬の開発が進展すると期待できます。
また、今回の研究で初めてレム睡眠がなくなっても生きられる個体の存在を確認しました。このことは、レム睡眠が動物にとって本当に必須なのか、必須であるのならどのような役割を持っているのか、そして睡眠はどこまで削れるのかという問いを、改めて検証するきっかけになると考えられます。ニつのアセチルコリン受容体遺伝子Chrm1とChrm3を欠損したマウスを見る限りでは、少なくともレム睡眠はなくてもよさそうです。
なお、本研究で使用した視索前野/基底前脳領域の遺伝子発現解析結果は、「BrainStars(英語)」で公開しています。
原論文情報
- Yasutaka Niwa*, Genki N. Kanda*, Rikuhiro G. Yamada*, Shoi Shi, Genshiro A. Sunagawa, Maki Ukai-Tadenuma, Hiroshi Fujishima, Naomi Matsumoto, Koh-hei Masumoto, Mamoru Nagano, Takeya Kasukawa, James Galloway, Dimitri Perrin, Yasufumi Shigeyoshi, Hideki Ukai, Hiroshi Kiyonari, Kenta Sumiyama, Hiroki R. Ueda# (*Co-first,#Lead contact), "Muscarinic acetylcholine receptors Chrm1 and Chrm3 are essential for REM sleep", Cell Reports, 10.1016/j.celrep.2018.07.082
発表者
理化学研究所
生命機能科学研究センター 合成生物学研究チーム
チームリーダー 上田 泰己(うえだ ひろき)
(東京大学大学院 医学系研究科 機能生物学専攻 システムズ薬理学 教授)
基礎科学特別研究員(研究当時) 丹羽 康貴(にわ やすたか)
(現 客員研究員、筑波大学 国際統合睡眠医科学研究機構 助教)
研究員 神田 元紀(かんだ げんき)
上級研究員 山田 陸裕(やまだ りくひろ)
お問い合わせ先
山岸 敦(やまぎし あつし)
Tel: 078-304-7138 / Fax: 078-304-7112
E-mail:ayamagishi[at]riken.jp
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
東京大学 医学部 総務係
Tel: 03-5841-3304 / Fax: 03-5841-8585
E-mail:ishomu[at]m.u-tokyo.ac.jp
産業利用に関するお問い合わせ
AMED事業に関するお問い合わせ先
革新的先端研究開発支援事業(AMED-CREST)
日本医療研究開発機構(AMED) 基盤研究事業部 研究企画課
〒100-0004 東京都千代田区大手町1-7-1
Tel: 03-6870-2224
E-mail:kenkyuk-ask[at]amed.go.jp
革新的バイオ医薬品創出基盤技術開発事業
日本医療研究開発機構(AMED) 創薬戦略部 医薬品研究課
〒100-0004 東京都千代田区大手町1-7-1
Tel: 03-6870-2219 / Fax: 03-6870-2244
E-mail:kaku-bio27[at]amed.go.jp
※上記の[at]は@に置き換えてください。
補足説明
- 1.アセチルコリン、コリン作動性神経、コリンアセチルトランスフェラーゼ
アセチルコリンは神経伝達物質の一つ。コリンアセチルトランスフェラーゼ(コリンアセチル転移酵素)の酵素作用によりコリンとアセチルCoAから合成され、シナプスに放出される。アセチルコリンを産生・伝達する神経はコリン作動性神経と呼ばれ、中枢神経系に広く分布し、記憶、睡眠、行動など、さまざまな神経活動の制御に関わることが知られている。 - 2.マイクロアレイ
塩基配列が既知の多種類の遺伝子のDNAをプローブとして、プレート上に規則正しく貼付けておく。調べたい細胞からmRNAを採取し、蛍光標識する。これをプレート上に貼付けられたDNAと反応させ、蛍光強度を読み取ることにより、mRNAの発現量を網羅的かつ定量的に調べることができる。 - 3.tTR
遺伝子導入により細胞特異的に発現させた遺伝子を、さらに細胞を絞り込んで発現抑制させるために開発した遺伝学ツール。細胞特異的な標的遺伝子の発現に用いる転写活性化因子tTA(tetracycline transactivator)に対して、tTRはtTAを阻害するタンパク質(tTA repressor)としてデザインされたものである。tTA発現細胞のうち一部の細胞でtTAを同時発現させると、その細胞でのみ標的遺伝子の発現をキャンセルすることができる。tTAとtTRを用いたシステムは、ハエの遺伝学実験で用いられる転写因子Gal4と転写抑制因子Gal80に相当する。tTRはtTAの転写活性化部位を転写抑制因子KRABドメインに変更することで作製され、tTAのホモ二量体化の阻害とtetO配列(tTAが結合するDNA配列)の占有による転写抑制の二つを作用機序として持つと考えられる。 - 4.トリプルCRISPR法
共同研究者らにより開発された手法注4)で、CRISPR法(CRISPR/Cas系を用いたゲノム編集技術の一つ)を改良し、3種類のガイドRNAを用いて、1世代目で極めて高い確率(ほぼ100%)で大量のノックアウトマウスを作製できる。
注4)2016年1月8日理化学研究所プレスリリース「次世代型逆遺伝学による睡眠遺伝子Nr3aの発見」
- 5.ニコチン型受容体、ムスカリン型受容体
アセチルコリンの受容体には2つのファミリーが存在し、アセチルコリンによるニコチン様作用を担うものとムスカリン様作用を担うものに大別される。 - 6.TrkA-TeNT/ChAT-tTRマウス
TeNTを発現するTrkA遺伝子発現細胞のうち、コリンアセチルトランスフェラーゼ(ChAT)発現細胞特異的にtTRを発現するマウス。TrkA-TeNTマウスに対して、ChAT遺伝子のC末端にP2A-tTR-T2A-3x mNeonGreenの発現カセットを挿入することで作製した。作製にあたってはノックインマウス個体高速作製法を用いた注5)。
注5)2017年11月17日理化学研究所プレスリリース「次世代型マウス遺伝学の実現」
- 7.SSS法
共同研究者らにより開発された手法注4)で、呼吸パターンを指標として用いることで、非侵襲かつ高効率に睡眠表現型解析を行う。レム睡眠・ノンレム睡眠の量は測定できないが、外科的な手術を伴わないため、多種類のマウスの睡眠量を高速に測定できる。SSSはSnappy Sleep Stagerの略。 - 8.脳波・筋電図測定
外科的な手術が必須であるものの、レム睡眠・ノンレム睡眠の量が測定可能である。
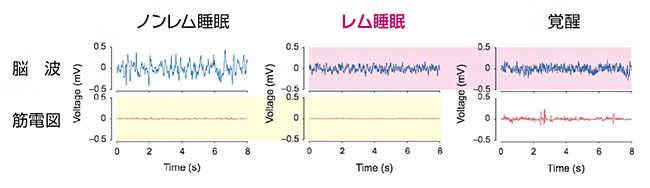
図1 覚醒、レム睡眠、ノンレム睡眠時の脳波と筋電図の波形例注1)
レム睡眠時、脳波は覚醒時と似たパターン(赤色網掛け)を示すが、筋電図はノンレム睡眠時と似たパターン(黄色網掛け)を示す。
注1)Genshiro A. Sunagawa, Hiroyoshi Séi, Shigeki Shimba, Yoshihiro Urade and Hiroki R. Ueda.
"FASTER: an unsupervised fully automated sleep staging method for mice". Genes to Cells, 2013.
2013年4月25日プレスリリース「睡眠状態を全自動で判定できる「FASTER法」を開発」

図2 TrkA遺伝子発現細胞のシナプス放出阻害と睡眠量の関係
TrkA遺伝子発現細胞のシナプス放出を阻害されたマウスは、阻害されていない対照マウスに比べて3時間近く睡眠量が減少した。
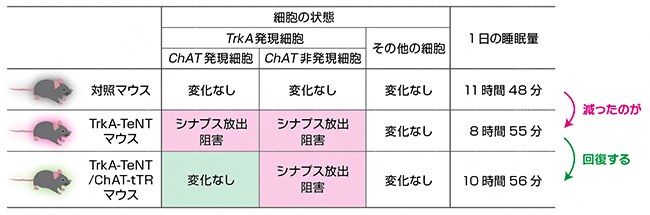
図3 ChAT遺伝子発現細胞のシナプス放出阻害の解除と睡眠量の関係
最下段のTrkA-TeNT/ChAT-tTRマウスは、TrkA遺伝子発現細胞のうちChAT遺伝子発現細胞(コリン作動性神経)でのみシナプス放出を正常化させたマウス。阻害によって減った睡眠量が回復したことから、TrkA/ChAT両遺伝子を共通して発現している細胞が睡眠量制御に重要な役割を果たしていることが分かった。
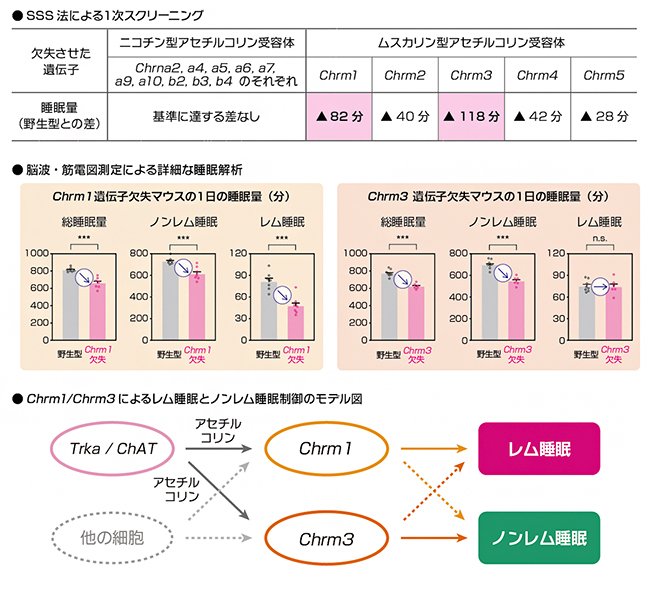
図4 アセチルコリン受容体のChrm1もしくはChrm3遺伝子の欠失と睡眠量の関係
- 上: アセチルコリン受容体を網羅的に欠失させてSSS法により睡眠量を評価した。Chrm1、Chrm3それぞれの遺伝子欠失マウスの睡眠量は野生型に比べて、それぞれ82分、118分少なかった。なお、Chrna3遺伝子欠失マウスは睡眠解析を行う週齢に至る前に死亡したため、解析から除外している。
- 中: 脳波・筋電図測定により、Chrm1遺伝子欠失マウスはレム睡眠とノンレム睡眠の両方が減少し(それぞれ約34分と117分短縮)、Chrm3遺伝子欠失マウスはノンレム睡眠のみが著しく減少した(約153分)ことが分かった。
- 下: レム睡眠とノンレム睡眠に関わる遺伝子のまとめ。実線は本研究で確認できた制御関係、破線は今後の研究で解明される可能性のある制御関係を示す。本研究から、Chrm1遺伝子はレム睡眠、Chrm3遺伝子はノンレム睡眠を主に制御すると考えられる。
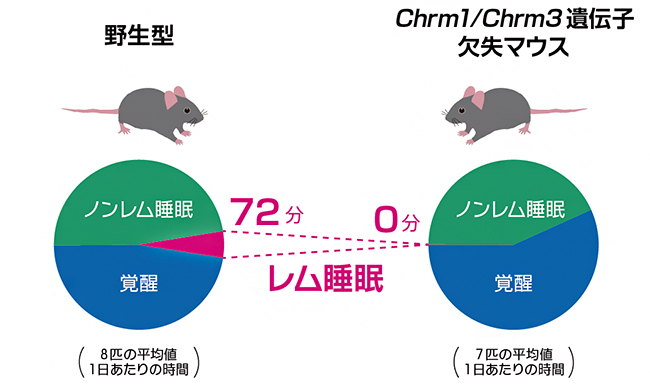
図5 野生型とChrm1/Chrm3遺伝子欠失マウスの睡眠量の比較
Chrm1とChrm3の両遺伝子欠失マウスの睡眠量を評価したところ、レム睡眠がほとんど検出されなかった。
