生命機能科学研究センター 生体分子動的構造研究チーム
チームリーダー 嶋田 一夫(Ph.D.)
研究概要

膜タンパク質は生体内において重要な役割を果たすとともに最大の創薬標的タンパク質です。X 線結晶構造解析などはその立体構造解析に大きく貢献してきましたが、得られた立体構造は基本的に静的スナップショットであり、膜タンパク質が機能している状態の動的構造や分子間相互作用を必ずしも反映していません。核磁気共鳴法(NMR)はin situでのタンパク質の動的構造情報を得ることができる分光法です。そこで、本研究チームでは生物学的に重要な生体分子を対象として、NMR を用いてその機能発現の構造基盤を解明します。
研究主分野
- 医歯薬学
研究関連分野
- 総合生物
- 生物学
- 物理系薬学
- 構造生物化学
- 生物物理学
キーワード
- 核磁気共鳴法
- 生体分子
- 膜タンパク質
- 動的構造
- 構造平衡
主要論文
「*」は、理研外のみでの成果です。
- 1.Shunsuke Imai, Hiroshi Suzuki, Yoshinori Fujiyoshi, Ichio Shimada.:
"Dynamically regulated two-site interaction of viral RNA to capture host translation initiation factor"
Nature communications 14:4977 (2023). doi: 10.1038/s41467-023-40582-6 - 2.Yutaro Shiraishi, Ichio Shimada.:
"NMR Characterization of the Papain-like Protease from SARS-CoV-2 Identifies the Conformational Heterogeneity in Its Inhibitor-Binding Site"
Journal of the American Chemical Society 145:16669-16677 (2023). doi: 10.1021/jacs.3c04115 - 3.Kaneko S, Imai S, Asao N, Kofuku Y, Ueda T, Shimada I.:
"Activation mechanism of the μ-opioid receptor by an allosteric modulator"
Proc Natl Acad Sci U S A. 119(16), e2121918119. (2022) doi: 10.1073/pnas.2121918119. - 4.Shiraishi Y, Kofuku Y, Ueda T, Pandey S, Dwivedi-Agnihotri H, Shukla AK, Shimada I.:
"Biphasic activation of β-arrestin 1 upon interaction with a GPCR revealed by methyl-TROSY NMR"
Nature Communnications 2(1), 7158. (2021) doi: 10.1038/s41467-021-27482-3. - 5.Iwahashi Y, Toyama Y, Imai S, Itoh H, Osawa M, Inoue M, Shimada I.:
"Conformational equilibrium shift underlies altered K+ channel gating as revealed by NMR"
Nature Communications 11, 5168 (2020) doi: 10.1038/s41467-020-19005-3 - 6.Mizukoshi Y, Takeuchi K, Tokunaga Y, Matsuo H, Imai M, Fujisaki M, Kamoshida H, Takizawa T, Hanzawa H, Shimada I.:
"Targeting the cryptic sites: NMR-based strategy to improve protein druggability by controlling the conformational equilibrium"
Science Advances 6(40), eabd0480 (2020) doi: 10.1126/sciadv.abd0480 - 7.* Mizumura T, Kondo K, Kurita M, Kofuku Y, Natsume M, Imai S, Shiraishi Y, Ueda T, and Shimada I*.:
"Activation of adenosine A2A receptor by lipids from docosahexaenoic acid revealed by NMR"
Sci. Adv. (2020) doi: 10.1126/sciadv.eaay8544 - 8.* Imai S, Yokomizo T, Kofuku Y, Shiraishi Y, Ueda T, and Shimada I*.:
"Structural equilibrium underlying ligand -dependent activation of β2 -adreno receptor."
Nat. Chem. Bio. (2020) doi: 10.1038/s41589-019-0457-5. - 9.* Kano H, Toyama Y, Imai S, Iwahashi Y, Mase Y, Yokogawa M, Osawa M, and Shimada I*.:
"Structural mechanism underlying G protein family-specific regulation of G protein-gated inwardly rectifying potassium channel"
Nat. Commun. 10(1),2008. (2019) - 10.* Shimada I*, Ueda T, Kofuku Y, Matthew T. Eddy, and Kurt Wuthrich*.:
"GPCR drug discovery: integrating solution NMR data with crystal and cryo-EM structures."
Nat. Rev. Drug Discov. 18(1), 59-82 (2019)
研究成果(プレスリリース)
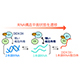
2024年4月25日
RNAの高次構造をほどく分子機構
2023年8月28日
脳心筋炎ウイルスはRNAの動的構造平衡を利用して増える
2023年7月31日
新型コロナウイルスパパイン様プロテアーゼの構造柔軟性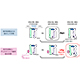
2022年4月12日
アロステリック薬剤はタンパク質の構造平衡を変化させる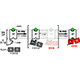
2021年12月13日
シグナル伝達複合体の2段階活性化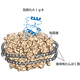
2021年7月9日
オートファゴソームを効率よく作る仕組みを発見
2021年2月16日
環状ペプチドは立体構造を変えて細胞に入る
2020年11月13日
細胞内ゲートを閉ざす構造平衡の崩れ
関連リンク
メンバーリスト
主宰者
- 嶋田 一夫
- チームリーダー
メンバー
- 今井 駿輔
- 上級研究員
- 林 文晶
- 上級研究員
- 白石 勇太郎
- 研究員
- 外山 侑樹
- 研究員
- 田村 さと子
- テクニカルスタッフⅠ
- 金子 舜
- 研修生
お問い合わせ先
〒230-0045 神奈川県横浜市鶴見区末広町1-7-22 中央研究棟C520
Email: ichio.shimada [at] riken.jp
※[at]は@に置き換えてください。
