要旨
理化学研究所(理研)生命システム研究センター合成生物学研究グループの上田泰己グループディレクターと洲﨑悦生客員研究員、大阪大学大学院医学系研究科の森井英一教授と野島聡助教らの共同研究チームは、組織透明化/3次元イメージング技術「CUBIC[1]」が病理組織診断に応用できることを実証しました。
病理組織診断は、腫瘍性疾患の悪性度・分化度・転移の有無や、炎症性疾患・自己免疫性疾患[2]の炎症・線維化の程度といった病的所見を組織形態学的に診断する医療行為のことで、患者への治療方針決定の根幹に関わる重要なものです。病理組織診断は、薄切した病変組織を染色し作製したスライドガラスを、訓練を積んだ病理診断医が顕微鏡で観察することによって行われます。しかし、現在用いられている標準的な方法には、肉眼で見て最も疑わしかった部位を通る断面だけを薄切し観察すること、平面上の二次元的な組織しか評価できないことといった技術的な限界がありました。
共同研究チームは今回、上田グループディレクターらが2014年に発表した組織透明化/3次元イメージング技術である「CUBIC」注1、2)の病理組織診断法における有用性を詳しく検討しました。その結果、①この技術により病理組織検体における正常および病的な組織所見を3次元的かつ明瞭に描出できること、②この技術が従来のスライドガラス作製法と両立可能なこと、③病院に長期保管されているパラフィンに包埋された状態の検体にも応用できることを示しました。さらにこの技術を、病変を発見するための実際の臨床病理検査におけるスクリーニング系に応用し、検査の感度を向上させることにも成功しました。
これらの技術を基盤として、3次元的な病理組織診断法についてさらに発展させることにより、今後、次世代の臨床病理診断における新たなスタンダードになるものと期待できます。
本研究成果は、英国のオンライン科学雑誌『Scientific Reports』(8月24日付け:日本時間8月24日)に掲載されました。
本研究は、日本医療研究開発機構(AMED)「革新的技術による脳機能ネットワークの全容解明プロジェクト」および「革新的バイオ医薬品創出基盤技術開発事業」、日本学術振興会科学研究費補助金、自然科学研究機構新分野創成センター「ブレインサイエンス研究分野プロジェクト」、民間研究助成(公益財団法人アステラス病態代謝研究会、公益財団法人かなえ医薬振興財団、公益財団法人千里ライフサイエンス振興財団、公益財団法人中島記念国際交流財団、公益財団法人武田科学振興財団、公益財団法人日本応用酵素協会)などの支援を受けて行われました。
注1)2014年4月18日プレスリリース「成体の脳を透明化し1細胞解像度で観察する新技術を開発」
注2)2014年11月7日プレスリリース「マウスを丸ごと透明化し1細胞解像度で観察する新技術」
背景
病理組織診断は、腫瘍性疾患の悪性度・分化度・転移の有無や、炎症性疾患・自己免疫性疾患の炎症・線維化の程度といった病的所見を組織形態学的に診断する医療行為のことで、患者への治療方針決定の根幹に関わる重要な診断技術です。病理組織診断は、薄切した病変組織をヘマトキシリン・エオシン染色(HE染色)で染色し作製したスライドガラスを、訓練を積んだ病理診断医が顕微鏡で観察することによって行われます。
しかし、その標本作製の基本的な手法には、19世紀にHE染色が開発されて以来、大きな改変は加えられていませんでした。また、この古典的な方法には、肉眼で見て最も疑わしかった部位を通る断面だけを薄切し観察すること、平面上の二次元的な組織しか評価できないこと、といった技術的な限界がありました。そのため、病変組織を3次元的かつ包括的に評価できる、新たな病理組織診断手法が求められていました。
研究手法と成果
共同研究チームは、上田グループディレクターらが2014年に開発し、主に基礎生物学領域における全脳・全臓器イメージングに用いられている組織透明化/3次元的イメージング技術「CUBIC」について、ヒト病理組織診断学における実用性を、詳細に検討しました。
まず、2014年に報告した組成のCUBIC試薬では、肺とリンパ組織が特に良好に透明化できることが分かりました。また、一度透明化した臓器片でも、その後に透明化試薬をよく洗浄することで、従来のHE染色のスライドガラスを問題なく作製することができました。これらの結果から、透明化処理による組織の変性はごくわずかであり、透明化した組織に対して従来の病理組織学的評価が十分可能なことが分かりました(図1)。これは、CUBICを標準的な病理組織診断法へ拡張的に組み合わせることができることを示しています。
また、ヒト病理組織検体にCUBICを応用し、3次元観察が可能な蛍光顕微鏡(共焦点顕微鏡[3]やシート照明顕微鏡[4])で撮像することにより、肺胞間質[5]を網目状に走行する血管やリンパ濾胞といった正常組織構築、血管壁におけるアミロイド[6]の沈着といった病的所見が、3次元的かつ明瞭に描出できることを示しました(図2)。
さらに、実際の臨床病理診断においては、薄切後の残った病変部組織はパラフィンブロックに包埋された状態で保存されます。よって、パラフィンブロックに包埋された病理組織検体についても、CUBICを適応できるか評価しました。その結果、適切な脱パラフィン操作(加熱および有機溶媒処理)を行うことで、CUBICによる透明化/3次元的イメージングが可能であることが分かりました(図3)。パラフィンブロック由来の組織を3次元的にイメージングできるということは、全国の病院病理部に保管されている、稀少疾患由来のものを含めたほぼ全ての病理組織検体について、集学的かつ包括的な3次元的評価が可能であることを意味します。
最後に、実際の臨床病理検査における有用性を検討するために、CUBICを用いた3次元イメージングによる評価系を、大腸直腸がんのリンパ節転移を同定するスクリーニング系に応用しました。通常の手法では、所属リンパ節へのがん転移巣が肉眼で明らかにならない場合、最大割面で評価面を作製し、この断面の薄切切片をスライドガラスにして顕微鏡で評価します。しかしこの方法では、肉眼では同定できない微小がん転移巣を完全に捉えることができませんでした。
そこで、CUBICによる3次元イメージングを用いて、このような微小がん転移巣がリンパ節内にあるかどうかを評価しました。疑わしい結節状シグナルが見られた場合には、この面を通る割面で薄切切片を作製し評価するという2段階検査を行いました(図4上)。その結果、従来法とCUBICを用いたスクリーニングを併用することで、新たに微小がん転移巣が同定され陽性と診断できた症例が出ました(図4下)。そして最終的に、本研究での検査成績では、検査感度を約85%から100%まで向上させることができました(表1)。
今後の期待
本研究は、これまで実験動物を用いた基礎生物学分野で主に使用されてきたCUBICを、本格的にヒト病理組織診断に応用することに成功したという意味で、臨床応用学的に大きな意義のある成果だと考えられます。また、透明化することでの試料へのダメージはほとんどなく、現在標準的な病理組織診断法へ拡張的に組み合わせることができることも大きな利点です。
今後、透明化試薬やプロトコール、顕微鏡機器の性能の改良に伴い3次元イメージング技術が標準化されることで、本研究を基盤とした評価法が病理診断の新たなスタンダードになるものと期待できます。
原論文情報
- Satoshi Nojima, Etsuo A. Susaki, Kyotaro Yoshida, Hiroyoshi Takemoto, Naoto Tsujimura, Shohei Iijima, Ko Takachi, Yujiro Nakahara, Shinichiro Tahara, Kenji Ohshima, Masako Kurashige, Yumiko Hori, Naoki Wada, Jun-ichiro Ikeda, Atsushi Kumanogoh, Eiichi Morii, Hiroki R. Ueda, "CUBIC pathology: three-dimensional imaging for pathological diagnosis.", Scientific Reports, doi: 10.1038/s41598-017-09117-0
発表者
理化学研究所
生命システム研究センター 細胞デザインコア 合成生物学研究グループ
グループディレクター 上田 泰己(うえだ ひろき)
客員研究員 洲﨑 悦生(すさき えつお)
 上田グループディレクター
上田グループディレクター
 洲﨑客員研究員
洲﨑客員研究員
 森井教授
森井教授
 野島助教
野島助教
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
大阪大学 大学院医学系研究科 広報室
Tel: 06-6879-3388 / Fax: 06-6879-3399
kouhousitsu [at] office.med.osaka-u.ac.jp
産業利用に関するお問い合わせ
理化学研究所 産業連携本部 連携推進部
お問い合わせフォーム
補足説明
- 1.CUBIC
臓器透明化と3次元イメージングのための化合物の混合溶液とコンピュータを用いた画像解析。CUBICの実現のために、研究グループは理研が2011年に開発した透明化試薬「Sca le(スケール)」をもとに、新しく構築した化合物スクリーニング系を用いて、40種類の化合物から最適な組成を検討した。その結果、サンプルを試薬に浸すだけの効率的で再現性のよい方法で、複数のサンプルを同等な条件で高度に透明化することが可能となり、1細胞解像度の全臓器蛍光イメージングと情報科学的解析によるサンプル間のシグナル比較法が実現した。CUBICは、Clear, Unobstructed Brain/Body Imaging Cocktails and Computational analysisの略。 - 2.自己免疫性疾患
何らかの免疫異常によって自分の身体を構成する物質を異物のように認識し、自己抗体や自己に反応するリンパ球を作り、自分の組織を攻撃する疾患。代表的なものに関節リウマチなどあるが、根本的な治療法は見つかっていない。 - 3.共焦点顕微鏡
小さく絞ったレーザー光を走査して画像を取得するレーザー走査型蛍光顕微鏡の1種。蛍光シグナルを検出する際、集光面にピンホールを設置して焦点面由来の光だけを検出するため、深さ方向にもレーザー走査することで3次元的な蛍光像を得ることができる。 - 4.シート照明顕微鏡
レーザー光をシート上に広げてサンプルの横から照射し上から撮影することで、サンプル内のある平面を1回で撮影することができる顕微鏡。シートまたはサンプルを、Z方向に動かして平面を重ねることで、高速に3次元画像を取得することができる。ただし、サンプルが高度に透明でなければ使用できない。 - 5.肺胞間質
肺の呼吸単位である肺胞において、呼吸上皮を支える線維などからなる硬い壁組織のこと。この中を多数の血管が走行し、効率的なガス交換を可能にしている。 - 6.アミロイド
ある特徴的な構造を持つ水に溶けない線維状のタンパク質のことで、これが臓器に沈着する疾患がアミロイド―シスである。
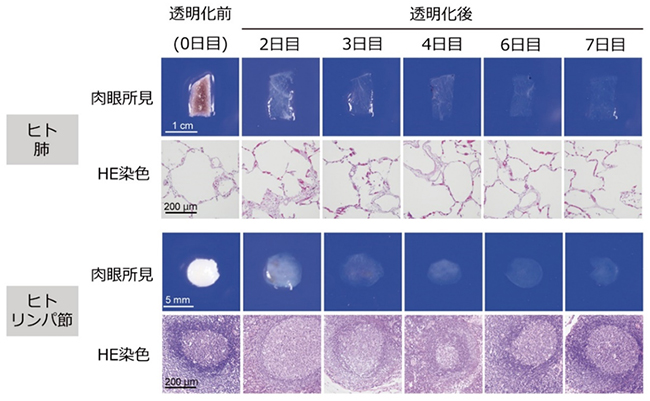
図1 ヒト臓器片の透明化
CUBIC試薬でヒトの肺、リンパ節の臓器片を透明化処理した。3日目~4日目には、ほぼ完全に透明化したことが分かる。一度透明化したこれらの臓器片をリン酸緩衝生理食塩水(PBS)でよく洗ったところ、従来の標準的病理診断用のスライドガラス作製法であるパラフィン包埋、薄切、HE染色のいずれの手技についても、問題なく行うことができた。また、できあがったスライドガラスを観察したところ、組織の変性はごくわずかで、病理組織診断に十分耐える組織像であった。
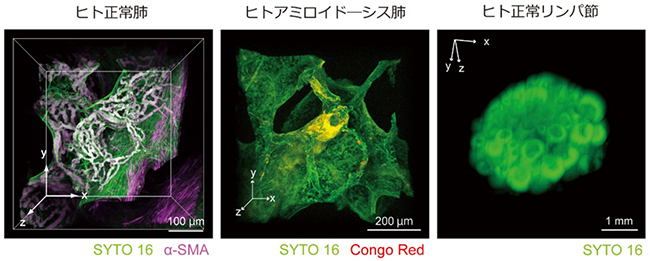
図2 ヒト病理組織検体の3次元イメージング
それぞれ、共焦点顕微鏡で撮像した正常肺組織(左;核をSYTO16という緑色蛍光色素、血管平滑筋を赤紫色の蛍光色素でラベルした抗α-SMA抗体で染色)、アミロイド―シス患者由来の肺組織(中央;核をSYTO16緑色蛍光色素で染色、血管壁に沈着するアミロイドをコンゴーレッド染色にて赤色に染色)、およびシート照明顕微鏡で撮像した正常リンパ節組織(右;核をSYTO16緑色蛍光色素で染色)。各種組成や病的所見が、3次元的かつ明瞭に描出できていることが分かる。
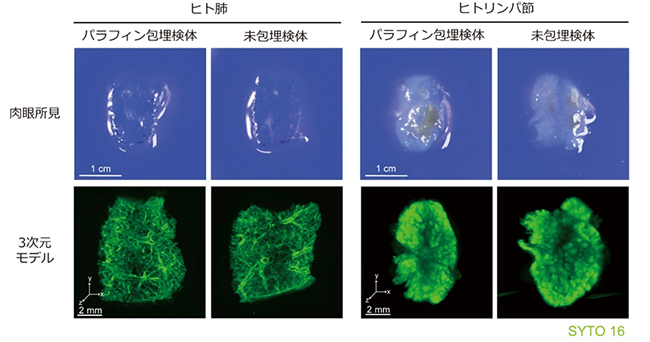
図3 パラフィンブロック由来組織の透明化および3次元イメージング
ヒト肺の臓器片およびリンパ節検体について、それらを半割し、一方をパラフィンブロックに包埋、もう一方は未包埋の状態で静置した。パラフィンブロックに包埋した組織検体を加熱および有機溶媒処理にて脱パラフィンし、未包埋検体と共に透明化/3次元イメージング(核をSYTO16緑色蛍光色素で染色、シート照明顕微鏡にて撮像)にて評価した。パラフィンブロック由来組織、未包埋検体のどちらも、同程度に良好に透明化/3次元イメージングができることが分かった。
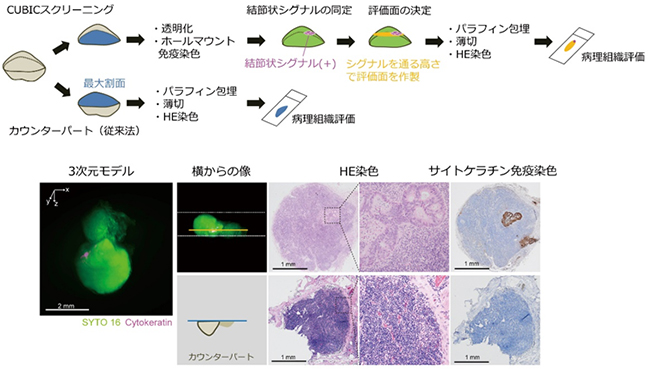
図4 CUBICを応用した大腸直腸がんリンパ節転移のスクリーニング系
上)病院病理部での診断において、肉眼的に腫瘍結節(腫瘍の小さな塊)が明らかでなく、最大割面で分割したリンパ節について、半割検体(カウンターパート)の残りのもう片方の半割検体をCUBICスクリーニングに応用した。抗サイトケラチン抗体を用いてホールマウント免疫染色を行い、シート照明顕微鏡で3次元的に観察し、転移巣が疑われる結節状のシグナルを検索。シグナルが認められた場合には、その部位を通る割面を入れ、これを通る面を評価できるようにスライドガラスを作製、最終的に光学顕微鏡を用いた病理組織診断法で評価した。
下)従来法(カウンターパート)では陰性と診断されたが、CUBICスクリーニングを併用した場合に転移巣が新たに同定され、陽性と診断された症例のうちの一つ。右上の画像で、サイトケラチン免疫染色で茶色に染まった部分が微小がん転移巣である。

表1 CUBICを応用したリンパ節転移のスクリーニング系の検査成績
リンパ節転移スクリーニング系を用いて、74症例のリンパ節について評価を行った検査成績。従来法で陽性だった23例は、CUBICスクリーニング併用でも陽性を示した。従来法で陰性だった51例のうち4例は、従来法とCUBICスクリーニングの併用で初めて陽性を捉えることができた。したがって、CUBICスクリーニング併用によって、陽性が23例から27例まで増加したことから、検査の感度は、85.2%(23/27)→100%(27/27)に向上したことになる。
