2010年8月23日
独立行政法人 理化学研究所
国立大学法人 東京大学大学院理学系研究科
核酸のように振る舞うタンパク質を明らかに
-翻訳因子EF-Pが転移RNAと同じ反応でアミノ酸を受け取ることを発見-
ポイント
- タンパク質が、まったく異なる物質である転移RNAと、形から反応まで酷似するように進化
- EF-Pが、転移RNAに働く酵素を先祖にもつGenXからアミノ酸を受け取る様子を3Dで解明
- 細菌だけに存在するGenXは副作用のない新規抗菌薬開発の有望なターゲットに
要旨
独立行政法人理化学研究所(野依良治理事長)と国立大学法人東京大学(濱田純一総長)は、遺伝情報の翻訳過程で必須の役割を果たす翻訳因子EF-Pと、機能不明であった酵素GenXとの複合体の立体構造解析に成功し、EF-PがGenXによりアミノ酸を受け取ることを発見しました。これにより、タンパク質であるEF-Pが、核酸である転移RNA(tRNA)※1と、形だけでなく、その反応までもが酷似していることを初めて明らかにすることができました。また、GenXによるEF-Pへのアミノ酸の受け渡しが、大腸菌など真正細菌※2の増殖に必須であることも見いだしました。これは、理研生命分子システム基盤研究領域の横山茂之領域長(東京大学大学院理学系研究科 構造生物学社会連携講座兼任教授)、柳沢達男研究員、澄田智美特別研究員らの研究チームによる成果です。
生物の遺伝情報から正しいタンパク質を作るためには、遺伝暗号に従って必要なアミノ酸と結合したtRNAを選び出し、正確にアミノ酸をつなげていく必要があります。この過程は「翻訳」と呼ばれ、さまざまなアミノアシルtRNA合成酵素(aaRS)※3や翻訳因子と呼ばれるタンパク質群が機能しています。研究チームはこれまでに、翻訳開始などで働く翻訳因子EF-Pの形がtRNAとよく似ていることなどを明らかにしてきました。今回、EF-PとGenX(aaRSと遠縁にあたる機能不明タンパク質)との複合体の結晶化と立体構造の解明に成功し、その立体構造がtRNA・aaRS複合体の構造と酷似していることを見いだしました。この発見に基づき、EF-PはtRNAと酷似した反応によってアミノ酸を受け取ることを解明しました。核酸とタンパク質という、まったく異なる分子でありながら、その形とともに、反応までも酷似していることを解明した例は初めてで、これは、異なる生物が進化して同じような形態と生活様式を獲得する現象「収斂(しゅうれん)進化」を類推させます。また、GenXによるEF-Pへのアミノ酸の受け渡しが、大腸菌の増殖に必須であることも見いだしました。GenXは、大腸菌やサルモネラ菌など真正細菌だけに存在し、ヒトなどの真核生物※2は持っていないことなどから、GenXが病原菌や薬剤耐性菌に対する副作用の無い新規抗菌薬開発の有望なターゲットになると期待されます。
本研究成果は「ターゲットタンパク研究プログラム」の一環として行われたもので、米国の科学雑誌「Nature Structural & Molecular Biology」オンライン版(8月22日付け、日本時間8月23日)に掲載されます。
背景
私たちの体を構成し、生命活動を主に制御しているのは、20種類のアミノ酸の組み合わせからなるタンパク質です。これらタンパク質の基となる遺伝情報は、DNAの配列中に遺伝暗号という形で記述されています。DNAの遺伝暗号は、まず伝令RNA(mRNA)へと「転写」され、続いてタンパク質合成工場であるリボソーム上で、決められた順番に正しくアミノ酸がつなげられてタンパク質が作られていきます。この過程を「翻訳」と呼びます。mRNA上の遺伝暗号に従って指定されたアミノ酸を運び込むのが、転移RNA(tRNA)と呼ばれる核酸分子です。tRNAは、20種類のアミノ酸の中から自分と対応する正しいアミノ酸を受け取る(アミノアシル化※3される)という必須の役割を担っており、その反応を触媒するのがアミノアシルtRNA合成酵素(aaRS)です。アミノ酸を受け取ったtRNAはリボソームに運ばれて、タンパク質合成にアミノ酸を提供します。この際、リボソームはさまざまな翻訳因子と呼ばれるタンパク質群の助けを借りてアミノ酸を効率的につなげていきます。その中で、最近注目を集めるようになった翻訳因子がEF-Pです。EF-Pはリボソームに結合することが知られており、研究チームによって、EF-Pの三次元構造は、tRNAとよく似たL型の構造であることが判明したものの(2004年6月22日プレス発表)、その詳細な機能はよく分かっていませんでした。
一方、近年になってaaRSによく似たタンパク質をコードする遺伝子が、生物のゲノム上に数多く存在することが知られるようになりました。これらのタンパク質は、進化的にaaRSと近縁でありながら、アミノ酸をtRNAに受け渡す活性を持たず、機能についてはほとんど分かっていません。研究対象にしたGenXもその1つで、tRNAにリシンというアミノ酸を受け渡す機能を持つaaRSと遠縁にあたると考えられますが、その機能は不明でした。
研究手法と成果
本研究では、翻訳因子EF-Pと、アミノ酸(リシン)をtRNAに受け渡すaaRS(LysRS)によく似た大腸菌由来の合成酵素GenXが結合することを見いだしました。EF-PとGenXとの複合体の結晶ならびにGenX単体の結晶を作製し、EF-P・GenX複合体結晶には理研の大型放射光施設SPring-8※4のビームラインBL41XUを用い、GenX単体結晶には大学共同利用機関法人高エネルギー加速器研究機構(KEK)のフォトン・ファクトリー(Photon Factory)を用いてX線結晶構造解析を行い、それぞれ2.5Å(オングストローム:1×10-10メートル)、1.9Åの分解能※5で立体構造を決定しました。その結果、GenX単体の構造はLysRSの触媒ドメイン※6と(図1)、EF-P・GenX複合体の構造はtRNA・aaRS複合体の構造と(図2)それぞれ酷似しており、EF-PはGenXからアミノ酸を受け取る機能があることが示唆されました。EF-Pがリシンを受け取る位置(Lys34)は、tRNAがアミノ酸を受け取る位置(A76)に相当しており、EF-Pがリシンを受け取る反応は、tRNAがアミノ酸を受け取る反応と酷似していました。さらに、生化学的な実験によって、実際にEF-PがGenXからリシンを受け取ることを証明しました。従って、EF-Pはリシンを受け取った形でリボソームに結合すると考えられ、その点でもtRNAと類似しています。
また、EF-P遺伝子を欠損させた大腸菌株やGenX遺伝子を欠損させた大腸菌株を用いて、細胞内でのEF-Pの修飾の役割を詳細に調べた結果、EF-Pのリシンの受け取りが大腸菌の増殖に必須であることも明らかとなりました(図3)。
今後の展望
本研究により、tRNAと形が似ている翻訳因子EF-Pは、アミノ酸を受け取る反応においてもtRNAと酷似していることが判明しました。近年、翻訳因子だけでなくさまざまなタンパク質が核酸の形と酷似しているという現象が報告されていますが、その形とともに反応までも酷似したことを解明した例は今までにないものです。この成果は、類縁関係の遠いモグラとケラの前足が同じような形と機能を有する現象(収斂進化)を類推させることから、生物の個体レベルだけでなくタンパク質などの分子レベルでも、生命現象において同様の進化が起こっていたと考えられ、遺伝暗号翻訳システムの分子機構を通じた生物の進化を知る上でも学術的に重要です。
また、GenXは、大腸菌、サルモネラ菌、腸炎ビブリオ菌、コレラ菌など真正細菌だけに存在し、ヒトなどの真核生物には存在しません。従って、GenXを特異的に阻害する低分子化合物は、感染症を引き起こす病原菌や薬剤耐性菌に対して、副作用の無い有効な抗菌薬となる可能性があります。このように、EF-Pの翻訳後修飾にかかわる構造・機能の解明は、創薬開発にも大きく貢献することが期待されます。
発表者
理化学研究所
生命分子システム基盤研究領域
領域長 横山 茂之(よこやま しげゆき)
Tel: 045-503-9196 / Fax: 045-503-9195
お問い合わせ先
横浜研究推進部 企画課Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel:048-467-9272 / Fax:048-462-4715
国立大学法人東京大学大学院理学系研究科・理学部
広報室 横山 広美(よこやま ひろみ)
Tel: 03-5841-7585 / Fax: 03-5841-1035
補足説明
- 1.転移RNA(tRNA)
転移リボ核酸の略号。翻訳の過程でmRNAの塩基配列であるアデニン(A)、グアニン(G)、シトシン(C)、ウラシル(U)は、3つが組(コドン)となって1つのアミノ酸がコードされている。DNAの塩基配列であるアデニン(A)、グアニン(G)、シトシン(C)、チミン(T) の情報とアミノ酸を対応付けるアダプター分子がtRNAである。tRNAはそれぞれの対応するアミノ酸を末端のA76リボースに結合したのちリボソームに運ばれる。mRNA上のコドンに従って運び込まれたアミノ酸がリボソーム上で結合しタンパク質が合成される。 - 2.真正細菌、真核生物
すべての生物は真核生物、古細菌、真正細菌の3つのグループに分類される。真核生物の特徴は細胞内に核を持ち、細胞のそれ以外の部分からは膜で仕切られていることである。核の中には遺伝情報が書き込まれたDNAが収められている。真正細菌とはいわゆる細菌(バクテリア)のことで大腸菌、サルモネラ菌、腸炎ビブリオ菌、コレラ菌、赤痢菌などを含む。真核生物と比較すると核を持たない非常に簡単な構造で、地球上のあらゆる環境に生息しており、その代謝系は多種多様である。 - 3.アミノアシルtRNA合成酵素(aaRS)、アミノアシル化
タンパク質を構成するアミノ酸は主に20種類存在する。20種類のアミノ酸のそれぞれに対してアミノアシルtRNA合成酵素が20種類存在し(アスパラギン酸に対応するAspRS、リシンに対応するLysRSなど)、ATPのエネルギーを利用して特定のアミノ酸を活性化したのち特定のtRNAのCCA末端に付加する(アミノアシル化)。
aaRS + アミノ酸+ATP + tRNA → aaRS・(アミノアシルAMP) + tRNA →アミノアシルtRNA + aaRS - 4.大型放射光施設SPring-8
兵庫県の播磨科学公園都市にある世界最高の放射光を生み出す理化学研究所の施設。SPring-8の名前はSuper Photon ring 8GeVに由来する。放射光とは、電子を光とほぼ等しい速度まで加速し、電磁石によって進行方向を曲げた時に発生する、絞られた強力な電磁波のこと。SPring-8では、この放射光を用いて、ナノテクノロジー、バイオテクノロジーや産業利用まで幅広い研究を行っている。 - 5.分解能
Å(オングストローム:1×10-10メートル)の単位を用いて表し、この数字が小さいほど分解能が高く、より精度の高い高解像度の構造であることを示す。 - 6.ドメイン
αへリックス、βシートなどの二次構造がいくつか組み合わさったモチーフが一体となり局所的にコンパクトな半独立のユニットを作ったもの。
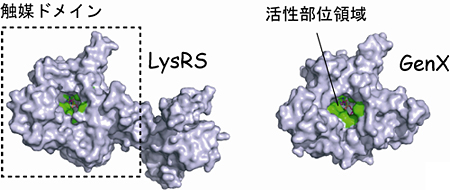
図1 LysRSとGenXの構造
LysRSとGenXとで保存されているアミノ酸残基群を緑で示した。LysRSの触媒ドメインとGenXの構造はよく似ている。
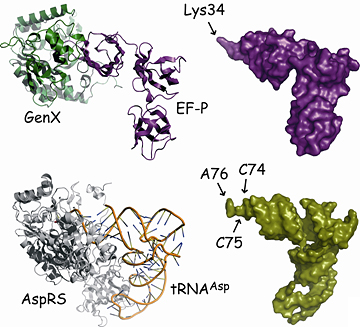
図2 EF-P・GenX複合体とtRNA・aaRS複合体構造の比較
例としてアスパラギン酸tRNAとアスパルチルtRNA合成酵素の複合体(tRNAAsp・AspRS)を示す。EF-P・GenX複合体(左上)とtRNA・aaRS複合体(左下)の構造はよく似ている。EF-PのLys34は、tRNAにアミノ酸が結合するCCA末端(A76)の位置に相当する。
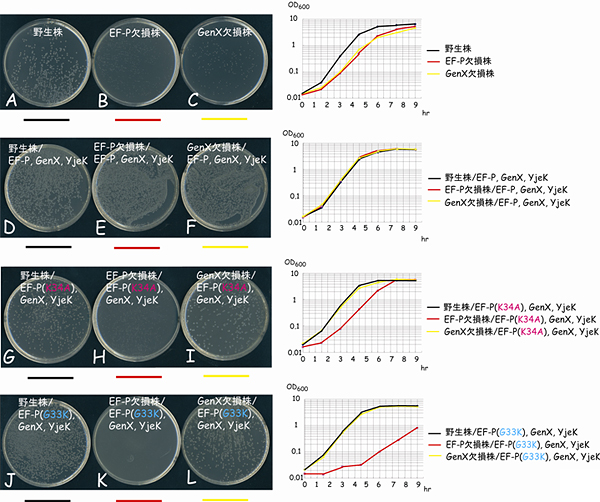
図3 EF-Pのリシル化(リシンの受け取り)が大腸菌の増殖に及ぼす影響
大腸菌野生株、EF-P欠損株、GenX欠損株の寒天培地での増殖(左)と液体培地での生長曲線(右)。大腸菌の野生株(A)からEF-Pの遺伝子、またはGenXの遺伝子を欠損させると増殖は悪くなるが(B, C)、野生型EF-P、GenX、およびYjeK(研究チームが発見したGenXによるEF-Pのリシル化を促進するタンパク質)を外から足すことで増殖は回復する(E, F)。リシルを受け取ることができない変異型EF-P(K34A)とEF-P(G33K)を足しても、EF-P欠損株の増殖を回復させることができないので(H, K)、細胞内のEF-Pは、リシルを受け取った形で機能する。従って、EF-Pのリシル化が大腸菌の増殖に必須であることが判明した。
