2012年5月28日
独立行政法人 理化学研究所
独立行政法人 国立がん研究センター
独立行政法人 医薬基盤研究所
肝臓がん27例の全ゲノムを解読
-多様なゲノム変異は肝炎ウイルスや飲酒などとも関連-
ポイント
- 27症例中16例(約60%)で、クロマチン制御遺伝子の異常が見つかる
- TERT遺伝子近くへのB型肝炎ウイルスゲノム挿入が、肝臓がんの原因の可能性
- クロマチン制御機構異常を標的とした新しい治療法や予防法の開発に期待
要旨
理化学研究所(野依良治理事長)と国立がん研究センター(堀田知光理事長)は、27例の肝臓がんの全ゲノムシーケンス解析を行い、肝臓がんの包括的ゲノム変異を解析しました。これは、理研ゲノム医科学研究センター(久保充明センター長代行)バイオマーカー探索・開発チームの中川英刀チームリーダーと、国立がん研究センターがんゲノミクス研究分野の柴田龍弘分野長らとの共同研究グループによる成果で、理研と医薬基盤研究所(山西弘一理事長)の資金的支援の下、国際がんゲノムコンソーシアム(ICGC)※1のプロジェクトの一環で行われました。
日本では、年間約4万人が肝臓がんと診断され、3万人以上が亡くなっています(出典:2011年国立がん研究センター がん対策情報センター調べ)。特に、日本や中国を含むアジア地域とアフリカ地域で発症頻度が高く、世界全体の部位別がん死亡率では第3位に挙げられています。主な原因は肝炎ウイルスの持続感染です。B型肝炎ウイルス※2やC型肝炎ウイルス※2の感染に伴う慢性肝炎の症状から、肝硬変を経て高頻度に発生する傾向があります。治療法にはさまざまな手法がありますが、その効果は十分ではなく、分子機構の解明による新たな治療法や予防法の開発が強く望まれています。
今回、共同研究グループは、25人27例の肝臓がん(B型肝炎関連11例、C型肝炎関連14例、非ウイルス性2例)の腫瘍のDNAと血液からの正常DNAの全塩基配列(約30億塩基対)を対象に次世代シーケンサー※3で解読し、がん特異的なゲノム変異を網羅的に解析しました。そのデータ総量は約7兆個もの塩基配列情報となり、東京大学医科学研究所ヒトゲノム解析センターのスーパーコンピューターを駆使してデータ解析を行いました。その結果、ゲノム変異の数は、1つの腫瘍あたり平均でポイント変異※4が約11,000カ所、ゲノム構造異常※5が21カ所でした。個々の肝臓がんは非常に多様なゲノム変異を示しましたが、塩基配列の置換パターンに着目し解析すると、肝炎ウイルスや飲酒の習慣など、がんの原因となるものの影響を受けていることが分かりました。
また、27症例中16例(約60%)において、ARID1A、ARID1B、ARID2、MLL、MLL3など、10個のクロマチン制御※6に関わる遺伝子変異が1つ以上起きていることが判明しました。細胞株実験の結果、これらの遺伝子は腫瘍抑制機能を有していることも分かりました。さらに、B型肝炎関連の肝臓がんの場合、染色体末端の構造を維持し、細胞の不死化に重要な働きをしているTERT遺伝子※7の近くに、B型肝炎ウイルスの塩基配列が高い頻度で挿入されていることも分かり、B型肝炎関連の肝臓がんの原因の1つと示唆されました。
今回、約60%の肝臓がんでクロマチン制御機構の異常を認めたことから、今後これを標的とした新たな治療法や予防法の開発が期待でき、さらには、がんのゲノム配列情報に基づいて、がん治療の個別化へ発展する可能性があります。また、今回の解析データは、ICGCのホームページ(英語)で公開しています。
本研究成果は、科学雑誌『Nature Genetics』の掲載に先立ち、オンライン版(5月27日付け:日本時間5月28日)に掲載されます。
背景
肝臓がんは、日本における部位別死亡者数では、男性で3位、女性では6位です。年間約4万人が肝臓がんと診断され、3万人以上が亡くなっています。特に、日本や中国を含むアジアとアフリカで発症頻度が高く、世界全体の部位別がん死亡率では第3位に挙げられています。また最近では、アジアだけでなく欧米でも増加しているがんとして対策が急がれています。主な原因は、肝炎ウイルスの持続感染であり、世界中の肝臓がんの約75%は、B型肝炎ウイルス(HBV)またはC型肝炎ウイルス(HCV)の感染によるものと推定され、慢性肝炎発症から肝硬変を経ると高頻度で肝臓がんが発生します。一方、日本では、肝臓がんの約75%がC型肝炎ウイルス、約20%がB型肝炎ウイルスの持続感染が原因と推定されています(独立行政法人国立国際医療研究センター 肝炎情報センター調べ)。肝炎ウイルスは血液を介して感染し、輸血あるいは血液製剤などの医療行為や注射器の共有などが主な感染原因として挙げられ、社会問題となっていました。肝臓がんは、こうしたウイルス肝炎の終末的な形として発生します。
肝臓がんの治療法には、外科的切除や肝動脈塞栓術など、さまざまな手段があります。2007年米国では、再発性や進行性肝臓がんに対して分子標的薬が使われるようになりました。しかし、その予後は悪く、肝臓がんの分子機構の解明による新たな治療法や予防法の開発が強く望まれています。
近年のDNA解読技術の飛躍的な進歩に伴い、次世代シーケンサーを用いて、さまざまなタイプのがんや病気のゲノム変異を包括的に解析することが可能になってきました。特にがんは、ゲノム変異が蓄積することで発生し進行する“ゲノムの病気”であり、世界中でがんのゲノムシーケンス解析が精力的に行われています。2008年、最大50種類のがんを選定し、そのゲノム変異の全貌解明とカタログ化を目指し、「国際がんゲノムコンソーシアム(ICGC)」が発足しました。日本では、理研と医薬基盤研究所の資金的支援の下、理研と国立がん研究センターなどの研究チームが、主に肝炎ウイルス関連の肝臓がんの全ゲノムシーケンス解析を進めています。
研究手法と成果
共同研究グループは、5つの肝臓がんの専門医療機関※8と共同で、25人の患者から27例の肝臓がん(B型肝炎関連11例、C型肝炎関連14例、非ウイルス性2例)の検体を収集し、その腫瘍のDNAおよび血液からの正常DNAについて、全ゲノム(約30億塩基対)シーケンス解析を行いました。これは、がん特異的なゲノム変異を網羅的に検索する手法です。そのデータ総量は約7兆個もの配列情報となり、東京大学医科学研究所ヒトゲノム解析センターのスーパーコンピューターを駆使してデータ解析しました。その結果、ゲノム変異の数は、1つの腫瘍あたり平均でポイント変異が約11,000カ所、ゲノム構造異常が21カ所ありました。
27例の腫瘍のうち4例は同じ患者(2例の腫瘍を持つ2人の患者)の肝臓から別々に発生した多中心性腫瘍※9でした。それら4例の肝臓がんの全塩基配列を比較した結果、全く異なるゲノム変異であることが分かりました。これは、同じ肝臓から発生したがんにもかかわらず、異なるゲノム変異を経て発生したものと推定されます。一方で、塩基の置換パターンに着目し、明らかに異なるゲノム異常を示した2例を除き25例の腫瘍の全ゲノムを比較したところ、肝炎ウイルスの種類や飲酒の習慣などと関連性があることが分かりました。中でも、がんの原因因子が同じと考えられる多中心性腫瘍に由来する4例は極めて類似していました(図1)。以上から、肝臓がんは非常に多様なゲノム変異を示す一方で、塩基配列の置換パターンは、がんの原因となる肝炎ウイルスや飲酒の有無の影響を受けることが分かりました。
次に、27例の肝臓がんでゲノム変異を起こした遺伝子リストを作成し、それらを統計解析しました。その結果、16例(約60%)の肝臓がんで、ARID1A、ARID1B、ARID2、MLL、MLL3などクロマチン制御に関わる10個の遺伝子のうち1つ以上の遺伝子変異が起きていました(図2)。また、細胞株を用いた実験により、それら遺伝子の多くは腫瘍抑制機能を有していることも分かりました。
B型肝炎ウイルスは、そのゲノムが肝細胞のゲノムに入りこみ、発がんさせると考えられてきています。今回の11例のB型肝炎関連の肝臓がんを解析すると、4例でTERT遺伝子周辺にB型肝炎ウイルスのゲノム配列が挿入されていることが分かりました。TERT遺伝子は、染色体末端の構造を維持し、細胞の不死化に重要な働きをするテロメラーゼの活性に関与しています。このB型肝炎ウイルスゲノムのTERT周辺への挿入が、B型肝炎関連の肝臓がんの原因の1つと考えられます。
今後の期待
今回、ウイルス性に限っても、肝臓がんのゲノム変異は非常に多様であることが分かりました。約60%の肝臓がんでクロマチン制御機構の異常が認められたことから、これを標的とした新たな治療法や予防法を開発できる可能性があります。また、個々の肝臓がんでは、分子標的治療の標的となるゲノム変異がリン酸化酵素(キナーゼ)などで多数見つかっています。今後、個々の腫瘍のゲノム変異情報に基づいて、がんの個別化医療を展開できる可能性がありますが、そのためにはさらに解析数を増やす必要があります。
2012年3月の時点で、ICGCでは47個のがんゲノムに関するプロジェクトが進行中であり、3,500症例以上の塩基配列の解析データが 一般に公開されています(英語)。日本の肝臓がんに関するゲノムプロジェクトについては、現在77例の肝臓がんの全塩基配列の解析データをICGCで公開しており、今後さらに解析数を増やしていく予定です。
原論文情報
- Akihiro Fujimoto, Yasushi Totoki, Tetsuo Abe, Keith A Boroevich, Fumie Hosoda, Ha Hai Nguyen, Masayuki Aoki, Naoya Hoshono, Michiaki Kubo, Fuyuki Miya, Yasuhito Arai, Hiroyuki Takahashi, Takuya Shirakihara, Masao Nagasaki, Tetsuo Shibuya, Kaoru Nakano, Kumiko Watanabe-Makino, Hiroko Tanaka, Hiromi Nakamura, Jun Kusuda, Hidenori Ojima, Kazuaki Shimada, Takuji Okusaka, Masaki Ueno, Yoshinobu Shigekawa, Yoshiiku Kawakami, Koji Arihiro, Hideki Ohdan, Kunihito Gotoh, Osamu Ishikawa, Shun-ichi Ariizumi, Masakazu Yamamoto, Terumasa Yamada, Kazuaki Chayama, Tomoo Kosuge, Hiroki Yamaue, Naoyuki Kamatani, Satoru Miyano, Hitoshi Nakagama, Yusuke Nakamura, Tatsuhiko Tsunoda, Tatsuhiro Shibata, and Hidewaki Nakagawa “Whole Genome Sequencing of Liver Cancers Identifies Etiological Influences on Mutation Patterns and Recurrent Mutations in Chromatin Regulators” Nature Genetics,2012.doi: 10.1038/ng.2291
発表者
理化学研究所
ゲノム医科学研究センター
バイオマーカー探索・開発チーム
チームリーダー 中川 英刀(なかがわ ひでわき)
がんゲノミクス研究分野
分野長 柴田 龍弘(しばた たつひろ)
お問い合わせ先
独立行政法人理化学研究所 横浜研究推進部 企画課Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel:048-467-9272 / Fax:048-462-4715
独立行政法人国立がん研究センター 広報室
Tel: 03-3542-2511(代表) / Fax: 03-3542-2545
独立行政法人医薬基盤研究所 研究推進課
Tel: 072-641-9803 / Fax: 072-641-9831
補足説明
- 1.国際がんゲノムコンソーシアム(ICGC)
2008年に発足。最大50種類のがんを選定し、それらについてゲノム変異の包括的なカタログを作成するため、メンバー機関間の調整を行う組織。ICGCのメンバーは、ICGCの定めたデータ収集・解析に関する共通基準に従い、特定のがんに関する各種ゲノム変異の包括的かつ高精度な解析を分担する。得られたデータは、全世界の研究コミュニティーに対して、特許や知的所有権などを主張せずに迅速かつ無償で提供される。2012年3月時点で、14カ国とEUの組織が参画し、47個のプロジェクトが遂行されている。 - 2.B型肝炎ウイルス、C型肝炎ウイルス
日本では、B型肝炎ウイルスで約100万人、C型肝炎ウイルスで150~200万人もの持続感染者がいると推測されている。世界では、慢性B型肝炎の患者数は約3億5,000万人、C型慢性肝炎の患者数は約1億7,000万人に上っており、世界的に極めて重大な健康リスクとなっている(出典:世界肝炎アライアンス)。 - 3.次世代シーケンサー
2003年のヒトゲノム解析計画終了後、ヒトゲノムの配列30億塩基対を1,000ドル以下のコストで解読すべく、欧米の政府や企業は技術開発を行ってきた結果、より高速高精度の性能を持つシーケンサーが開発された。通常のサンガーシーケンス法と比べて、超大量のDNAシーケンス反応を並列して行う技術であり、現在の第2世代の場合、12日間で約6,000億個の塩基配列を解読することができる(ヒトゲノム6人分をカバー)。さらに、現在開発中の第3世代の場合、高速で一分子シーケンスも可能であり、1日で個人のゲノム解読が可能になりつつある。 - 4.ポイント変異
ゲノム上の塩基配列の1個~数個が入れ変わったり、抜けたり、挿入されたりする変異。 - 5.ゲノム構造異常
ゲノム上の塩基配列の1個~数個が変異するポイント変異に対して、数百から数千万塩基にわたって、通常2コピーある配列が1コピーになったり(コピー数異常)、別の染色体部位に位置が変わったり(転座)、方向が入れ替わったり(逆位)など、大きく塩基配列が変化する異常。 - 6.クロマチン制御
高等生物のDNAはヒストンというタンパク質と複合体を形成してクロマチン構造をとり、その複合体の形成を通して、RNAへの転写やDNA複製を制御している。DNAのメチル化やヒストンの化学的修飾、他にさまざまなタンパク質との複合体形成によってクロマチン構造の開閉が行われる。この現象をDNAの配列情報であるゲノムとの対比で、エピゲノムと呼ぶ。 - 7.TERT遺伝子
ヒトの5番染色体に位置する TERT( telomere reverse transcriptase)遺伝子は、テロメラーゼの逆転写酵素活性を持つ触媒サブユニットをコードしている。テロメラーゼとは、染色体末端(テロメア)の反復配列を伸長させる酵素。テロメラーゼ活性が低い細胞は、細胞分裂ごとにテロメアの短縮が進み、やがて細胞分裂の停止が起きる。一方、がん細胞、生殖細胞、幹細胞では、高いテロメラーゼの活性が認められ、それらの細胞が分裂を継続できる性質に関与している。 - 8.共同研究を行った肝臓がんの専門医療機関
和歌山県立医科大学第2外科(山上 裕機教授) 国立がん研究センター中央病院(小菅 智男副院長) 広島大学医学部消化器内科(茶山 一彰教授) 大阪府立成人病センター(石川 治院長) 東京女子医科大学消化器外科(山本 雅一教授) - 9.多中心性腫瘍
肝臓がんは、肝硬変などの非常に強い発がんの危険のある背景をもつ肝臓のもと、転移ではなく、独立した肝臓がんの腫瘍が同時性または異時性に多発してくる傾向がある。
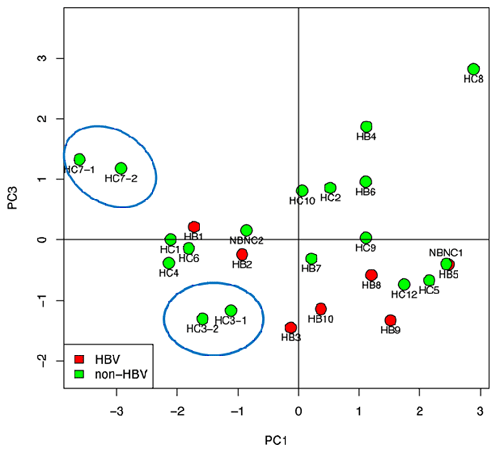
図1 塩基置換パターンに基づく、肝臓がんのゲノム全体でみた変異の類似状況
収集した27例のうち2例は、他と明らかに異なるゲノム異常を示していたので事前に排除し、23人の患者からの25例の肝臓がん(内2人の患者は2例の腫瘍を持つ)について塩基置換パターンについて解析を行った。
B型肝炎関連のうち3例(HB4、HB6、HB7)には、B型肝炎ウイルスの挿入は見られなかった。また、同じ患者由来の多中心性腫瘍(青丸)では、塩基が置換されたパターンは酷似している。
HB:B型肝炎関連、HC: C型肝炎関連、NBNC: 非ウイルス性
HBV:B型肝炎ウイルスゲノムの挿入がある肝臓がん(赤丸)
non-HBV:B型肝炎ウイルスゲノムの挿入がない肝臓がん(緑丸)
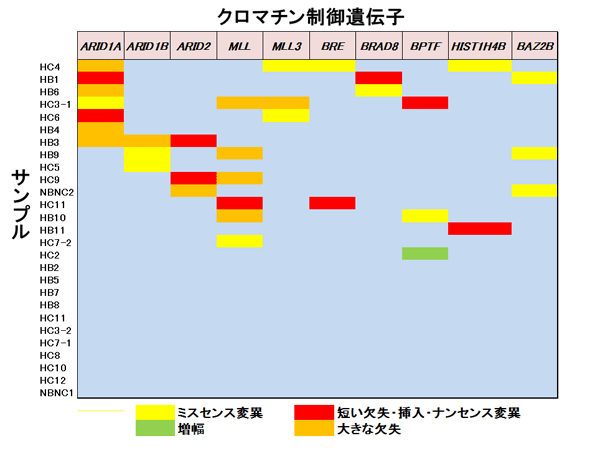
図2 27例の肝臓がんのクロマチン制御遺伝子の変異の有無
約60%の肝臓がんで、1つ以上のクロマチン制御遺伝子の変異が認められる。
ミスセンス変異:ゲノム変異の結果、タンパク質のアミノ酸配列が変化する
短い欠失・挿入・ナンセンス変異:ゲノム変異の結果、タンパク質が短くなる
増幅:ゲノム上で本来のコピー数以上に増加すること
大きな欠失:ゲノム配列の大部分が欠損する
