2017年1月11日
理化学研究所
日本医療研究開発機構
iPS細胞由来の網膜組織を用いた視機能の回復
-マウス網膜変性末期モデルへの移植による機能検証-
要旨
理化学研究所(理研)多細胞システム形成研究センター網膜再生医療研究開発プロジェクトの万代道子副プロジェクトリーダーらの研究チーム※は、マウス網膜変性[1]末期モデルを用いて、マウスiPS細胞(人工多能性幹細胞)[2]由来の網膜組織を移植することにより、光に対する反応が回復することを確認しました。
網膜は再生力が低い組織で、障害を受けると自然な治癒は見込めません。ごく一部の原因遺伝子に対しては海外で遺伝子治療の治験がすすめられていますが、末期の網膜変性では現在のところ人工物を用いる人工網膜以外に確立した治療法はありません。2006年にiPS細胞が発見されて以来、世界中で成体幹細胞[3]由来、ES細胞(胚性幹細胞)[2]由来、iPS細胞由来の網膜組織を変性網膜に移植する試みが行われています。しかし、既に視細胞[4]をほぼ消失した末期の変性網膜において、移植された網膜組織が成熟して光に応答し、さらにシナプス[5]が形成されたことをはっきりと確認した報告はありませんでした。
研究チームは2014年に、マウスのES細胞やiPS細胞から自己組織化[6]により分化させた立体網膜組織が、移植先の網膜変性末期マウスの網膜にきれいに生着し、視細胞が高度に成熟した外節構造[7]を持つ形態になることを報告しました。今回、研究チームは遺伝的な標識法を用いて、網膜変性末期マウスの網膜細胞と移植片内の視細胞が接触したことを確認しました。また、新たに開発した視機能の評価方法により、移植後のマウスの行動パターンを解析したところ、光応答性に関わる行動パターンに変化がみられました。続いて移植後の網膜の光応答を電気生理学的に記録したところ、さらに上流の脳につながる神経節細胞からも光応答がシナプスを介して得られることを確認しました。これらの結果は自己組織化により分化した網膜組織が実際に移植素材として有効であること、さらに開発した視機能の評価方法が従来の視機能検査法では確認が困難だった部分的な視野回復の変化を捉えるのに有効な手段であることを示しています。
本研究は、研究チームが目指している網膜色素変性[1]患者に対するiPS細胞由来網膜組織の移植治療における裏付け実験として大きな意義があります。
本成果は米国の科学雑誌『Stem Cell Reports』に掲載されるのに先立ち、オンライン版(1月10日付け:日本時間1月11日)に掲載されます。
本研究は、日本医療研究開発機構(AMED)「再生医療実現拠点ネットワークプログラム 疾患・組織別実用化研究拠点(拠点A)」(平成27年度より科学技術振興機構から移管)、科学研究費補助金「基盤C」の支援を受けて行われました。
※研究チーム
理化学研究所 多細胞システム形成研究センター
網膜再生医療研究開発プロジェクト
副プロジェクトリーダー 万代 道子(まんだい みちこ)
プロジェクトリーダー 高橋 政代(たかはし まさよ)
研究員 砂川 玄志郎(すながわ げんしろう)
研究員 金子 潤(かねこ じゅん)
テクニカルスタッフ 藤井 桃(ふじい もも)
テクニカルスタッフ 橋口 朋代(はしぐち ともよ)
テクニカルスタッフ 庄 隼生(しょう じゅんき)
テクニカルスタッフ 山田 千佳子(やまだ ちかこ)
研修生(研究当時) 孫 嘉楠(ソン カナン)
研修生 伊藤 晋一郎(いとう しんいちろう)
背景
網膜は光を感じ取る感覚網膜とそれを支える網膜色素上皮で構成されています(図1)。感覚網膜は神経節細胞、双極細胞、視細胞など5種類の神経細胞が層状になっています。神経細胞は他の神経細胞とシナプスという構造を形成して繋がり、情報伝達を行っています。光が感覚網膜に達すると、視細胞で電気信号に変換され、網膜内での神経細胞間の伝達を経た後、視覚情報として脳に伝えられます。
網膜は再生力が低い組織であり、障害を受けると自然な治癒は見込めません。網膜色素変性は遺伝的な背景要因により、網膜の中で最初に光に反応する視細胞が特異的に変性し消失していく疾患です。視細胞がほぼ消失している末期の網膜変性では、現在のところ人工物を用いる人工網膜以外に確立した治療法はありません。
2006年にiPS細胞が発見されて以来、世界中で成体幹細胞、ES細胞(胚性幹細胞)またはiPS細胞(人工多能性幹細胞)由来の視細胞を変性網膜に移植する試みが行われています。しかし、末期の網膜変性に対して、視細胞を移植してシナプスが形成されることをきちんと確認した報告はありません。
研究チームは2014年に、マウスのES細胞やiPS細胞から自己組織化により分化させた立体網膜組織を網膜変性末期マウスの網膜に移植すると、移植片の中の視細胞は外節構造という最終形態まで成熟することを示し、移植先の神経細胞(双極細胞)との間にシナプスを形成する可能性があることを報告しました注1)。
今回、①移植先の双極細胞と移植片視細胞との間のシナプス形成、②移植後のマウスの光に対する行動、③移植後の網膜の光応答を順を追って詳しく調べることにより、立体網膜組織の移植によって実際に光応答性を獲得できるか検討しました。
注1)Assawachananont J et.al.. Stem Cell Reports. 2014 Apr 24:662-74
研究手法と成果
研究チームはまず、感覚網膜にある双極細胞を蛍光緑色タンパク質(GFP)で標識したL7-GFPマウスと、病気の進行が早い網膜変性マウス(rd1)を交配させ、網膜変性末期マウスを作製しました。この網膜変性末期マウスは、L7-GFPマウスの遺伝情報を引き継いでいるため双極細胞がGFPで標識されています。
次に別のマウスから樹立したiPS細胞を使い、網膜変性末期マウスに移植する網膜組織を作製しました。視細胞には錐体細胞と桿体(かんたい)細胞[4]の2種類がありますが、この網膜組織の中の視細胞は桿体細胞のシナプス末端マーカーであるCtBP2タンパク質を赤色蛍光タンパク質(tdTomato)で標識しています。
シナプスは双極細胞の軸索末端と視細胞のシナプス末端が接触することで形成されます。作製した網膜組織を網膜変性末期マウスの網膜に移植したところ、移植先の双極細胞の軸索末端と移植片内の視細胞のシナプス末端が実際に接触していることを確認しました。(図2)。
続いて、シャトルアボイダンス・テスト(SAS)という行動検査用システムを用いて、網膜組織移植後の網膜変性末期マウスの行動解析を行いました。SASシステムでは、マウスは隣り合った二つの部屋の間を自由に行き来きます。まず、無作為なタイミングでマウスのいる部屋にブザー(音)と光の両方を先行シグナルとして与え、続いて5秒後に電気ショックを与えることにより、先行シグナルの後5秒以内に反対の部屋に移動すれば電気ショックを避けられることをマウスに学習させます(図3)。次に、ブザーをなくして光のみの先行シグナルに続いて5秒後に電気ショックを与えるよう学習させると、目が見えている野生型マウスは光が点灯すれば反対の部屋に移動しますが、目が見えないマウスはシグナルに気づくことができないため電気ショックを受けてしまいます。
この訓練を繰り返し、電気ショックを回避する率を調べます。目が見えないマウスの中には、動き回っている方が安全なことに気づくマウスが出てきます。つまり、動き回ることで偶然に電気ショックを逃れることができるようになり、光シグナルとは無関係に見かけ上の回避率が上がります。そこで、動き回るほど電気ショック回避率が上がるという行動パターンをモデル式に当てはめ、光シグナルを認識して電気ショックを避けているマウスを検出する推定法を確立しました(図4)。
従来の視機能検査法では、移植後に視野の一部が限局的に回復する状態を検出することは困難でした。しかし、この方法では移植後の網膜変性末期マウス21匹のうち9匹の光シグナルに対する行動パターンが改善したことを確認できました。
今回の実験では、移植部分は全体の視野の5%にも満たないため、網膜のより広い範囲に視細胞を移植すれば、改善率(回避率)がさらに向上する可能性があります。
さらに、移植後の網膜変性末期マウス7匹から網膜を取り出し、多電極アレイシステム[8]を用いて詳しい電気生理学的な解析を行いました。その結果、全例で移植部分に網膜全体としての光応答性の反応が検出されました(図5A)。また、脳に直接電気信号を送る神経節細胞からも光応答性の反応が検出されました(図5B)。さらにこの反応は、シナプス遮断により視細胞からの入力をブロックする薬剤(L-AP4)を添加すると消失し、その薬剤を洗い流すと回復しました。このことから、移植片視細胞からの入力を受けた反応であることが示されました(図5C)。
加えて、同じ移植部位について三次元的な組織学的解析を行いました。その結果、神経節細胞からの反応は露出した移植網膜組織内の細胞から検出されたものではなく、移植先の網膜からの反応であることを確認しました。また、神経節細胞の応答の性質と状態をその反応パターンごとに分類(クラスター分類)したところ、変性網膜の神経節細胞からは記録されない一過性 ON反応[9]が移植後網膜の神経節細胞から記録されました。これは、光応答反応が回復していることを示しています。
以上の結果より、光応答性を失った網膜変性末期マウスにおいて、マウスiPS細胞由来の網膜組織を移植すると、移植部位において光に対する反応が回復することを確認しました。
今後の期待
研究チームは、2016年にヒトES由来網膜組織をラットやサルの末期変性モデルに移植すると、マウスと同様に組織学的に成熟、生着することを報告しました注2)。現在、ヒトES細胞やiPS細胞由来網膜においても、視機能の検証を行っています。今後、末期変性の病態において、ヒトiPS細胞由来網膜移植によって光に対する反応が回復することを実証できれば、臨床研究への応用が期待できます。
注2)Shirai et al. Proc Nat Acad Sci U S A.2016 (1):E81-90
原論文情報
- Michiko Mandai, Momo Fujii, Tomoyo Hashiguchi, Genshiro A Sunagawa, Shinichiro Ito, Jianan Sun, Jun Kaneko, Junki Sho, Chikako Yamada, Masayo Takahashi, "iPSC-derived retinal transplants improve vision in rd1 end-stage retinal degeneration mice", Stem Cell Reports
発表者
理化学研究所
多細胞システム形成研究センター 網膜再生医療研究開発プロジェクト
副プロジェクトリーダー 万代 道子(まんだい みちこ)
 万代 道子
万代 道子
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
日本医療研究開発機構(AMED)
戦略推進部 再生医療研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
Tel: 03-6870-2220 / Fax: 03-6870-2242
saisei [at] amed.go.jp(※[at]は@に置き換えてください。)
産業利用に関するお問い合わせ
理化学研究所 産業連携本部 連携推進部お問い合わせフォーム
補足説明
- 1.網膜変性、網膜色素変性
網膜変性は、網膜を構成する中でも光受容体である視細胞が加齢や遺伝的原因などで変性し、脱落するために起こる。失明を含む強度の視力障害に至る重篤な疾患である。代表的なものは、視細胞が遺伝的原因などで変性して起こる網膜色素変性と、色素上皮が加齢などの原因で機能不全を起こして生じる加齢黄斑変性がある。 - 2.iPS細胞(人工多能性幹細胞)、ES細胞(胚性幹細胞)
脊椎動物の初期胚が持つ、全ての種類の体細胞へ分化する能力を多能性という。多能性を持ち、試験管内で培養して無限に増やすことができる細胞を多能性幹細胞という。iPS細胞は、成人の皮膚細胞などの体細胞・組織から採取した細胞に Oct3、 Sox2、 Klf4遺伝子などを導入して初期化し多能性を持たせ、人工的に作製した多能性幹細胞である。ES細胞は、哺乳類の着床前胚(胚盤胞)に存在する内部細胞塊から作製された多能性幹細胞。 - 3.成体幹細胞
生体内に存在する未分化な細胞で、増殖、組織に応じた分化能を持つ細胞。網膜では毛様体細胞、ミュラー細胞などが成体幹細胞としての性質を持つと考えられている。 - 4.視細胞、桿体(かんたい)細胞
視細胞は光を受け、その信号を網膜内の神経細胞へ伝達する重要な役割を担っている。視細胞は大きく分けて、錐体細胞と桿体細胞の2種類が存在する。錐体細胞は、明るいところで物を見るときに使われ、桿体細胞は、暗いところで物を見るときに使われる。 - 5.シナプス
神経細胞同士の情報伝達に関わる構造。情報を伝える細胞と伝えられる細胞の間には約20ナノメートル(nm、1nmは10億分の1m)のすき間がある。情報を伝える細胞はこのすき間に神経伝達物質を放出し、伝えられる細胞側の神経伝達物質受容体がそれを受け取ることにより神経情報が伝わる。 - 6.自己組織化
1種類あるいは少数の種類の要素が、外部から特別の「指示」となる情報を受けることなく、自分たちの内在的な特性を発揮して自発的に複雑な高次の構造を組み上げて行くこと。例えば、雪の結晶形成のようにパターンのない集合体の中で、自発的な秩序が生まれてパターンが形成される自然現象が観察される。その他、ナノテクノロジーや光学結晶の作製などで工学的に利用されている。 - 7.外節構造
視細胞は、外節、内節、核を含む細胞体、接合部から構成されている。桿体細胞の外節(下図)は円盤膜が積み重なった円筒状の形状をしていて、光受容物質のロドプシンを高密度で含有しており、この部分で光子と反応する効率を高めている。外節構造を持つことにより、視細胞は高感度で光を捉えることができる。一方、内節にはミトコンドリアなどがあり、視細胞に必要なエネルギーを作っている。なお、錐体細胞の外節は円錐状をしている。
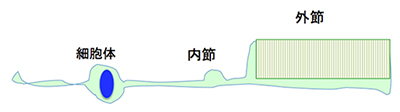
- 8.多電極アレイシステム
複数の電極が配置されており、その上に組織を載せて、電極に隣接している細胞の細胞外電位を捉えることにより、細胞の活動を記録することができる。網膜においては、電極上の網膜全層の電位の変化を捉えるいわゆる「網膜電位図」のような波形と、電極に隣接している神経節細胞の活動の両方を記録することができる。網膜電位図では網膜内の各種細胞の活動を大まかに捉えることができる。 - 9.一過性 ON反応
神経節細胞には多くの種類があり、光照射やそのパターンに対して、さまざまな反応がみられる。光の刺激開始時のON反応、終了時のOFF反応、ON・OFFの立ち上がりの早いもの遅いもの、一過性の反応、持続性の反応などさまざまである。本研究では正常網膜の全照射時によくみられる反応の一つとして、一過性のON反応に注目して解析した。
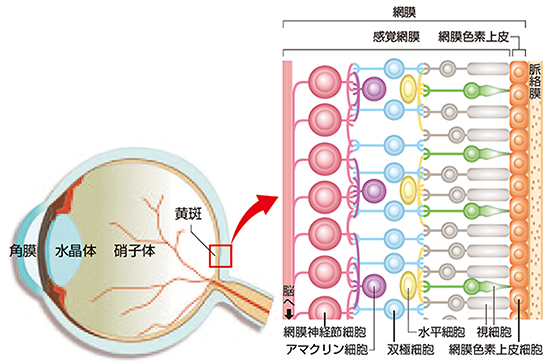
図1 眼球と網膜の基本構造
網膜は大きく分けて視細胞、水平細胞、双極細胞、アマクリン細胞、(網膜)神経節細胞の5種類の神経細胞から成る感覚網膜と、それを支える網膜色素上皮から構成される。光が眼球の角膜、水晶体、硝子体を通って感覚網膜に達すると、視細胞で電気信号に変換される。電気信号は網膜内での神経細胞間の伝達を経た後、網膜神経節細胞から視覚情報として脳に伝えられる。また、視細胞は錐体細胞(緑色)と桿体細胞(灰色)の2種類がある。網膜の中心部に直径2mm(ヒト)ほどの黄班という領域がある。黄班は視力を担い、その周辺部は視野を担っている。『理研ニュース』2014年7月号より転載。
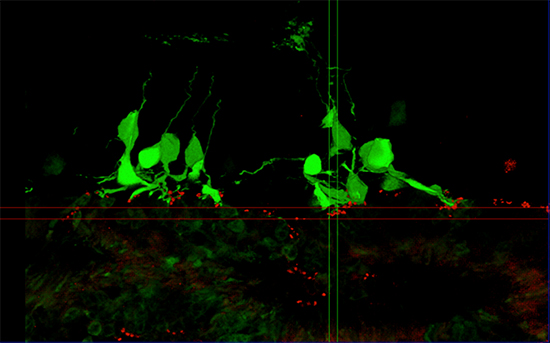
図2 マウスiPS細胞から分化させた網膜組織を移植した網膜変性末期マウスの網膜
網膜組織を移植した後の網膜の蛍光顕微鏡画像。網膜変性末期マウスの双極細胞(緑)の軸索末端と移植片内の視細胞のシナプス末端(赤)が接触していることが分かる。

図3 行動検査用シャトルアボイダンス・テスト(SAS)システムの仕組みと実験装置
(左)マウスは左と右の二つの部屋を自由に行き来でき、無作為なタイミングでマウスのいる部屋で光とブザーシグナル、または光シグナルのみを与えた後5秒後に電気ショックを与える。マウスは光シグナルを認識すると、反対の部屋に移動して電気ショックを避けることができる。
YouTube:iPS由来網膜移植後の光応答性行動解析(効果が見られた例)
YouTube:iPS由来網膜移植後の光応答性行動解析(効果が見られなかった例)
(右)SASシステムの実験装置の写真。
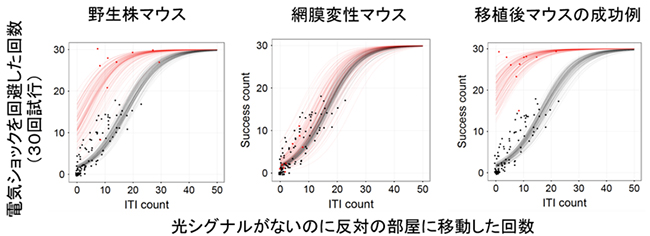
図4 SASシステムで電気ショックを回避するマウスを検出する推定法
目が見えないマウスは光シグナルを認識できないため、動き回るほど(横軸で右にいくほど)偶然に電気ショックを回避する率(縦軸)が高くなる。そのような目の見えない行動パターン(黒点、網膜変性マウス11匹からのデータ)をモデル式にあてはめると、黒のカーブのようになる(コントロール)。
左図:目が見えるマウス(野生株)の1例。無駄な動きが少なく、電気ショックを回避するため(赤点)、そのパターンを近似した曲線は4匹全例で赤線のように上に外れた。
中図:他の系統の網膜変性末期マウスの1例。10匹全例で黒のカーブで示したコントロールと同じような行動パターンとなった。
右図:移植後のマウスの1例。21匹のうち9匹で目が見えるマウス(野生株)と似た行動パターンがみられた。
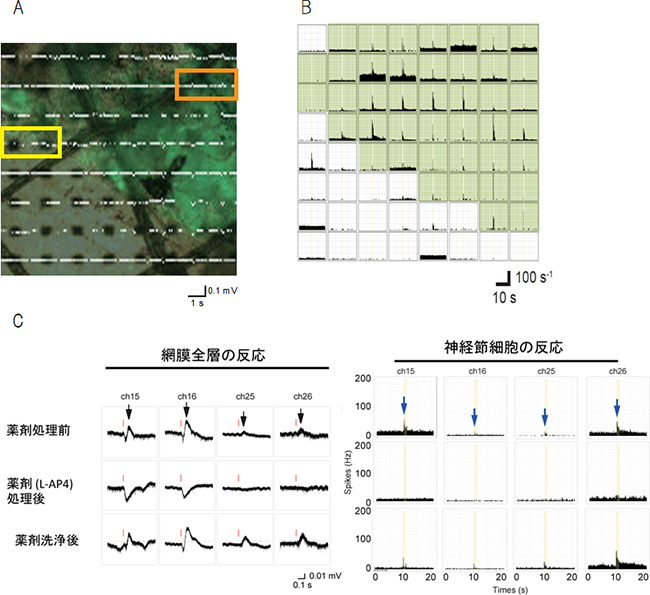
図5 移植片視細胞移植後マウスの神経節細胞の電気生理学的な解析
A:網膜組織移植片およびその近くの網膜の光反応を64電極(8x8)上で計測した。右上半分の緑色の部分は移植片が生着した網膜部分である。オレンジ色の線で囲んだ2電極(ch15とch16)は移植片上にあり、黄色の線で囲んだ2電極(ch25とch26)は移植片周縁にある。大きさは縦横50マイクロメートル(μm、1μmは1,000分の1mm)の電極が100マイクロメートル間隔で並んでいる。
B:A全体の神経節細胞の電位変化を記録した図。移植片上およびその周辺(薄緑色をつけた部分)で光応答が記録された。
C:Aの移植片上の2電極と移植片周縁の2電極の網膜全層および網膜神経節細胞の光応答反応。いずれの電極でも、視細胞からの入力をブロックする薬剤(L-AP4)で処理すると、上むきの波形である双極細胞の反応および神経節細胞の反応が消失したが、薬剤を洗浄すると復活した。
