2010年9月30日
独立行政法人 理化学研究所
食物アレルギーの画期的な治療法につながる経口免疫寛容の仕組みを発見
-マウスの経口免疫寛容の分子作用機構を世界で初めて証明-
ポイント
- 経口免疫寛容を誘導する腸管内の「樹状細胞(白血球)」の役割を解明
- 経口免疫寛容の成立に必須な共刺激分子2種をマウスで発見
- 免疫寛容の仕組みを利用して食物アレルギーの新たな治療法を提示
要旨
独立行政法人理化学研究所(野依良治理事長)は、免疫システムが飲食物を異物として認識し、食物アレルギー※1と呼ぶ免疫反応を引き起こすことを防ぐ「経口免疫寛容※2」の仕組みを、マウスの実験で初めて明らかにしました。この経口免疫寛容が成立するためには、腸管に存在する樹状細胞※3がB7-H1とB7-DCという分子を介して、免疫抑制能を持つ制御性T細胞※4を誘導することが必須であることを見いだしました。これは、理研免疫・アレルギー科学総合研究センター(谷口克センター長)樹状細胞機能研究チームの佐藤克明チームリーダーらによる研究成果です。
免疫寛容は、生体の防御システムにおいて通常の免疫反応を引き起こすことができなくなった状態のことで、生体が自己の成分を異物として認識せず、免疫反応を引き起こさないのは、この免疫寛容によるものです。この自己に対する寛容性が崩れると、自己免疫疾患を発症することが知られている一方で、さまざまな方法によって免疫寛容を成立させて、自己免疫疾患を抑制する治療法の開発が進んでいます。
食物アレルギーは、免疫寛容が崩れることで起こりますが、通常では、腸管で食物中の異種タンパク質に対する免疫反応を抑制する経口免疫寛容が成立しているため、食物アレルギーは起こりません。この経口免疫寛容の成立には、腸間膜リンパ節※5で、免疫細胞の1つであるT細胞の食物に対する過剰な反応を抑えることが重要と考えられていますが、その仕組みは不明のままでした。
研究チームは、マウス食物経口投与免疫モデル※6を使い、共刺激分子※7のB7-H1とB7-DCが経口免疫寛容の成立に必須であることを初めて突き止めました。さらに、腸間膜リンパ節の樹状細胞が、B7-H1とB7-DCを介して制御性T細胞を誘導し、食物を異物と認識するT細胞の活性化を阻害するという仕組みを明らかにしました。この経口免疫寛容の仕組みを応用することで、食物アレルギーの画期的な治療法につながる可能性が期待できます。
本研究成果は、米国の科学雑誌『Blood』オンライン版(9月30日付け:日本時間9月30日)に掲載されます。
背景
食物中には、生体にとって異物である異種タンパク質が含まれ、飲食により食物アレルギーを引き起こすことがあります。食物の種類や生体の免疫システムの状況によってアレルギーの症状は異なりますが、一般的には下痢、湿疹、じんま疹、咳、ぜんそくを発症します。重篤な場合はアナフィラキシーショックを発症し、命にかかわることがあります。卵、ピーナッツ、そばなどがよく知られていますが、こうした食物アレルギーの予防は社会的な課題の1つで、食品衛生法の施行規則により、特定原材料の表示が義務化されるまでに至っています。
腸管では、これらの免疫反応を抑制する経口免疫寛容が成立しており、通常、すべての食物に対するアレルギーは起こりません。しかし、食物アレルギーは、経口免疫寛容が適切に働かないことが原因で引き起こされます。経口免疫寛容の仕組みを応用すると、食物アレルギーの画期的な治療法につながると期待されています。
腸間膜リンパ節を切除したマウスでは、経口免疫寛容成立がしないため、腸間膜リンパ節が、経口免疫寛容の成立に重要な腸管粘膜免疫組織であると考えられています。研究チームのこれまでの研究から、共刺激分子として知られるB7-H1とB7-DCが、腸間膜リンパ節にある樹状細胞で、脾臓(ひぞう)などほかの組織にある樹状細胞よりも高く発現していることが分かってきていました。また、経口免疫寛容の成立には、腸間膜リンパ節において、免疫細胞の1つであるT細胞の食物に対する過剰な反応を抑えることが重要であると考えられていました。しかし、共刺激分子を含む詳細な分子メカニズムは明らかとなっていませんでした。
研究手法と成果
(1)経口免疫寛容の成立に関与する分子の同定
研究チームは、B7-H1とB7-DCが経口免疫寛容の成立に関与していることを明らかにするために、野生型マウスとB7-H1とB7-DCをそれぞれ欠損したマウス(B7共刺激分子欠損マウス)を用いて、経口免疫寛容の誘導について検討しました。
野生型マウス1匹に対して、アレルギーの原因物質となる卵白アルブミンを体重20g当たり0.1mgの量と免疫強化剤0.05mgを皮下注射(皮下免疫)すると、卵白アルブミン反応性T細胞が誘発し、卵白アルブミンに対する抗体(抗卵白アルブミン抗体)が大量に産生しました。しかし、あらかじめ卵白アルブミンを体重20g当たり25mgの量を経口摂取させておくと、卵白アルブミン抗体の誘発が80%も阻害されました(図1)。これは、野生型マウスでは、あらかじめ卵白アルブミンを経口摂取させることで、卵白アルブミンに対する経口免疫寛容が成立していることを示しています。しかし、B7共刺激分子欠損マウスでは、あらかじめ卵白アルブミンを経口摂取させても、卵白アルブミン抗体の誘発阻害効果が30%以下にとどまり、免疫寛容が成立しませんでした(図1)。これらの結果から、経口免疫寛容の成立には、腸間膜リンパ節にある樹状細胞でのB7-H1とB7-DCの発現が必須であることが分かりました。
(2)経口免疫寛容の成立における腸管膜リンパ節樹状細胞の役割の解明
卵白アルブミンをあらかじめ経口摂取した野生型マウスの群は、摂取しなかった群と比較して、腸間膜リンパ節での免疫抑制能をもつ制御性T細胞の数が約1.5倍増加していました。さらに、卵白アルブミンの経口摂取後に制御性T細胞を除去する機能を持つ抗CD25抗体を投与すると、経口免疫寛容は成立しませんでした。これらのことから、卵白アルブミンを経口摂取することによって、腸間膜リンパ節では制御性T細胞が誘導し、卵白アルブミン反応性T細胞の活性化を抑制することにより、経口免疫寛容が成立することが分かりました。
さらに、試験管内の実験により、野生型マウスから採取した腸間膜リンパ節の樹状細胞が、ナイーブT細胞※8に卵白アルブミンを提示して、制御性T細胞を効率良く誘導することが分かりました。しかし、B7-H1欠損マウスやB7-DC欠損マウスから採取した腸間膜リンパ節の樹状細胞の場合は、その誘導効果がそれぞれ50%以上減弱していました(図2)。また、このB7共刺激分子欠損マウスでは、卵白アルブミンをあらかじめ経口摂取させても、腸間膜リンパ節の制御性T細胞の増加は認められませんでした。これらのことから、腸間膜リンパ節では、食物タンパク質を取り込んだ樹状細胞がナイーブT細胞にその情報を提示した後、B7-H1とB7-DCを介して制御性T細胞を誘導し、食物タンパク質に特異的に反応する反応性T細胞を抑制することで経口免疫寛容が成立することを解明することができました。
今後の期待
今回、経口免疫寛容の成立の仕組みを明らかにしたことから、この仕組みを応用した画期的な食物アレルギーの治療法の開発が期待できます。今後は、B7-H1とB7-DCをターゲットとした自己免疫病の分子標的治療の開発を進めていきます。
発表者
理化学研究所
免疫・アレルギー科学総合研究センター
樹状細胞機能研究チーム
チームリーダー 佐藤 克明(さとう かつあき)
Tel: 045-503-7013 / Fax: 045-503-7013
お問い合わせ先
横浜研究所 研究推進部Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.食物アレルギー
食物を飲食することで体内に取り込まれ、アレルギー状態が発生する免疫反応。食物アレルギーでは、口腔(くう)粘膜の腫脹や腹痛・下痢など口腔・消化管の炎症、皮膚の湿疹や浮腫などが代表的な症状。重篤な場合には、毛細血管の拡張による血圧の低下などでアナフィラキシー症状を誘発することもある。 - 2.経口免疫寛容
食物などの生体にとって必要なものを異物として認識せず免疫反応を起こさない仕組み。 - 3.樹状細胞
樹状突起を持つ白血球で、多くの亜集団がある。微生物の排除やT細胞に異物の情報を伝える細胞(抗原提示細胞)として働き、免疫反応の本質的な司令塔としての役割を担っている。 - 4.制御性T細胞
CD4陽性T細胞の5~10%を占めるT細胞亜集団で免疫抑制能を示す。膠(こう)原病などの免疫病の発症を阻止することが示されている。制御性T細胞を特定するマーカー分子は、表面抗原分子のCD25と転写因子のFoxp3である。 - 5.腸間膜リンパ節
多様な免疫細胞が存在し、食物や腸内細菌に対する免疫反応を誘導する腸管免疫組織で、小腸の管をつなぐ膜(腸間膜)に存在する結節状のリンパ節のこと。ちなみに腸管は、大腸、小腸、結腸、回腸などからなる。 - 6.マウス食物経口投与免疫モデル
マウスを用いたモデルで、食物と免疫強化剤をともに皮下注射して誘発する食物特異的な免疫反応を、あらかじめ食物を経口投与して阻害することができる実験モデル。 - 7.共刺激分子
免疫細胞の細胞膜に発現する分子で、免疫細胞同士がこれを介して結合し、お互いに活性化・抑制の情報を伝える。 - 8.ナイーブT細胞
異物に感作されていないT細胞。制御性T細胞の一部は、樹状細胞から提示される抗原などの情報によりナイーブT細胞から分化誘導する。
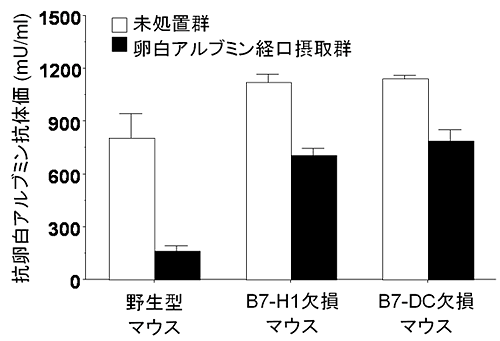
図1 卵白アルブミンの経口摂取による経口免疫寛容の誘導
卵白アルブミンと免疫強化剤を投与し、2週間後に血清中の抗卵白アルブミン抗体価を測定した。卵白アルブミン経口摂取群には、食物と免疫強化剤投与の1週間前に卵白アルブミンを経口投与しておいた。
野生型マウスでは、あらかじめ卵白アルブミンを摂取することで免疫寛容が成立しているが、B7共刺激分子欠損マウスでは、抗体産生の阻害効果が弱く(30%以下)免疫寛容が成立していない。
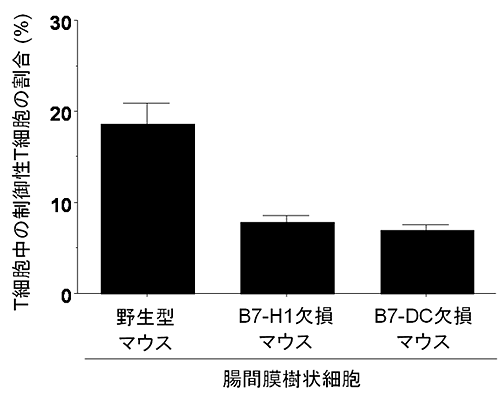
図2 腸間膜樹状細胞による卵白アルブミン特異的制御性T細胞の誘導
卵白アルブミンを取り込んだ腸間膜リンパ節樹状細胞とナイーブT細胞を3日間試験管内で培養し、全T細胞中で制御性T細胞の誘導率を測定した。野生型マウスでは、制御性T細胞を効率良く誘導したが、B7共刺激分子欠損マウスでの誘導効果は50%以上減弱している。
