2011年8月30日
独立行政法人 理化学研究所
独立行政法人 科学技術振興機構
生体をゼリーのように透明化する水溶性試薬「Scale」を開発
-固定した生体組織を傷つけることなく、数ミリの深部を詳細に蛍光観察-
ポイント
- マウス脳の神経回路を3次元再構築するコネクトミクスプロジェクトに貢献
- ラット、ブタ、サルなど、マウス以外の実験動物、脳以外の器官・組織にも適用可能
- 既存の生体イメージング技術のギャップを埋める、ヒト病理標本への応用に期待
要旨
独立行政法人理化学研究所(野依良治 理事長)は、生物試料を透明にする水溶性試薬「Scale試薬」を開発し、試料を傷つけることなく表面から数ミリの深部を高精細に観察する技術を確立しました。例えば、ホルマリンで固定した哺乳類動物の脳をScale溶液に浸すだけで透明化することができます。神経細胞を蛍光タンパク質で標識したマウスの脳に適用すると、神経回路の詳細な3次元構造を脳全体にまで広げて再構築することができます。これは、理研脳科学総合研究センター(利根川進センター長)細胞機能探索技術開発チームの宮脇敦史チームリーダー、濱裕研究員らが、JST戦略的創造研究推進事業「(ERATO)」宮脇生命時空間情報プロジェクトと共に行った研究の成果です。
研究グループは、保湿クリームや肥料に広く使われている尿素をもとにして、生体試料内の光散乱を最小限に抑える水溶性試薬「Scale」を開発し、生体試料をゼリーのように透明化することに成功しました。Scaleは、生体試料内の光の吸収にはまったく影響を与えず、生体試料内に存在する蛍光色素、特に蛍光タンパク質のシグナルにもまったく影響を与えないので、蛍光標識した構造を生体試料の深い部位まで高精細に観察することが可能になります。1つの神経細胞を1本の木にたとえるなら、従来の蛍光イメージングは「木を見て森を見ず」あるいは「森を見て木を見ず」のどちらかに偏る傾向がありましたが、Scaleは「木も森も見る」イメージングを可能にするといえます。Scale技術を、細胞周期を可視化する細胞周期蛍光プローブFucci※1を全身に発現するマウスに適用すれば、マウス胚における増殖と分化の空間パターンを丸見えにすることができます。思い通りのパターンで蛍光タンパク質を発現させる現代の遺伝子工学技術と組み合わせることによって、注目する組織構造をさまざまな空間スケールでズームインまたはズームアウトすることができるのです。さらに、研究グループは、Scale技術で透明化した脳を使って、脳の左と右の半球を連絡する神経線維束の走行や、生後の海馬における新生神経細胞と血管との位置相関を包括的に観察することに成功しました。Scale技術の普及によって、実験動物、特に哺乳類動物の個体、器官、組織レベルでの蛍光イメージング技術が一段と進展することが期待されます。
本研究成果は、米国の科学雑誌『Nature Neuroscience』への掲載に先立ち、オンライン版(8月30日付け:日本時間8月30日)に掲載されます。
背景
現代の形質転換技術や遺伝子導入技術を使えば、マウス脳のさまざまな神経回路を選択的に蛍光タンパク質の蛍光で標識することができます。標識した脳をホルマリンで固定し、蛍光を指標に3次元的に神経回路を可視化し再構築するという試みは世界的規模で行われており、神経細胞同士の連絡(コネクション)を網羅的に調べることから「コネクトミクス(プロジェクト)」と呼ばれています。
神経回路の構造を高精細に観察するためには、脳組織の切片の蛍光画像を何枚も連続的に取得し、それらを積み上げていくことが必要です。切片の作り方には2通りあり、機械的に切る方法と光学的に切る方法が採用されています。機械的な方法では、脳表面からの深さにかかわらず高精細な蛍光観察が可能ですが、大変な労力を伴うだけでなく3次元に再構築することが非常に困難です。一方、光学的な方法では、光が脳組織内部で散乱するため、観察部位が脳表面から深くなるにつれ画像が暗くぼやけるという問題があります。一般的に、蛍光イメージング技術においては、生体試料の表面から深部に向かってどこまで蛍光を観察できるか(観察深度限界)という課題があります。脳組織の場合、通常の一光子励起顕微鏡※2で0.15ミリメートル、二光子励起顕微鏡※3でも0.7ミリメートル程度が限界です。マウスの脳の場合は、表層の皮質の厚さが約1ミリメートルあり、皮質よりも脳の内側にある海馬や視床を観察するには、数ミリメートルまで観察深度限界を広げる必要があります。
私たちが肉眼で感じる可視領域の光は、なかなか生体試料を直進することができません。光の直進を妨げる主な要因は散乱です。試料の中で光の散乱が起こり、光の進行方向が変わってしまうのです。これまで光の散乱を取り除く技術(透明化試薬)がいくつか開発されてきましたが、ほとんどが有機溶媒がもとになっており、ホルマリン固定した組織を脱水する過程や透明化試薬そのものの影響で、観察したい生物構造の蛍光シグナルが消失してしまうという問題がありました。そのため、生体試料の脱水を必要としない水溶性で、かつ蛍光タンパク質にやさしい透明化試薬の開発が求められていました。近年、蛍光標識した構造を大規模・高精細に3次元で再構築するという網羅的研究アプローチは、脳神経系以外の器官や組織を対象として、ますます盛んになっており、生体組織を透明化して光学的に深くまで蛍光を観察する技術のさらなる進歩が待望されています。
研究手法と成果
(1)Scale試薬の開発
今回の研究開発における鍵分子は尿素です。研究グループは、尿素で処理をすると、いろいろな材料が水になじみやすくなること、さらに、高濃度の尿素の存在下でも、蛍光タンパク質の蛍光の明るさがまったく減弱しないことに注目しました。そこで、尿素を含む水溶性の透明化試薬の開発に取り組み、グリセロールと界面活性剤を添加したScaleA2試薬を完成させました。ホルマリン固定したマウス胎仔やマウスの脳をScaleA2試薬で2日から2週間処理したところ、ゼリーのように透明になりました(図1)。また、黄色蛍光タンパク質(YFP)を発現するマウスの脳を使って、ScaleA2試薬が蛍光タンパク質の蛍光シグナルを完全に保存することを確認しました。
(2)透明脳を使った観察例
ある神経細胞集団を黄色蛍光タンパク質(YFP)の蛍光で標識した形質転換マウス(YFP-Hライン)全身をホルマリン固定し、取り出した全脳をScaleA2溶液に1週間浸漬しました。二光子励起蛍光顕微鏡を使って、作動距離が2ミリメートルの対物レンズを脳表面に置いて観察したところ、脳皮質の全層(I層からIV層まで)、さらに白質を超えて海馬の一部まで一挙に観察することができました。また、各蛍光画像における空間分解能は高く、樹状突起の棘突起(スパイン)構造の詳細が確認できました。(図2)
二光子励起蛍光顕微鏡を使った理由は、一般的にこの観察方法における観察深度限界(~0.7ミリメートル)が一光子励起蛍光顕微鏡の限界(~0.15ミリメートル)に比べて大きいことにあります。しかし、同様の深部(~2ミリメートル)蛍光観察が、通常の一光子励起蛍光顕微鏡を使ってもできることが分かりました(図3)。
ScaleA2試薬で透明化した生体試料の観察深度限界が、対物レンズの作動距離に依存する事実を踏まえて、作動距離の長い対物レンズ(4ミリメートル カスタムメイド)を使った観察を二光子励起蛍光顕微鏡で行いました。すると脳表面から、皮質、白質を経て、さらに海馬の歯状回にいたる神経回路を可視化し3次元構築することができました(図4)。また、こうした観察を水平方向に広げることで、海馬全体の3次元構築を得ることができました(図5)。
電気穿孔技術※4を使って、子宮内のマウス胎仔の脳右半球の第II/III層の錐体細胞にYFP遺伝子を導入し、これらの神経の軸索が発生に伴って左半球に投射する経路を蛍光で標識しました。生後10日目の脳をホルマリン固定、透明化し、低倍率の対物レンズを使って一光子励起蛍光顕微鏡で観察を行ったところ、左右の半球を連結する投射線維の束の走行を3次元的に追跡することができました。(図6)。このような広視野かつ高精度に観察する技術が普及すれば、数多くの変異マウスのなかから、投射線維の走行パターンに異常があるマウスを見つけることができ、特に発生神経研究の進展につながると期待できます。
研究グループは、細胞周期の進行を指標にして、マウス脳の海馬における神経新生の可視化を行ってきました。細胞周期蛍光プローブFucciの形質転換マウスを用いると、細胞分裂に向かう神経幹細胞の核(緑色)を海馬組織内に見つけることができます。マウスの全身の血管を赤色の蛍光色素で標識して、ホルマリン固定した脳を透明化した後、緑と赤の2色蛍光観察を行いました。すると海馬の歯状回において神経幹細胞の核が血管に寄り添う様子を観察することができました。(図7)さらに研究グループが独自に開発したソフトウエア「RINZO」を使って、3次元空間における最短距離の自動測定計算を行ったところ、増殖する神経幹細胞の核が他の神経核に比べて有意に血管に近いことを証明することができました。この結果は、神経新生に必要な栄養が血管から供給されることに関連する現象と考えられます。
今後の展望
蛍光タンパク質でいろいろな生物構造を蛍光標識する技術と連携して、Scale試薬による生体試料の透明化技術は、大規模かつ高精細な3次元構造の再構築プロジェクトに著しく貢献することが期待できます。従来の光学顕微鏡や電子顕微鏡による網羅的観察は、1ミリメートル以内のスケールで詳細に行われます(木を見て森を見ず)。一方、MRIやPETなどによる観察は、個体丸ごとのスケールで粗く行われます(森を見て木を見ず)。Scale技術は、これら2つの可視化技術の間にあるギャップを埋める役割を果たすと期待されます(木も森も見る)。驚いたことに、一度透明化した生体試料もScale試薬の洗浄によって簡単に元の状態に戻せることが分かりました。つまり、透明化の後も免疫組織観察を行うことが可能なので、ズームアウトして3次元的に全体を観察し、それから注目すべき構造にズームインして詳細に組織を観察することができます。
今回の研究では、主にマウスの脳を材料にしましたが、Scale技術は脳以外の器官、組織にも適用可能です。マウス以外の哺乳類実験動物、例えばラット、ブタ、サルの試料にも適用可能です。ヒトの病理標本に適用すれば、いろいろな標識技術と組み合わせて、標本内を隈なく観察しての病変を確実に見つけ出す技術に発展することが期待できます。さらにScaleA2試薬の組成は非常に簡単です。試料の性質に合わせて自由自在にScale試薬の組成を変えることができます。研究グループは、生体試料の多様性を考慮し、ScaleA2の組成を変更してScaleU2試薬および ScaleB4試薬を開発しました。ScaleU2試薬は、透明化に伴う試料の柔軟化を抑えることができ、ScaleB4試薬は、透明化にかかる時間を短縮することができます。Scale試薬はいずれも非常に安価で、大量の試薬調製が可能です。従って大型の生体試料についてもScale技術の適用が期待できます。
研究グループは、次の目標として生物個体や生体試料を生きたまま透明化する技術の開発に乗り出しています。蛍光タンパク質を含む蛍光イメージング技術が動物個体に適用される可能性を無限に広げるための技術革新を目指しています。
発表者
理化学研究所
脳科学総合研究センター 先端基盤技術研究コア 細胞機能探索技術開発チーム
チームリーダー 宮脇 敦史(みやわき あつし)
Fax: 048-467-5924
お問い合わせ先
脳科学研究推進部 企画課
Tel: 048-467-9757 / Fax: 048-462-4914
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
研究プロジェクトに関するお問い合わせ
独立行政法人科学技術振興機構 戦略的創造事業本部
研究プロジェクト推進部
金子 博之 (かねこ ひろゆき)
Tel: 03-3512-3528 / Fax: 03-3222-2068
補足説明
- 1.Fucci
Fluorescent Ubiquitination-based Cell Cycle Indicatorの略で細胞周期の進行をリアルタイムに可視化する蛍光のプローブ。個々の細胞核を赤色(G1/G0期)または緑色(S/G2/M期)に標識する。細胞周期依存的に起こるタンパク質分解機構を活用している。2008年に理研脳科学総合研究センター細胞機能探索技術開発研究チームによって発表された。 - 2.一光子励起顕微鏡
通常の蛍光顕微鏡システムは、共焦点レーザー走査顕微鏡も含めてほとんどが一光子励起タイプである。励起光の波長は紫外領域から可視領域にあり、それぞれの蛍光分子の波長は励起光のそれより長くなる。一光子励起顕微鏡は、生体試料の散乱の影響を受けやすいので、光散乱を抑えるSca le技術の効果が際立つと考えられる。 - 3.二光子励起顕微鏡
励起光の波長が長く(近赤外光)散乱しにくいので、生体試料の深い部位にある蛍光分子を励起することができる。さらに、蛍光分子から放射される蛍光が効率よく回収される仕組みになっており、生体試料の深部観察に適している。ただ、特殊なレーザー光源が必要なため顕微鏡システムが高価格になる。 - 4.電気穿孔技術
細胞に電気パルスをかけることで細胞膜に微小な穴を開け、DNAを細胞の中に送り込む技術。今回の実験では子宮壁を貫いてYFP遺伝子を胎仔の脳室に導入し、子宮の外側から電気パルスをかけて脳室横の神経細胞にYFP遺伝子を発現させた。

図1 透明化したマウス胎仔(胎生15日)
- 左: ホルマリン固定後、生理食塩水溶液に浸漬。
- 右: ホルマリン固定後ScaleA2試薬に2週間浸漬。肝臓の色素が確認できることから光の吸収は残存されている。
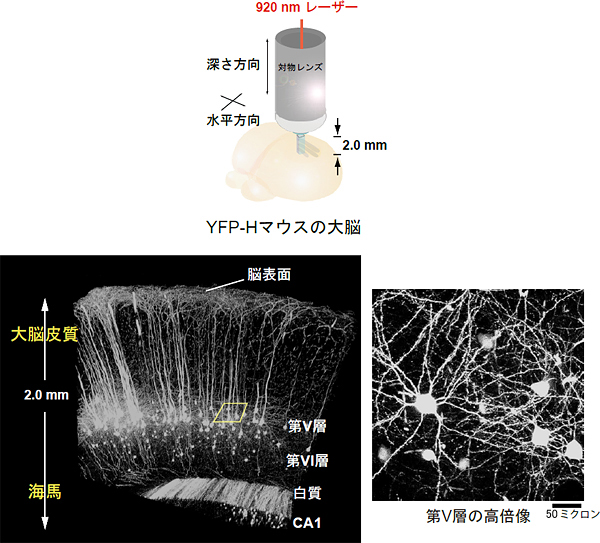
図2 二光子励起蛍光顕微鏡で観察したマウスの脳
ある神経細胞集団を黄色蛍光タンパク質(YFP)の蛍光で標識した形質転換マウスをホルマリン固定し、その全脳を二光子励起蛍光顕微鏡(励起波長920nm)を用いて作動距離2ミリメートルの対物レンズで観察。脳表面から大脳皮質、白質、海馬CA1の上部までの神経回路を高精細に観察(左図)。
第V層における高倍率画像。樹状突起の上の緻密な構造(棘突起)が見える(右図)。
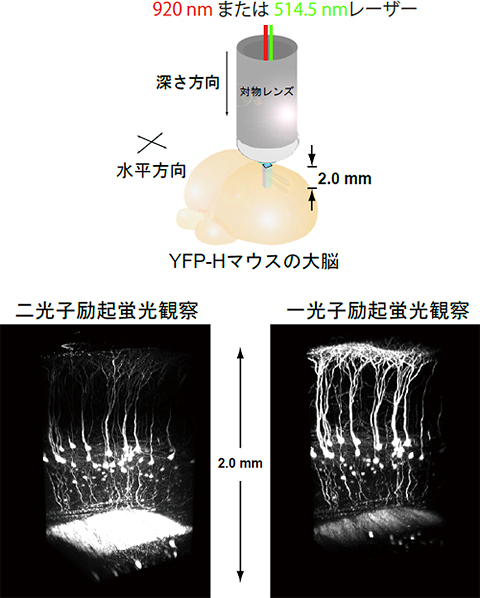
図3 二光子励起蛍光顕微鏡と一光子励起蛍光顕微鏡で観察したマウスの脳
図2同様の全脳を作動距離2ミリメートルの対物レンズを置いて観察。
まず二光子励起蛍光顕微鏡(励起波長920nm)で観察。脳表面から大脳皮質、白質、海馬CA1の上部まで確認できた(左図)。
次に同じ部位を一光子励起蛍光顕微鏡(励起波長514.5nm)で観察。
二光子励起蛍光観察とほぼ同様に高精細に神経細胞を確認できた(右図)。
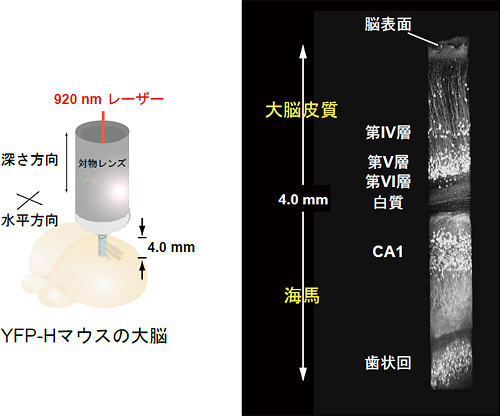
図4 二光子励起蛍光顕微鏡で観察したマウスの脳
図2同様の全脳を、作動距離4ミリメートルの対物レンズ(カスタムメイド)を置いて観察。脳表面から大脳皮質、白質、海馬CA1、歯状回まで高精細に確認。
[動画を見る]
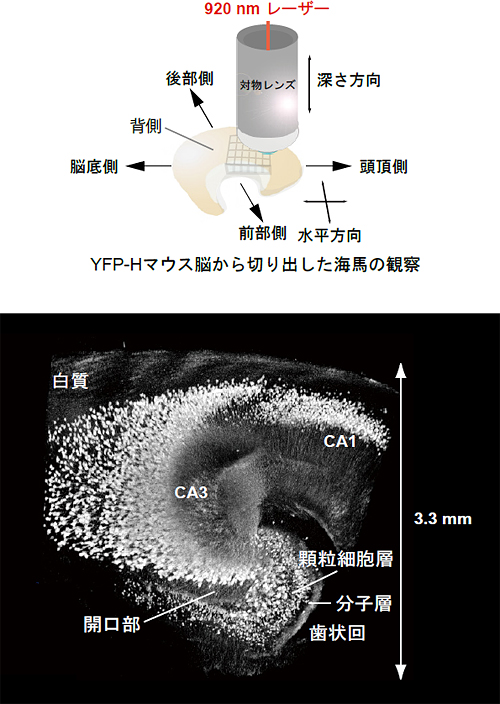
図5 3次元再構築したマウスの海馬
図2同様の全脳から切り出した海馬に、作動距離4ミリメートルの対物レンズ(カスタムメイド)を置いて垂直水平方向に観察。二光子励起蛍光顕微鏡(励起波長920nm)を使用。広範囲に海馬の神経回路を可視化。
[動画を見る]
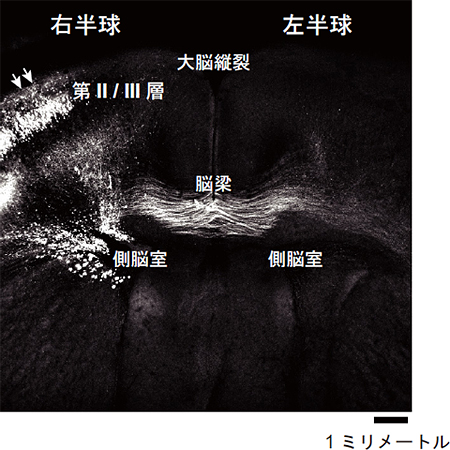
図6 右半球から左半球へ投射する神経線維束
子宮内のマウス胎仔の脳右半球の第II/III層の錐体細胞にYFP遺伝子を導入し(図中矢印部分)、生後10日目のマウス脳をホルマリン固定、ScaleA2で処理。低倍率の対物レンズを用いて一光子励起蛍光顕微鏡で観察。蛍光標識した神経線維の3次元構造を再構築。
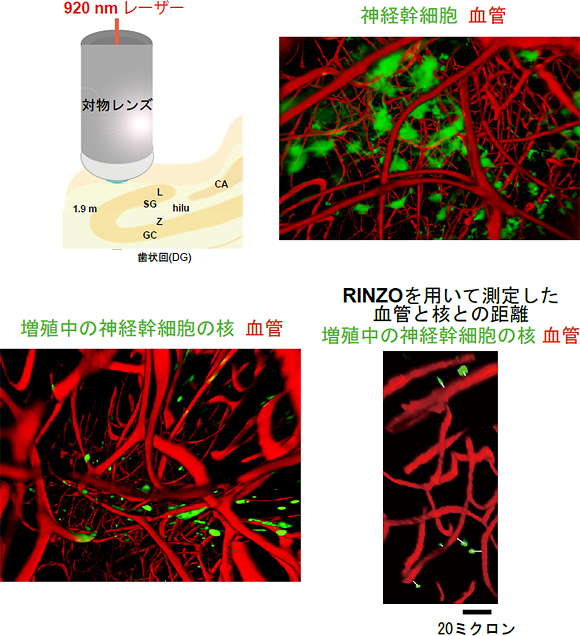
図7 マウスの海馬における神経新生(緑色蛍光)と血管(赤色蛍光)
マウスをホルマリン固定する直前に、赤色蛍光色素を血管に流して赤色で標識した。
