2012年11月9日
独立行政法人理化学研究所
ES細胞の分化制御に重要な遺伝子を発見
-半世紀以上前に見いだされた自然変異マウスに、ゲノム解析と遺伝子改変技術を適用-
ポイント
- 酵母では細胞内物質輸送を担うVps52遺伝子が、哺乳類では多能性細胞の分化を制御
- Vps52は、細胞間相互作用を介して多能性細胞の分化を制御
- ES細胞やiPS細胞の分化制御技術の開発に期待
要旨
理化学研究所(野依良治理事長)は、半世紀以上前に発見された自然発症突然変異マウスを解析し、さまざまな細胞・組織の元となる多能性細胞が分化・増殖するときに、重要な役割を果たす遺伝子「Vps52」を同定しました。これは、理研バイオリソースセンター(小幡裕一センター長)動物変異動態解析技術開発チームの阿部訓也チームリーダー、杉本道彦開発研究員、遺伝工学基盤技術室の小倉淳郎室長および米国テキサス大学オースチン校などによる共同研究グループの成果です。
哺乳類の胚※1には、将来、さまざまな細胞や組織に分化し、体全体を形成する能力を持つ多能性細胞が存在します。万能細胞と呼ばれるES細胞(胚性幹細胞)は、この多能性細胞から作製されます。多能性細胞は胚が子宮へ着床した後、原始外胚葉※2という細胞に分化します。その過程では、エピジェネティック※3状態と遺伝子発現の大規模な変動が起きるとされており、近年、幹細胞生物学の分野で注目されています。しかし、この分化過程を制御する因子については、大部分が未解明でした。
共同研究グループは、半世紀以上も前に報告された突然変異体で、この分化過程に異常を示す突然変異マウス「tw5※4」に着目し、原因遺伝子の同定、その働きや制御のメカニズム解明に挑みました。
変異マウスtw5は、大規模な染色体異常を持つため解析が困難でしたが、共同研究グループは、ゲノム解析や遺伝子改変技術を組み合わせてその困難を克服し、分化過程で異常をきたす原因遺伝子「Vps52」を突き止めました。Vps52は、酵母では細胞内の物質輸送を担うことが知られていましたが、哺乳類では細胞間相互作用を介して多能性細胞の分化や増殖を制御することを明らかにしました。また、分化に異常をきたすtw5変異胚のES細胞にVps52を導入すると分化が正常に進行したことから、Vps52はES細胞の分化を促進する能力があることも発見しました。
今後、ES細胞やiPS細胞(人工多能性幹細胞)の分化制御技術の開発、未解明な部分が多い多細胞生物における細胞内外の情報伝達メカニズム解明などに貢献すると期待できます。
本研究は、文部科学省特定領域研究「生殖系列の世代サイクルとエピゲノムネットワーク」、新学術領域研究「哺乳類初期発生の細胞コミュニティー」などの支援を受けて行われ、成果は米国の科学雑誌『Cell Reports』(11月29日号)に掲載されるに先立ち、オンライン版(11月8日付け:日本時間11月9日)に掲載されます。
背景
ヒトを含む哺乳類の成長過程において、子宮への着床はさまざまな細胞・組織への分化が始まる契機となる重要な出来事です。着床前後の胚には、将来の体全体を形成する元となる多能性細胞が存在します。着床前胚である胚盤胞※5には、内部細胞塊とよばれる細胞群があり、その中にある多能性細胞から、万能細胞であるES細胞が作製されることはよく知られています。
胚が子宮へ着床すると、多能性細胞は、多能性を保持したまま原始外胚葉へと分化していきます。この過程は、哺乳類発生における大きな節目で、細胞内ではエピジェネティック状態と遺伝子発現の大規模な変動が起きていると考えられています。しかし、この過程で働く遺伝子やその制御メカニズムについては、ほとんどが未解明でした。
共同研究グループは、半世紀以上前に報告されていた、この分化過程に異常を示すマウスの突然変異体「tw5」に着目しました。正常胚の多能性細胞は、着床後に増殖しながら内腔構造を形成しますが、tw5変異胚の多能性細胞は、それ自体の数が極端に少なく、内腔も形成されず、原始外胚葉への分化も起こりません(図1)。従って、着床後間もなく致死となります。tw5変異胚は、大規模な染色体逆位(染色体上の遺伝子の向きが逆転している)などの染色体異常を伴っています。逆位を持つため、正常な染色体とは交叉※6が起きないことなどから、正常な染色体の解析に使われる手法が適用できず、変異の原因遺伝子は不明のままでした。共同研究グループは、このtw5の詳細な解析を行い、多能性細胞の分化制御メカニズム解明の手がかりを得ようとしました。
研究手法と成果
共同研究グループは、原因遺伝子を含むゲノム領域を約750kb(75万塩基長)まで狭めた後、このゲノム領域をカバーする5種類のBACクローン※7を単離しました。これらを一つ一つtw5変異胚に導入し、どのBACクローンを導入すると致死表現型が回復するかを検討した結果、ある1つのBACクローンにより回復することを見つけました。このBACクローンは、なお16の遺伝子を含んでいたため、さらに分割して同様な導入実験を繰り返しました。最終的には20kb(2万塩基長)のゲノム領域にまで絞り込み、変異マウスtw5の原因遺伝子がVps52であることを突き止めました。さらに、正常胚のVps52のタンパク質コード領域では、グアニン(G)という塩基の繰り返しが9回あるのに対し、tw5変異胚では11回の繰り返しがあること、また、変異マウスtw5の復帰突然変異※8であるtw5G変異胚では、もう1個のGの挿入があって12回の繰り返しとなるため致死にならないことも見いだしました。また、Vps52を人為的に破壊した胚は、tw5変異胚と同様な多能性細胞の異常を示すことを確認したので、Vps52が変異マウスtw5の原因遺伝子であるという結論を得ました。
興味深いことに、変異胚で異常が認められる時期の多能性細胞ではVps52の発現は認められず、多能性細胞を包む臓側内胚葉※9で発現していることが分かりました。これは一見矛盾するようですが、Vps52が臓側内胚葉で働き、細胞間相互作用を介して多能性細胞の増殖や分化を促進するものと予測しました。これを検証するため、多能性細胞だけでVps52遺伝子を欠損する遺伝子改変マウス系統を作製し、その胚を調べたところ、tw5変異胚やVps52欠損胚が致死となる胎生6.5日ごろの段階を越えて、より後期の段階まで生存することが分かりました。しかしこの胚も、血管形成の異常などのため、胎生9.5日には致死となりました(図2)。これらの結果から、着床後すぐの段階では、Vps52は臓側内胚葉で発現して多能性細胞の発達を促し、さらに後期の段階になると多能性細胞に由来する組織でも発現し、血管などの組織の発達に必要な働きを持つことが分かりました。
また、tw5変異を持つES細胞の分化を誘導すると、細胞の集合塊が形成された後で分化が停止しますが、そこにVps52を導入すると、分化は正常に進行することも見いだしました(図3A、B)。さらに、tw5変異を持つES細胞と、Vps52を導入して正常となったtw5変異ES細胞を混ぜ、胚と類似した構造(胚様体)を形成すると、外側に位置する臓側内胚葉の層はVps52を導入した細胞で占められますが、内側の多能性細胞のほとんどはtw5変異のES細胞に由来しており、原始外胚葉によく似た細胞層を形成していました。この場合、胚様体は正常に発達できることが分かりました(図3C、D)。これらの結果から、Vps52は、ES細胞が分化するときも臓側内胚葉で発現し、細胞間相互作用を介して多能性細胞の分化や増殖を促進することが確認できました。
今後の期待
過去の酵母を用いた研究により、Vps52という遺伝子は、細胞内外の物質輸送を担うと考えられていました。しかし今回、哺乳類特有の機能として、あらゆる組織の元となる多能性細胞の増殖・分化に必須であり、その後の血管形成などの発生にも深く関わることを発見しました。これ以外にも、さまざまな組織や器官形成の重要な局面でVps52が機能している可能性があります。また、臓側内胚葉は、多能性細胞の発生に必須な信号を発信していることが知られており、Vps52がそれらの情報伝達に関わっていると考えられます。
今後は、今回使用したtw5変異マウス、復帰突然変異したtw5G変異マウス、原因遺伝子同定のために作製した変異マウスなどのバイオリソースを用いることで、哺乳類のさまざまな組織や器官形成のメカニズムとその情報伝達ネットワーク、単細胞生物である酵母と哺乳類の生命機能の比較、さらにはES細胞、iPS細胞などの分化操作技術の開発へと発展していくことが期待できます。
原論文情報
- Michihiko Sugimoto, Masayo Kondo, Michiko Hirose, Misao Suzuki, Kazuyuki Mekada, Takaya Abe, Hiroshi Kiyonari, Atsuo Ogura, Nobuo Takagi, Karen Artzt, and Kuniya Abe, "Molecular identification of tw5:Vps52 promotes pluripotential cell differentiation through cell-cell interactions", Cell Reports, 2012, doi. 10.1016/j.celrep.2012.10.004
発表者
理化学研究所
バイオリソースセンター 動物変異動態解析技術開発チーム
チームリーダー 阿部 訓也 (あべ くにや)
お問い合わせ先
筑波研究推進部企画課
Tel: 029-836-9058 / Fax: 029-836-9100
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.胚
胚子とも呼ぶ。発生過程の初期のステージにある個体を指し、マウスの場合、子宮の中で発達する。器官原基の形成が認められるステージ以降は胎仔(胎児)と呼ばれる。 - 2.原始外胚葉
着床後すぐの胚に存在する多能性細胞からなる細胞層。この細胞層からさらに外胚葉、中胚葉、内胚葉が作られ、将来の体全体が形成される。 - 3.エピジェネティック
DNAメチル化やヒストンアセチル化など、ゲノムに書かれた遺伝情報であるDNA塩基配列の変化を伴わずに、遺伝子発現を活性化したり、不活性化したりする化学反応とその周辺の学問領域を指す。エピジェネティックな化学修飾は、個体発生や細胞分化の過程で重要な役割を果たし、誤った化学修飾はさまざまな疾病をもたらす。 - 4.tw5
マウス17番染色体に位置する劣性の致死突然変異の1つ。ホモ胚は着床後すぐに原始外胚葉が形成されず致死となる。1957年に米国のD. ベネット博士、L.C. ダン博士が最初に報告した。 - 5.胚盤胞
卵割の終わった胚を指す。マウスの場合、受精後3.5日目の着床前胚を胚盤胞と呼ぶ。中空のボール状の構造をとり、胎児の元になる内部細胞塊(ICM)と、将来胎盤へ分化する1層の外側の細胞群(TE)に分かれている。 - 6.交叉
精子や卵子などの配偶子を形成する過程の減数分裂の際に起きる相同染色体間の部分的 な交換をいう。これにより、同一染色体上の遺伝子の組み合わせが変化し、遺伝的な多様性が生じる。逆位がある領域は相同部分のペアリングができないため、交叉は抑制される。 - 7.BACクローン
BACはBacterial Artificial Chromosome(細菌人工染色体)の略。100~200kb程度の比較的大きなサイズのDNAをクローン化するための技術であり、ゲノム解析によく用いられる。 - 8.復帰突然変異
突然変異により、正常な形質から変異表現型が生じるが、さらに突然変異が加わることにより、元の正常形質に復帰する場合がある。この2度目の変異を復帰突然変異と呼ぶ。 - 9.臓側内胚葉
着床後すぐの胚に存在する内胚葉系の細胞からなる細胞層。この細胞層は、内側の細胞への栄養や物質の供給、および細胞分化のための信号伝達に働くと考えられている。
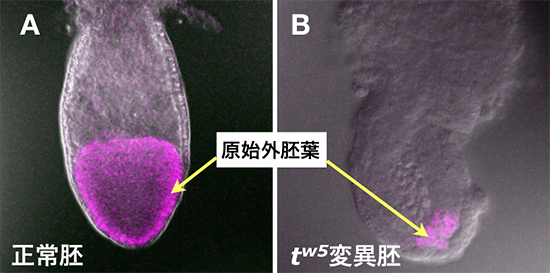
図1 tw5変異胚で見られる原始外胚葉の発達異常
受精後6.5日のマウス胚。正常胚(A)では、原始外胚葉(紫色の部分)が発達するが、tw5変異胚(B)では、原始外胚葉を構成する細胞が激減している。
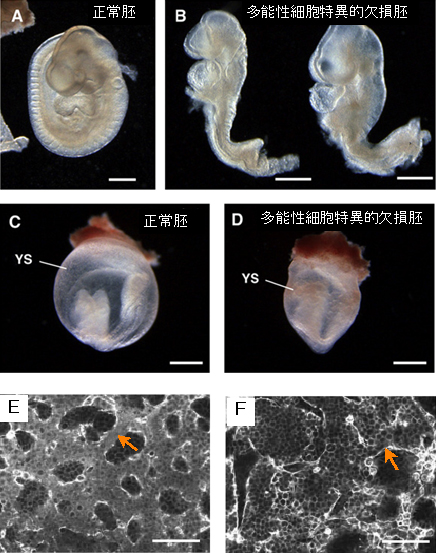
図2 多能性細胞特異的にVps52遺伝子を破壊したマウス胚の表現型
- A. 受精後9.5日の正常マウス胚
- B. 受精後9.5日の多能性細胞だけでVps52遺伝子を欠損させたマウス胚
- C. 2つの欠損胚(B)は、正常胚(A)と比較すると胚体の前半部は正常だが、後半部(B青矢印)に形態異常が認められる。受精後6.5日には致死となる通常のVps52欠損胚と異なり、多能性細胞特異的に欠損させた場合はより後期のステージまで発生することが分かる(スケールバーは0.5mm)。
- D. 受精後8.5日の正常マウス胚
- E. 受精後8.5日の変異マウス胚
- F. 変異マウス胚(D)では卵黄嚢(YS)に鬱血(うっけつ)を確認した(スケールバーは0.5mm)。
- G. 受精後9.5日の正常マウス胚の卵黄嚢
- H. 受精後9.5日の変異マウス胚の卵黄嚢
- I. 正常マウス胚の卵黄嚢では明瞭な血管構造を確認した(E矢印)が、変異マウス胚では確認できない(F矢印)(スケールバーは100μm)。
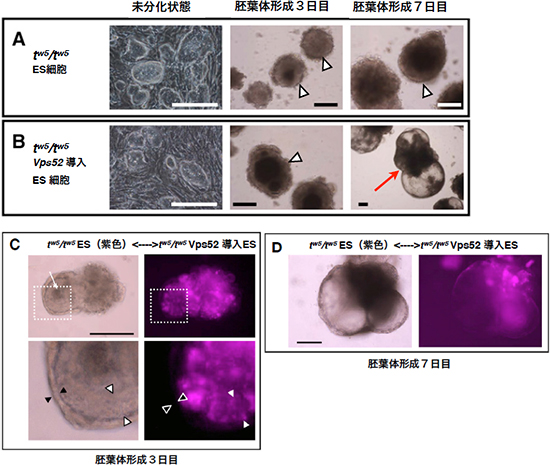
図3 ES細胞の分化・増殖を促進するVps52
- A.
tw5変異ES細胞の胚葉体形成
分化を誘導後3日目には集合塊(△)を作るが、その後の発達が見られず、7日目でも集合塊のままで分化が停止している(スケールバーは200μm)。 - B.
Vps52を導入した
tw5変異ES細胞の胚葉体形成
分化を誘導後3日目には集合塊(△)を作るが、Vps52導入により、それ以降の分化が促進され、7日目にはよく発達し、分化した胚葉体(矢印)が形成された(スケールバーは200μm)。 - C.
胚葉体形成3日目の細胞集合塊の光学顕微鏡(上段左)と蛍光顕微鏡画像(上段右)、および白点線枠内の拡大図(下段)
Vps52を導入して正常となった tw5変異ES細胞(正常細胞)と、紫色に蛍光標識した tw5変異ES細胞を混ぜて分化させると、正常細胞で占められた臓側内胚葉層(▲)が tw5変異ES細胞を取り囲んで存在し、内側の tw5変異ES細胞は原始外胚葉に似た構造(△)を作った(スケールバーは200μm)。 - D.
胚葉体形成7日目の細胞集合塊の光学顕微鏡(左)と蛍光顕微鏡画像(右)。
(C)の胚様体は、その後正常に発達し、分化細胞からなる胚葉体を形成した(スケールバーは200μm)。
