2012年12月13日
独立行政法人理化学研究所
細胞の維持に必須な微小管の最先端構造が明らかに
-光学顕微鏡の限界を超えたイメージング技術でとらえた新たな構造-
ポイント
- 超解像顕微鏡法と高精度の画像解析手法を駆使して25nmの分解能を達成
- 微小管最先端部に100nmにわたる新領域を開拓、2つのタンパク質の役割分担を解明
- 微小管の特定部位を標的とした副作用が少ない抗がん剤の開発へ期待
要旨
理化学研究所(野依良治理事長)は、超解像顕微鏡法※1を応用して25ナノメートル(nm)の分解能を実現し、細胞の中で物質輸送のレールとして働く微小管※2の先端に新しい構造領域とその機能を発見しました。これは、理研発生・再生科学総合研究センター(竹市雅俊センター長)光学イメージング解析ユニットの清末優子ユニットリーダーらと、オランダ・ユトレヒト大学のイリヤ・グリゴリエフ(Ilya Grigoriev)研究助手、米国・リーハイ大学のリン・カシメリス(Lynne Cassimeris)教授による共同研究グループの成果です。
細胞骨格※3は細胞内で繊維状の構造をしており、細胞の形や生理活動を維持するために必須です。そのネットワークは構築と崩壊を活発に繰り返し、細胞の形や機能を変化させて外部環境の変化に対応します。細胞骨格の1つである微小管は構造的に非対称で、その先端には多様な分子が結合してネットワークの構築と崩壊に寄与します。先端部のどこにどんな分子が結合するかを観察するには光学顕微鏡が欠かせませんが、従来の光学顕微鏡の分解能は200nmが限界で、詳細な構造は分かっていませんでした。
研究グループは、光学顕微鏡の限界を超える分解能100nmレベルの超解像顕微鏡法を用い、さらに、蛍光シグナルの最高輝度の位置を25nmの分解能で求める画像解析手法を導入しました。この手法で微小管先端構造を解析した結果、これまで最先端に結合していると考えられていたタンパク質EB1※4より100nm以上先端に、がん細胞で高発現するタンパク質ch-TOG※4が結合することを発見しました。さらに、ch-TOGが微小管ネットワーク全体の再配置を促すのに対して、EB1は微小管先端を細胞表層に結合させるという異なる役割を担っていることも分かりました。
微小管は細胞の増殖に必須なため、その阻害剤は抗がん剤にも利用されますが、副作用が強い、耐性細胞が出現して抗がん剤が効かなくなる、などの問題があります。今回、微小管の先端部には異なる機能を持つ分子が結合する多様な構造領域が存在し、最適な細胞骨格ネットワークを構築する仕組みが分かりました。今後、微小管の特定の部位を標的とした、副作用が低い抗がん剤の開発などへの応用が期待できます。
本研究は、総合科学技術会議の「最先端・次世代研究開発支援プログラム」により日本学術振興会を通して助成された「形態形成における微小管細胞骨格の役割の解析」と、上原記念生命科学財団により助成された「微小管プラス端動態制御因子群の機能解剖」などの一環として行われ、成果は米国のオンライン科学雑誌『PLOS ONE』(12月12日付け:日本時間12月13日)に掲載されます。
背景
体の中で、ある細胞が他の細胞たちと協調しながら細胞内外の情報を正確に伝えたり、その形や活動を決めたりするには、細胞の中の骨組みである細胞骨格の働きが重要です。細胞骨格は、異なる機能を持つ複数の構造体で形成されており、その中でも“微小管”は、細胞の中で物質輸送のレールとして機能します。微小管は、チューブリン※5というタンパク質が縦方向につながった13本の素繊維が側面で結合し、構造的に非対称性をもつチューブ状の中空構造を形成します。チューブリンの付加が活発な側は“プラス端”、反対側は“マイナス端”と呼ばれています(図1A)。ヒトの健康や病気に関わる多くの物質が微小管を伝って運ばれるため、微小管の正しい配置はヒトの健康維持に重要です(図1B)。研究グループはこれまでに、微小管のプラス端に結合するタンパク質集団「+TIPs※4」が、微小管の長さや配置の決定に重要な役割を果たすことを明らかにしてきました。微小管が伸長するとき、+TIPsは最先端に結合します。中でも、+TIPsの1つであるタンパク質EB1は、微小管先端に付加されたばかりのチューブリンだけに次々と結合するため、微小管の伸長に伴って、まるで彗星(すいせい)のように移動します(図2A、YouTube:EB1-GFPのタイムラプス動画(マウス繊維芽細胞)、 EB1-GFPのタイムラプス動画(マウス筋芽細胞))
一方、がん細胞で高発現するタンパク質ch-TOGも+TIPsに分類され、微小管の長さ調節に重要です。EB1もch-TOGも微小管の先端に結合しますが、これまで、それらの詳細な位置関係や役割分担は分かっていませんでした。また、微小管が伸長する様式も不明で、これまでの試験管内の解析から、「付加されたチューブリンがシート状になった後にファスナーを閉じるようにして中空構造になる」、「チューブリンが螺旋(らせん)状に付加されチューブ状を保ったまま伸長する」、「チューブリンがランダムに付加されながら各素繊維がばらばらに伸長する」、などの諸説があり、結論が出ていませんでした。特に、細胞内にある微小管の状態を詳細に観察する手段がありませんでした。これらを調べるには、分子ごとに違う色で染色し、超高解像度の顕微鏡を用いて、微小管先端の構造を細胞内部で直接観察するのが有効です。しかし、従来の光学顕微鏡では分解能200nmが限界とされていたため、さらなる分解能向上が求められていました。
研究手法と成果
研究グループは、近年開発された超解像顕微鏡法の1つ“構造化照明顕微鏡法(SIM)※1”を、微小管先端部の観察に用いました。SIMでは約100nmの分解能での解析が可能です。さらに、SIM画像をもとに、蛍光シグナルの最高輝度を25nmの分解能で求める画像解析手法を導入しました。実際に、ヒトの子宮頸(けい)がん由来の細胞であるHela細胞※6を用いて、EB1とch-TOG と微小管をそれぞれ違う色で染色し、微小管先端部分を超高解像度で解析しました。数百の画像を平均化した結果、ch-TOGはEB1よりも100nm以上先の部分に結合していることが分かりました(図2B、C)。つまり、これまで微小管の最先端に結合していると考えられていたEB1より約100nm以上微小管は突出しており、この未知の領域にch-TOGが結合していました。さらに、2012年にイギリスの研究グループが、EB1はチューブ状に閉じた素繊維の間に結合するという知見を得たことから(Maurer et al., Cell. 2012, 149, 371-382)、EB1よりも先の約100nmの領域では素繊維が閉じていないと予測できました(図3)。これは、微小管が伸長するとき、素繊維が閉じる前にチューブリンがランダムに付加されながら、各素繊維が異なる長さで伸長することを示唆しています。100nmという長さはこれまでに予想されていたよりもずっと長く、チューブリン2量体の約12個分にあたり、従来の微小管の伸長様式の諸説に貴重な知見を与えます。
さらに、サンプルの表面から約200nm以内の距離にある蛍光物質だけを可視化する“全反射顕微鏡※7”を用いて、細胞の表面近くに位置する微小管を詳細に観察しました。その結果、EB1は微小管先端を細胞表層に結合させて微小管を正しく配置させるのに対し、ch-TOGは微小管ネットワーク全体の再配置を促す効果を持つと分かりました。つまり、EB1とch-TOGは微小管の異なる場所に結合し、微小管に対して異なる役割を担っていました。
これらにより、微小管の先端で厳密に住み分けされた多様な分子は、微小管を正しく配置するように機能し、細胞外からの情報の正確な伝達と細胞の適切な生理活動に寄与すると考えられます。
今後の期待
今回、超解像顕微鏡技術と新しい画像解析手法を組み合わせて25nmの分解能を達成し、微小管先端部分に新たな構造を明らかにしました。今後、解析の自動化などで多くのデータを統合すると、解析精度の向上が見込まれます。この解析手法は、細胞骨格研究だけでなく、細胞膜や核などの構造研究や細胞接着研究など、さまざまな研究分野にも適用できます。
医療分野では、微小管は抗がん剤の標的とされています。そのため、タキソールをはじめとした微小管阻害剤が抗がん治療に用いられてきました。しかし、副作用の強さや薬剤耐性細胞の出現などの問題があり、新たな抗がん剤の開発が必要です。今後、微小管に関する知見を積み重ねることで、副作用の少ない、特定な領域を標的にした抗がん剤候補分子の選定などに貢献すると期待できます。
原論文情報
- Satoko Nakamura, Ilya Grigoriev, Taisaku Nogi, Tomoko Hamaji, Lynne Cassimeris, Yuko Mimori-Kiyosue "Dissecting the nanoscale distributions and functions of microtubule-end-binding proteins EB1 and ch-TOG in interphase HeLa cells"
PLOS ONE 2012, doi: 10.1371/journal.pone.0051442
発表者
理化学研究所
発生・再生科学総合研究センター 光学イメージング解析ユニット
ユニットリーダー 清末 優子(きよすえ ゆうこ)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.超解像顕微鏡法、構造化照明顕微鏡法(SIM)
超解像顕微鏡法とは、光学顕微鏡の分解能を上回る高解像度情報を得る手法の総称。光学顕微鏡では、光の波長程度より高い分解能(異なる2点を分離して検出できる限界)を得られず、その限界は約200nmとされてきた。この限界を超えるため、異なる原理による超解像顕微鏡法が開発されている。蛍光標識した試料を1分子レベルで検出し、その中心位置を求める方法「PALM/STORM」、蛍光の発生場所を小さく絞って分解能を向上させる「STED」、励起光を照射する領域を精密にパターン化して制限し、高分解情報を抽出する「構造化照明顕微鏡法(structured illumination microscopy: SIM)」などがある。 - 2.微小管
細胞骨格の1つ。細胞の骨組みとして細胞の形態維持や変形に必要である。キネシンやダイニンを含むモータータンパク質による能動輸送のレールとして機能するため、分子や液胞などの移動の足場、細胞分裂の時には紡錘体を形成し染色体の移動を担っている。α/β-チューブリン2量体が縦方向に重合した13本の素繊維が筒状に束ねられて形成される直径約25nmの繊維状構造をとる。微小管には構造的に非対称なプラス端とマイナス端の“向き”があり、この向きを利用してモータータンパク質が物質を正しい方向に運ぶ。細胞の中では微小管の向きと場所が正しく配置されて、適切な物質輸送が可能となる。 - 3.細胞骨格
細胞内に張り巡らされている繊維状の構造の総称。アクチンや微小管などがその代表。細胞の運動、分裂などさまざまな機能を担っている。小さな単位が一定の方向性を持って重合・脱重合することにより、常に動的不安定性を保っている。この動的不安定性が機能発現に重要。 - 4.EB1、ch-TOG、+TIPs
+TIPs(微小管プラス端集積因子)とは、微小管のプラス端に結合する分子の総称で、微小管のプラス端先端に結合する。+TIPsに分類されるタンパク質は多数あるが、その中でEB1(end-binding 1)は直接微小管先端に結合し、他の多くの+TIPsを微小管先端に集める中心的な分子。ch-TOG(colonic and hepatic tumor over-expressed gene)は、がん細胞で高発現しているタンパク質として同定された推定がん遺伝子で、この分子も微小管先端に直接結合できることが報告されている。 - 5.チューブリン
真核生物の細胞内にあるタンパク質で、微小管や中心体の構成成分。チューブリンは規則正しく重合して微小管を形成する。微小管形成は細胞分裂にも密接に関与しており、がん細胞の増殖の標的となるため、チューブリン阻害剤は抗がん剤としても用いられている。 - 6.Hela細胞
世界で初めて樹立されたヒトの細胞株(生体外で一定の性質を持って長期間培養できる細胞)。子宮頸(けい)がん由来の細胞で、世界中でさまざまな研究に利用されている。名前は、患者である黒人女性の名前(Henrietta Lacks)に由来する。 - 7.全反射顕微鏡
標本のガラス表面から200nm程度の深さだけを照射する顕微鏡法。励起光をカバーガラスの表面で全反射する角度で入射すると、ガラスの反対側に特殊な光(エバネッセント光)が染み出す現象を利用している。背景にある物質からの信号が発生しないため、表面からごく限られた深度にある蛍光物質を超高感度に観察することができる。
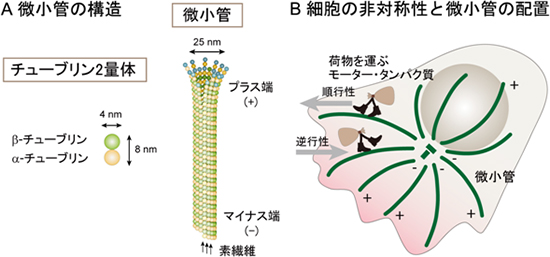
図1 微小管の構造と物質輸送
- A: 微小管は、チューブリン2量体が縦方向につながった13本の素繊維が、チューブ状に束ねられた直径約25nmの繊維状構造である。チューブリンの構造に依存して、微小管にはプラス側とマイナス側の向きがあり、チューブリンの付加と離脱は主にプラス端側で起こる。
- B: 微小管の向きは、微小管依存性のモータータンパク質の移動方向を決める。順行性、逆行性のモータータンパク質が正しい方向に荷物を運ぶために、微小管は正しい向きに配置される必要がある。
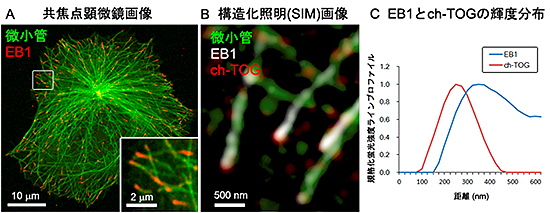
図2 微小管プラス端集積因子(+TIPs)の局在
- A: HeLa細胞での、+TIPsの中心的分子EB1(赤)と微小管(緑)の蛍光免疫染色画像。微小管先端の挙動や配置を決めるため、+TIPsは重要な働きをし、特にEB1は、微小管の先端だけに結合する。生きた細胞の中で標識したEB1をコマ送りでみると、EB1は微小管が伸長する間だけその先端に集まるため、まるですい星のように見える(YouTube:EB1-GFPのタイムラプス動画(マウス繊維芽細胞)、EB1-GFPのタイムラプス動画(マウス筋芽細胞))。
- B: SIMを用いて撮影した、微小管(緑)、EB1(白)、ch-TOG(赤)の染色像。ch-TOGのシグナルが、EB1よりも先端に見られる。
- C: EB1とch-TOGのシグナルの輝度分布を、微小管に沿って先端から後方に向けて解析し比較した例。ch-TOGの輝度のピークが、EB1のピークよりも約100nm先にある。
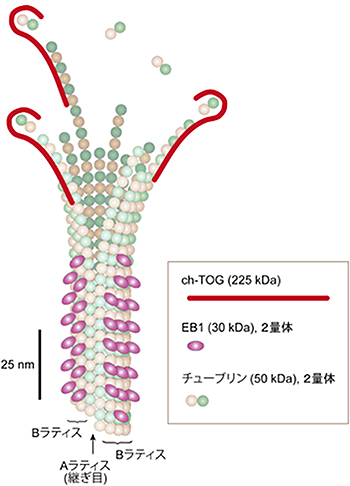
図3 伸長する微小管先端の構造
EB1とch-TOGの結合場所と、これにより予測した伸長する微小管先端の構造を示した。ch-TOGが伸長する素繊維の最先端に結合するのに対し、EB1は閉じた素繊維の間に結合する。これにより、微小管の最先端部には、閉じていない素繊維がおよそ100nm(約12個のチューブリン2量体からなる)にわたって突出していることが明らかになった。EB1とch-TOGは、異なる微小管領域を認識し結合して、微小管先端の挙動に異なる作用を及ぼす。
