ポイント
- 脳に発現する糖転移酵素GnT-IXを欠損したマウスで再ミエリン化が促進
- GnT-IXが作る分岐型O-マンノース糖鎖がアストロサイトの活性化を制御
- 分岐型O-マンノース糖鎖合成を阻害するような新規脱髄治療薬の開発に期待
要旨
理化学研究所(理研、野依良治理事長)は、脳に発現する糖転移酵素「N-アセチルグルコサミン転移酵素IX(GnT-IX)[1] 」が作る分岐型O-マンノース糖鎖[2]が脱髄[3]を進行させることを発見し、この糖鎖が多発性硬化症[4]をはじめとする脱髄疾患治療のための新たなターゲットになる可能性を示しました。これは、理研グローバル研究クラスタ(玉尾皓平クラスタ長)理研-マックスプランク連携研究センターシステム糖鎖生物学研究グループ(谷口直之グループディレクター)疾患糖鎖研究チームの兼清健志(かねきよけんじ)協力研究員、北爪しのぶ副チームリーダーらと、東北薬科大学分子生体膜研究所機能病態分子学教室の稲森啓一郎准教授ら、放射線医学総合研究所分子・イメージング研究センター脳分子動態チームの樋口真人チームリーダーら、および高知大学医学部生化学講座の本家孝一教授らとの研究グループによる成果です。
脱髄疾患は、神経を覆っているミエリン[5]が消失し(脱ミエリン化[5])、神経信号がうまく伝達できなくなるため、四肢のしびれなどさまざまの神経症状が出る原因不明の難病です。病気の進行には脳内に存在するアストロサイト[6]などの細胞の活性化が関わっています。脱ミエリン化を抑制し、再ミエリン化[5]を促すことが治療の鍵とされています。
研究グループは、2003年に自らが発見した糖転移酵素GnT-IXが作る分岐型O-マンノース糖鎖に着目し、まずGnT-IXを欠損させた「GnT-IX欠損マウス」を作製しました。次に野生型マウスとGnT-IX欠損マウスそれぞれにクプリゾン[7]を投与し、人為的に脱髄を進行させて両者を比較、解析しました。その結果、クプリゾン投与により野生型は脱髄が進行したのに対し、GnT-IX欠損マウスは脱髄が軽症化し、再ミエリン化が促進されました。さらに、細胞レベルで解析した結果、分岐型O-マンノース糖鎖は主に活性化アストロサイトに発現しており、野生型ではアストロサイトの活性化が強く起っていたのに対し、GnT-IX欠損マウスでは活性化が抑制されることが分かりました。今回の研究成果に加え、GnT-IX欠損マウスが通常の飼育条件で正常に発育することを考えると、GnT-IX阻害剤が脱髄疾患の新たな治療薬候補になると期待できます。
本研究成果は、米国の科学雑誌『J Neurosci』オンライン版(6月12日付け:日本時間6月13日)に掲載されました。
背景
中枢神経系の髄鞘(ずいしょう)(ミエリン鞘)[8]は、オリゴデンドロサイト[9]からなり、神経細胞の軸索を覆い、神経信号の高速伝達に重要な役割を果たしています(図1)。多発性硬化症などの脱髄疾患では、ミエリンが消失し(脱ミエリン化)、修復機構である再ミエリン化が障害されています。したがって、脱髄疾患の治療には脱ミエリン化を抑制することだけでなく、再ミエリン化を促進することが重要です。この再ミエリン化の実体は、未成熟なオリゴデンドロサイト前駆細胞がミエリンを産生できる成熟したオリゴデンドロ細胞へ分化することですが、脱髄の過程で活性化されるアストロサイトが間接的にオリゴデンドロサイトの分化を抑制するという報告もあります。このように、複数の細胞によって複雑に制御されていると考えられる脱ミエリン化と再ミエリン化の制御機構には不明な点が多く残されています。
一方で、ポリシアル酸などの脳に特異的に発現する糖鎖が脱髄を制御していることが分かってきました。糖鎖は糖転移酵素によって合成されますが、特定の糖鎖が脱ミエリン化、あるいは再ミエリン化を制御していることが分かれば、その糖転移酵素の阻害剤もしくは促進剤が新たな治療のターゲットとなり得ます。
そこで今回、研究グループは脳だけに発現する糖転移酵素「N-アセチルグルコサミン転移酵素IX(GnT-IX)」を欠損させた「GnT-IX欠損マウス」を作製し、糖鎖による脱ミエリン化/再ミエリン化の制御機構の解明に挑みました。
研究手法と成果
野生型とGnT-IX欠損マウスそれぞれに銅のキレート化合物[10]のクプリゾンを投与し、人為的に脱髄を進させて両者を比較、解析しました。その結果、野生型マウスではクプリゾン投与により脱髄が時間経過とともに進行しましたが、GnT-IX欠損マウスでは一度脱髄が起った後で、髄鞘が顕著に回復していました(図2)。つまりGnT-IX欠損マウスでは再ミエリン化が促進されていました。
また、細胞レベルで解析したところ、糖転移酵素GnT-IXが作る分岐型O-マンノース糖鎖は主に活性化アストロサイトに発現しており、野生型マウスでは活性化が強く起っていたのに対して、GnT-IX欠損マウスでは活性化が抑制されていました。活性化アストロサイトは再ミエリン化を阻害することが報告されていますが、アストロサイトの活性化が抑制されているGnT-IX欠損マウスでは、再ミエリン化の実体であるオリゴデンドロサイト前駆細胞から成熟オリゴデンドロサイトへの分化が増加していました。
さらに、生化学的な実験から、GnT-IXが糖鎖を付加するタンパク質の1つが、受容体型チロシンホスファターゼβ(RPTPβ)[11]であることも分かりました。野生型では分岐型O-マンノース糖鎖がRPTPβに付加されていましたが、GnT-IX欠損マウスでは非分岐型O-マンノース糖鎖がRPTPβに付加されていました。これはGnT-IXが欠損したことにより糖鎖が分岐できなくなったためです。また、非分岐型O-マンノース糖鎖は細胞膜の脂質ラフト[12]という領域に多く存在していました。
これらの結果から、GnT-IX欠損マウスではO-マンノース型糖鎖の分岐の欠損により、アストロサイトの活性化が抑制され、それに伴いオリゴデンドロサイト前駆細胞から成熟オリゴデンドロサイトへの分化が促進されるため、再ミエリン化が亢進したと考えられます(図3)。
今後の期待
現在、脱髄疾患の治療のターゲットとして、一度起った脱髄部分を回復させる再ミエリン化の過程(オリゴデンドロサイト前駆細胞から成熟オリゴデンドロサイトへの分化)を促進するような薬剤の開発が求められています。今回、脳特異的な糖転移酵素GnT-IXが作る分岐型O-マンノース糖鎖が、アストロサイトの活性化を介して再ミエリン化の阻害因子として働いている可能性が示されたため(図3)、今後、GnT-IXの阻害剤、特にアストロサイト特異的な阻害剤を探索することで、間接的に再ミエリン化を促進する新規治療薬の開発が期待できます。
原論文情報
- Kanekiyo, K, Inamori, K, Kitazume, S, Sato, K, Maeda, J, Higuchi, M, Kizuka, Y, Korekane, H, Matsuo, I, Honke, K, Taniguchi, N. "Loss of branched o-mannosyl glycans in astrocytes accelerates remyelination." J Neurosci 2013;33(24):10037-47.
発表者
理化学研究所
グローバル研究クラスタ 理研-マックスプランク連携研究センター システム糖鎖生物学研究グループ 疾患糖鎖研究チーム
副チームリーダー 北爪 しのぶ (きたづめ しのぶ)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.N-アセチルグルコサミン転移酵素IX (GnT-IX)
糖鎖の生合成はさまざまな糖転移酵素によって、1つずつ糖を付加することにより行われているが、一群の糖転移酵素の中でもN-アセチルグルコサミンを転移することで、特にO-マンノース型の糖鎖に分岐を作る役割を担っている酵素。 - 2.分岐型O-マンノース糖鎖
マンノースを介してタンパク質に結合している糖鎖(O-マンノース型糖鎖)のうち、そのマンノースにN-アセチルグルコサミンが2つ結合して枝分かれした構造をとっているもの。 - 3.脱髄
神経細胞には軸索と呼ばれる突起があり、それがほかの神経細胞に繋がって細胞間の情報(神経信号)をやり取りしている。通常は軸索が髄鞘(ミエリン鞘)と呼ばれる絶縁体に覆われて保護されていることで、正常に情報が伝達されているが、さまざまな原因によりこの髄鞘が破壊されることを脱髄と言う。脱髄が起ると正常な情報伝達ができなくなり、しびれや麻痺を引き起こす。 - 4.多発性硬化症
脱髄疾患の一種で、脳や脊髄、視神経などに神経症状が出て、治癒と再発を繰り返すことが知られており、日本では特定疾患に認定されている原因不明の難病。 - 5.ミエリン、脱ミエリン化、再ミエリン化
ミエリンは髄鞘(ミエリン鞘)を形成する脂肪性の物質で、それが破壊されることを脱ミエリン化と言う。再ミエリン化は、一度破壊された髄鞘が修復されることを言う。 - 6.アストロサイト
脳の細胞のうち神経細胞以外の細胞をグリア細胞と呼ぶが、アストロサイトはそのグリア細胞の1つである。通常時は神経細胞に栄養を供給したり、脳内に異物が入らないように血液脳関門として機能している。脱髄疾患においては、脱髄の進行に関わっている。 - 7.クプリゾン
銅のキレート化合物で、経口投与すると髄鞘を形成しているオリゴデンドロサイトにのみダメージを与え、結果的に脱髄を引き起こす。 - 8.髄鞘(ミエリン鞘)
グリア細胞の中でも、オリゴデンドロサイトが神経細胞の軸索に巻き付いて形成している絶縁性の物質。神経細胞が正常に情報を伝達するのに不可欠な構造である。 - 9.オリゴデンドロサイト
神経細胞の軸索に巻き付いて、髄鞘(ミエリン鞘)を形成するグリア細胞。神経細胞の正常な機能維持に寄与している。 - 10.キレート化合物
金属イオンをと結合し、金属イオンの作用をなくしてしまう物質。 - 11.受容体型チロシンホスファターゼβ(RPTPβ)
細胞の増殖や移動、細胞同士のコミュニケーションはタンパク質の特定のチロシン部分のリン酸化修飾によってコントロールされている。チロシン部分にリン酸基をつける酵素をチロシンキナーゼというのに対して、リン酸基を外す酵素をチロシンホスファターゼと呼んでいる。RPTPβは、一連のチロシンホスファターゼ群の中でも神経系に発現しており、脱髄に関わる受容体型の分子である。 - 12.脂質ラフト
ラフトとは筏(いかだ)の意味。タンパク質が密に集まることでその機能を発揮する場所が細胞の脂質膜上に筏が浮かぶように存在することから脂質ラフトと呼ばれている。つまり、脂質膜上の機能ドメインである。
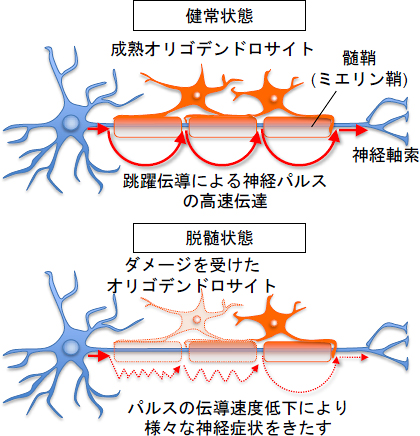
図1 正常時と脱髄時の神経信号の伝達
- 上: 中枢神経系の髄鞘(ミエリン鞘)はオリゴデンドロサイトからなり、神経細胞の軸索を覆っており、神経信号の高速伝達に重要な役割を果たしている。
- 下: 脱髄疾患ではミエリンが消失し(脱ミエリン化)、神経信号の伝達が低下するために四肢のしびれなど、さまざまな神経症状をきたす。
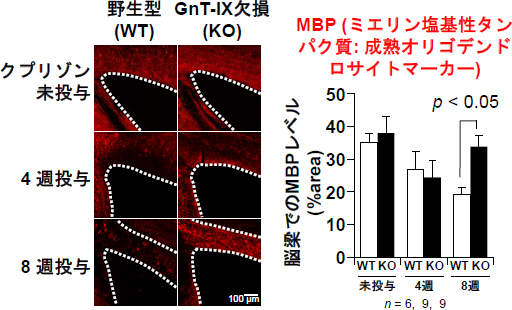
図2 免疫組織染色による野生型マウスとGnT-IX欠損マウスの脱髄の比較
野生型(WT)およびGnT-IX欠損(KO)マウスに脱髄刺激を与えた後に、脳切片を作製し、髄鞘を形成する細胞であるオリゴデンドロサイトを免疫組織染色した(赤)。点線は髄鞘の豊富な神経線維が密集している脳梁の境界。野生型マウスでは脱髄刺激によってオリゴデンドロイトの染色性がだんだん減少していった。一方、GnT-IX欠損マウスでは、刺激8週目にオリゴデンドロサイトの染色性が顕著に回復しているのが分かる。
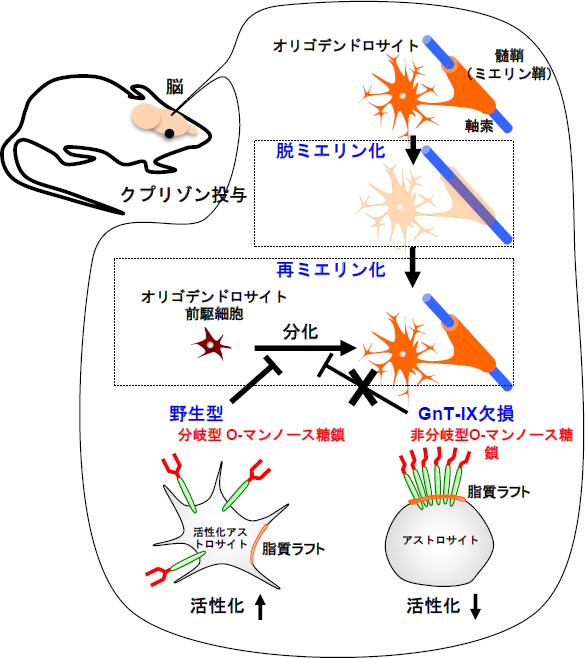
図3 GnT-IXが再ミエリン化を調節する推定モデル
GnT-IX欠損マウスは分岐型の糖鎖を作ることができないため、O-マンノース型糖鎖の分岐が欠損する。その結果、アストロサイトの活性化が抑制され、オリゴデンドロサイト前駆細胞から成熟オリゴデンドロサイトへの分化が促進され、再ミエリン化が亢進する考えられる。
