ポイント
- Meis2遺伝子に着目しポリコム複合体による遺伝子の発現制御の仕組みを解明
- 遺伝子発現は染色体の高次構造に依存している
- ポリコム複合体が染色体の高次構造を変化させ、遺伝子発現活性化にも関与
要旨
理化学研究所(理研、野依良治理事長)は、マウスの胚を用い、遺伝子の発現を抑制すると考えられてきた「ポリコム複合体[1]」が、遺伝子発現の活性化にも関わっていることを明らかにしました。これは、理研統合生命医科学研究センター(小安重夫センター長代行)免疫器官形成研究グループの近藤隆研究生、古関明彦グループディレクター(副センター長)らの研究グループの成果です。
細胞が未分化の状態から特定の細胞へと分化する運命決定には、どの遺伝子がいつどこで発現(オン)するか、あるいは抑制(オフ)するかといった遺伝子発現の切り換えが深く関わっています。この遺伝子発現のオン・オフの切り換えを管理しているのが、ポリコムタンパク質群です。ポリコムタンパク質群は、その標的となる遺伝子の特定の領域で、巨大なポリコム複合体を形成し、標的遺伝子の発現を抑制することが知られていました。しかし、ポリコム複合体が遺伝子のどの領域に結合し、遺伝子発現を制御しているのかなど、詳細な分子メカニズムは解明されていませんでした。
研究グループは、中脳の形成に重要なMeis2[2]という遺伝子に着目して、ポリコム複合体による遺伝子の発現制御の仕組みを調べました。その結果、ポリコム複合体は、Meis2が不要な時期には、遺伝子転写に必要な領域「プロモーター[3]」と遺伝子の抑制制御領域「サイレンサー[4]」に結合し、Meis2の発現を抑制していることが分かりました。また一方で、Meis2が必要な時期がくると、ポリコム複合体が染色体の高次構造[5]を変化させて、遺伝子の転写活性化領域「エンハンサー[6]」をプロモーターに引き寄せ、遺伝子発現を活性化していることが明らかになりました。
これは、ポリコム複合体が、遺伝子の発現を抑制すると同時に、活性化する役割も担っていることを示唆しています。
本研究成果は、米国の科学雑誌『Developmental Cell』(2014年1月13日号)に掲載されるに先立ち、オンライン版(12月26日付け:日本時間12月27日)に掲載されました。
背景
細胞が未分化の状態から特定の細胞へと分化する運命決定には、どの遺伝子がいつどこで発現(オン)するか、あるいは抑制(オフ)するかといった遺伝子発現の切り換えが深く関わっています。未分化の細胞が、さまざまな細胞へと分化するための多能性を維持するには、分化に関連する遺伝子が活性化できる性質を保ちながらも実際には不活性な状態にとどまっている必要があります。同時に、必要な時期がきたら、必要な細胞において、遺伝子を活性化できるようにしておくことで、正常な個体発生が可能になります。
このような遺伝子発現のオン・オフ機能を維持するために、重要な役割を果たしているのがポリコムタンパク質群です。ポリコムタンパク質群は巨大な「ポリコム複合体」を形成し、細胞の分化や増殖抑制に関わる遺伝子に結合して、その遺伝子発現を抑制することが報告されています。しかし、ポリコム複合体がどのように遺伝子発現を抑制し、また、どのようにその抑制を解除するのかなど詳細な分子メカニズムは、ほとんど解明されていませんでした。
研究グループは、これまでに、ポリコム複合体が重合して染色体の高次構造を変化させ、遺伝子発現のオン・オフに関わることを報告してきました※。しかし、ポリコム複合体が遺伝子のどの領域に結合し遺伝子発現を制御しているのか、といった詳細なメカニズムの解明には至っていませんでした。
※2013年10月1日プレスリリース「細胞の運命を左右する新しい分子メカニズムの一端を解明」
研究手法と成果
研究グループは、Meis2という遺伝子に着目して、ポリコム複合体による遺伝子発現の制御メカニズムを調べることにしました。Meis2は、発生のさまざまな場面で重要な役割を果たす転写調節因子の1つで、特に中脳の形成に重要なことが知られています。そこで、マウスの胚を用い、中脳を形成する細胞へと分化する未分化細胞において、Meis2の発現を調節する領域同士の相互作用を最新の分子生物学的手法や細胞生物学的手法を使い解析しました。今回、使用した手法の1つ「Immuno-FISH(immunohistochemistry and FISH)」は、タンパク質とDNA断片の相互作用を、組織切片において同時に可視化できる手法で、研究グループが独自に開発したものです。
解析の結果、Meis2が発現しないときは、ポリコム複合体が遺伝子の転写に必要な領域「プロモーター」に結合しているのに対し、Meis2が発現する時期が近づくと、ポリコム複合体がプロモーターから離れていました。このことから、ポリコム複合体は、Meis2のプロモーターに結合して遺伝子発現を調節していることが分かりました。
次に、プロモーターに加え、Meis2の「サイレンサー(抑制制御領域)」と「エンハンサー(転写活性化領域)」について、ポリコム複合体との結合や立体的な位置関係を解析しました(図1)。その結果、ポリコム複合体は、Meis2が不要な時期には、サイレンサーとプロモーターに結合し、遺伝子発現を抑制していることが分かりました(図1の6.5日胚)。一方、Meis2が必要な時期の直前に(図1の16体節以降)、ポリコム複合体が染色体の高次構造を変化させて、エンハンサーを引き寄せており、この過程においても、ポリコム複合体が必要なことが分かりました。染色体の高次構造の変化の結果として、エンハンサーがサイレンサーとポリコム複合体をプロモーターからはじき出し、Meis2の発現を活性化することが分かりました(図2)。このように、Meis2の発現は、染色体の高次構造に相関しており、その調節をポリコムタンパク質群からなるポリコム複合体が行なっていることが明らかになりました。
今後の期待
今回の研究により、ポリコム複合体が遺伝子発現の抑制を担うだけでなく、発現の活性化も制御していることが分かりました。しかし、遺伝子の発現抑制や活性化において、ポリコム複合体がどのようにサイレンサーやエンハンサーといった転写調節領域をプロモーターに引き寄せるのか、どうやってエンハンサーがポリコム複合体とサイレンサーをプロモーターからはじき出すのかなど、未解決の謎が多く残されています。
このような遺伝子の発現調節メカニズムは、細胞の正常な分化・脱分化の過程の解明、ES細胞(胚性幹細胞)やiPS細胞(人工多能性幹細胞)の分化のコントロールなど、発生にかかわるさまざまな面で大変重要です。また、細胞のがん化や、がん細胞の抑制制御などにおいても、発現調節機構の解析が重要と考えられ、今回の成果がこれらの課題の解決につながるものと期待できます。
原論文情報
- Takashi Kondo, Kyoichi Isono, Kaori Kondo, Takaho A. Endo, Shigeyoshi Itohara, Miguel Vidal, and Haruhiko Koseki. Polycomb potentiates Meis2 activation in midbrain by mediating interaction of the promoter with a tissue-specific enhancer. Developmental Cell, 2014, http://dx.doi.org/10.1016/j.devcel.2013.11.021.
発表者
理化学研究所
統合生命医科学研究センター 免疫器官形成研究グループ
研究生 近藤 隆(こんどう たかし)
グループディレクター 古関 明彦(こせき はるひこ)
お問い合わせ先
統合生命医科学研究推進室
Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ポリコム複合体
ショウジョウバエで見いだされた一群のクロマチン因子。ホメオティック遺伝子群の調節因子として発見されたが、後にDNAが巻き付いているタンパク質「ヒストン」のメチル化、ユビキチン化の活性を有することが分かり、遺伝子の発現を抑制することが知られている。 - 2.Meis
myeloid ecotropic insertion siteの略で、白血病の原因遺伝子の1つとして発見された。ショウジョウバエにおけるホメオティック遺伝子群( Hox)のコファクターとして知られる homothoraxのホモログで、TALE(three amino acid loop extension)ホメオボックス遺伝子で、転写調節因子の1つ。近年、 Hox遺伝子群以外の多くの転写調節因子(HLH、Znフィンガーなど)とも複合体を形成することが判明した。哺乳動物には Meis1、 2、 3が存在する。 - 3.プロモーター
遺伝子の転写開始点を含む転写開始に必須なDNA領域。 - 4.サイレンサー
遺伝子の発現抑制を担っているDNA領域。 - 5.染色体の高次構造
染色体は、2本鎖のDNAからなる巨大分子であり、核分裂静止期においては、直径5~10μmの核の中に詰め込まれている。DNA配列は一次元的な情報であるが、核の中では、配列上遠く離れているDNA領域が三次元的に近傍に位置していることもある。それを染色体高次構造と呼んでいる。 - 6.エンハンサー
遺伝子の転写を活性化する際に必要なDNA領域。真核生物においてはプロモーターとは離れて存在することも多い。
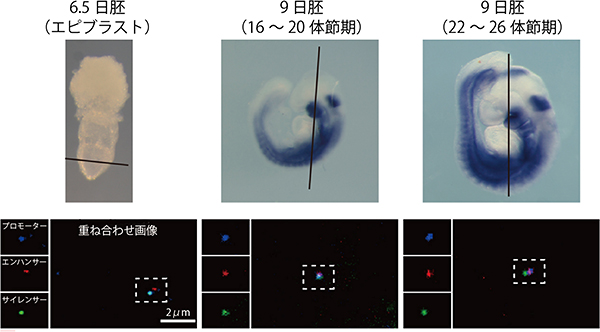
図1 中脳の発生に伴うMeis2の発現と各DNA領域の立体での位置変化
- 上: マウス胚でのMeis2の発現領域。青く染まった領域は、Meis2遺伝子が発現していることを示す。6.5日胚ではMeis2の発現はなく、9日胚の22体節期に中脳での発現が始まる。線は切片作成の際の切断面を示す。
- 下: 6.5日胚のエピブラスト(将来、胎児本体を形成する細胞群)、16から20体節期の中脳、22体節期以降の中脳での組織切片。青がプロモーター、赤がエンハンサー、緑がサイレンサー。6.5日胚ではMeis2が発現しておらず、サイレンサーがプロモーターと結合している。16から20体節期には、Meis2の発現はまだ見られないが、一時的にプロモーター、エンハンサー、サイレンサーの3つが結合している。発現が活性化されている22体節以降には、エンハンサーがプロモーターに作用し、サイレンサーは外れている。
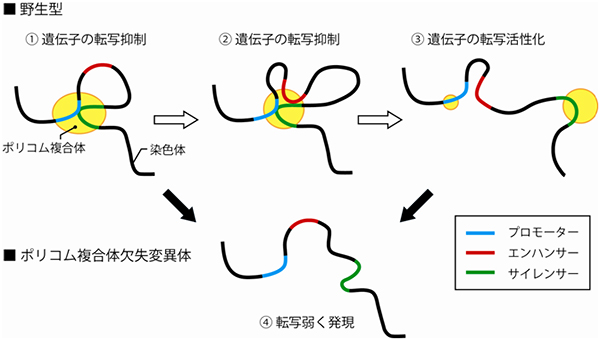
図2 ポリコム複合体と染色体高次構造の変化モデル
- ① Meis2が必要でない時期は、ポリコム複合体は、プロモーターとサイレンサーに結合しており、そのプロモーターとサイレンサーは立体的に近傍に存在する。
- ② その後、Meis2発現開始直前になると、ポリコム複合体が染色体の高次構造を変化させ、エンハンサーが引き寄せられ、一時的にプロモーター、エンハンサー、サイレンサー、ポリコム複合体の4つが集合する。
- ③ サイレンサーとともにポリコム複合体がプロモーターから外れていく。このため、エンハンサーの働きにより、Meis2の転写活性化が起こる。
- ④ また、遺伝子変異によって、ポリコム複合体が存在しない状態においては、染色体はいずれの高次構造もとることができず、遺伝子は発現の抑制も活性化も受けることが不可能となり、弱く発現し続ける状態になる。
