ポイント
- 大脳嗅内皮質-海馬間で新規の神経回路を発見
- 新規の神経回路は記憶の連結と分離を調整する
- アルツハイマー病や精神神経疾患メカニズムの解明に貢献
要旨
理化学研究所(理研、野依良治理事長)は、脳の記憶形成の中枢である大脳嗅内皮質[1]-海馬[2]間において、記憶の連結と分離を調節する新たな神経回路を発見しました。これは、理研脳科学総合研究センター(BSI、利根川進センター長)RIKEN-MIT神経回路遺伝学研究センター利根川研究室の北村貴司研究員、ミケレ・ピグナテーリ(Michele Pignatelli)研究員、ジャンヒュップ・スー(Junghyup Suh)研究員、小原圭吾研究員、利根川進センター長(米国マサチューセッツ工科大学、CNCGディレクター)と、理研バイオリソースセンターの吉木淳コーディネーター、阿部訓也副センター長らの共同研究グループの成果です。
私たちはさまざまな出来事に出合い、それらを記憶しています。この記憶には「何が」、「どこで」、「いつ」という情報が含まれます。この記憶の形成には、大脳嗅内皮質-海馬間の神経回路が関わっていることが知られています。「何が」、「どこで」については脳の中でどう統合され、記憶されていくかのメカニズムが解明されつつあるものの、「いつ」については、近年になって研究が進んできたという状況です。2011年に利根川研究室は、数秒から数十秒離れた2つの出来事を1つのエピソードとして記憶するには大脳嗅内皮質Ⅲ層[1]の神経細胞から海馬のCA1領域[2]への直接入力が必要であることを報告しています。しかし、時間的に離れすぎている2つの出来事までは連結して記憶する必要がありません。記憶するのか記憶しないのか?時間的に離れた2つの出来事の連結と分離を脳がどう調節しているのかは全く知られていませんでした。
今回、共同研究グループは、大脳嗅内皮質Ⅱ層[1]に内包されている細胞集団「アイランドセル[3]」を発見しました。アイランドセルは海馬の抑制性神経細胞を介して大脳嗅内皮質Ⅲ層の海馬への入力を抑制することから、アイランドセルを活性化すると、連結すべき2つの出来事が連結できなくなり、また、アイランドセルを抑制すると本来は連結すべきでない2つの出来事が1つのエピソードとして記憶されました。
本研究によって、記憶形成にも調節機構が神経回路レベルで存在することが明らかになりました。この成果は、記憶に関わる脳内の神経活動や、さまざまな神経系変性疾患、精神神経疾患のメカニズム解明につながると期待できます。
本研究成果は、米国の科学雑誌『Science』(日本時間2月21日付け)及びオンライン版(日本時間1月23日付け)に掲載されました。
背景
私たちは、日々の生活の中でさまざまな出来事に遭遇し、それを覚えます。これをエピソード記憶と呼び、「何が」、「どこで」、「いつ」、という情報を含みます。エピソード記憶の形成には、大脳嗅内皮質―海馬間の神経回路が必須であることが分かっています。これまでの研究によって、「何が」、「どこで」の2つの情報がどのように脳の中に統合され、記憶されていくかについては、比較的理解が進んでいますが、「いつ」という時間的情報が、「何が」や「どこで」という情報と、どのように脳の中で統合され、記憶されるのかについては、近年ようやく研究が進み始めたという状況です。
「いつ」と「何が」をどのように統合するかに関する研究は、2011年、利根川研究室が報告しています注1)。研究チームは、数秒から数十秒にわたって時間的に離れた2つの出来事を1つのエピソードとして記憶するためには、大脳嗅内皮質のⅢ層に位置する神経細胞から海馬CA1領域への直接入力が必須であることを報告しています。
例えば、何も知らない土地で電車を待っている時、突然音が鳴り、鳴り終わった20秒後に電車が到着するとします。この場合、経験によって、音が鳴って、その後しばらくすると電車が来るということが分かります。このように時間的に離れた2つの出来事を連結することをテンポラルアソシエーション[4]と呼び、エピソード記憶の形成に重要な要素となります。
しかし、このテンポラルアソシエーションの機能は、動物の行動利潤[5]のために、適切に調節される必要があります。たとえば、時間的に離れすぎている2つの出来事、もしくは、印象が非常に弱い出来事同士などは覚える必要がありません。そうしないと、脳の中で記憶の混乱が生じます。しかし、そのような時間的に離れた2つの出来事の連結分離を調節するような仕組みは全く知られていませんでした。
注1)Suh J, Rivest AJ, Nakashiba T, Tominaga T, Tonegawa S. “Entorhinal cortex layer III input to the hippocampus is crucial for temporal association memory”Science, 2011 Dec 9; 334(6061):1415-20.
研究手法と成果
大脳嗅内皮質Ⅱ層の神経細胞の多くは、海馬の歯状回[2]に軸索を投射していることが知られています。これを実証するために、歯状回に逆行性トレーサー[6]を注入し、大脳嗅内皮質Ⅱ層のどの神経細胞が、歯状回に投射しているのかを調べました。すると、非常に面白いことに、Ⅱ層内でトレーサーによって染色されない神経細胞群が存在し、それらの神経細胞は球状の細胞集団(クラスター)を形成していました(図1)。
共同研究グループは、この細胞集団に特異的な遺伝子群を調べ同定しました。この細胞集団は、100個程度の神経細胞からなる球状の細胞集団を形成していました。約30個の細胞集団が、まるでボールが壁にめり込んでいるかのように、格子状に大脳嗅内皮質Ⅱ層に内包されていました。共同研究グループは構造上の特徴からこの神経細胞をアイランドセルと名付けました。また、大脳嗅内皮質Ⅱ層から歯状回に投射している神経細胞をオーシャンセル[7]と名付けました。アイランドセルは海馬のCA1領域の限られた層(SL層)に軸索を投射する興奮性神経細胞であり(図2)、そのSL層に位置する抑制性神経細胞とシナプスを作ることで、海馬に対して抑制的に働くことを明らかにしました。
これまでの研究成果から、数秒から数十秒にわたって時間的に離れた2つの出来事を1つのエピソードとして記憶するためには、大脳嗅内皮質Ⅲ層から海馬への直接入力が必須ということが分かっています。共同研究グループは、解剖学的知見、生理学的知見を積み重ね、アイランドセルが海馬の抑制性神経細胞を介して、大脳嗅内皮質Ⅲ層の海馬への入力を抑制することを明らかにしました(図3)。このことから、共同研究グループは、「アイランドセルが、時間的に離れた2つの出来事を1つのエピソードとして記憶することを遮断する」という仮説を立てました。
オプトジェネティックス[8]の技術を用いて、光により人為的にアイランドセルを活性化させたり、抑制したりすることで、テンポラルアソシエーションメモリーにどのような影響が出るかを調べました。
アイランドセルを強く活性化すると、連結すべき2つの出来事が連結できませんでした。逆に、アイランドセルを抑制すると本来連結すべきでない2つの出来事が1つのエピソードとして記憶されてしまいました。つまり、車で例えると、Ⅲ層からの入力がアクセルとして、アイランドセルからの入力がブレーキとして働き、時間的に離れた出来事同士の連結と分離を調節していることが明らかになりました。
今後の期待
共同研究グループは、新規の神経回路を発見しただけでなく、時間的に離れた2つの出来事の連結と分離をアイランドセルが制御することを解明しました。遺伝子の発現にも正と負の調節機構が存在しますが、今回、記憶形成にもそうした調節機構が神経回路レベルで存在することが初めて明らかになりました。アイランドセルの機能研究は始まったばかりで謎が多く、なぜアイランドセルの細胞集団が格子状に並んでいるのか、グリッドセルとは関係があるのか、なども大変興味深い研究課題です。
また、記憶に関わる脳内の神経活動や、さまざまな神経系変性疾患、あるいは精神神経疾患のメカニズムの謎を解明していく上で、脳神経回路の正確な地図は欠かせません。現在、脳の正確な地図は部分的にしかでき上がっていませんが、脳の地図の完成を目指して、大型の国家プロジェクトが欧州、米国、日本で動き始めました。
今回の研究では、新技術や既存技術を複合的に用いることで、新規の神経回路を明らかにし、新規神経回路の情報を基礎として新たな仮説を考え、そして、時間的に離れた2つの出来事の連結と分離を調節する仕組みを明らかにしました。正確でより完成された脳の地図を効率的に作ることで、記憶の謎や神経系変性疾患・精神神経疾患のメカニズムの謎の解明がさらに進展していくと期待できます。
原論文情報
- Kitamura T, Pignatelli M, Suh H, Kohara K, Yoshiki A, Abe K, Tonegawa S. “ Island cells control temporal association memory ” Science, 2014 Feb 21, 343: 896-901
doi; 10.1126/science.1244634
発表者
理化学研究所
脳科学総合研究センター 理研-MIT神経回路遺伝学研究センター
利根川進研究室
博士研究員 北村 貴司(きたむら たかし)
脳科学総合研究センター
センター長 利根川 進(とねがわ すすむ)
(RIKEN-MIT神経回路遺伝学研究センター 教授)
お問い合わせ先
脳科学研究推進室
Tel: 048-467-9757 / Fax: 048-467-4914
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.大脳嗅内皮質、大脳嗅内皮質Ⅲ層、大脳嗅内皮質Ⅱ層
空間情報や物体情報の情報処理を行う皮質領域。ここで情報処理された後に、海馬に情報が伝達される。
大脳嗅内皮質は、I層からV層から成る層構造を形成している。Ⅲ層に位置する興奮神経細胞は、海馬CA1領域の興奮性神経細胞へ直接投射を行う。一方、Ⅱ層に位置する神経細胞の多く(オーシャンセル)は、海馬歯状回の興奮性神経細胞へ投射を行うことがされていたが、今回の研究によって、オーシャンセルとは別に、Ⅱ層に位置するアイランドセルが、海馬CA1領域の抑制性神経細胞に投射していることが分かった。 - 2.海馬、海馬のCA1領域、海馬の歯状回
海馬:大脳辺縁系の一部でヒトでは大脳側頭葉の内下部にある。長期記憶の形成や空間学習に重要な役割を果たしている。湾曲した細長い構造がタツノオトシゴ(ラテン語:hippocampus / 英語:sea horse)に似ていることから海馬と名付けられた。海馬は、特徴的な層構造をした細長い形をしており、CA1、CA2、CA3、歯状回(DG)の各部位からなる。海馬には、「大脳嗅内皮質Ⅱ層→歯状回(DG)→CA3→CA1」から構成される3つのシナプスを介するトライシナプス性神経回路と、「大脳嗅内皮質Ⅲ層→CA1」から構成される直接経路の神経回路が知られている。 - 3.アイランドセル
今回の研究によって発見された神経細胞群。大脳嗅内皮質Ⅱ層に位置するアイランドセルは、球状の細胞集団(クラスター)を形成し、CA1領域の抑制性神経細胞に投射していることが分かった。 - 4.テンポラルアソシエーション
数秒数十秒と時間的に離れた2つの出来事を連結する機能。エピソード記憶の重要な要素の1つ。 - 5.行動利潤
動物にとって利益となる行動原理。 - 6.逆行性トレーサー
軸索内部には神経終末より細胞体に向かう原形質の流れと、細胞体より終末に向かう原形質の流れがある。前者を逆行性軸索輸送といい、後者を順行性軸索輸送という。今回の研究に用いられた逆行性トレーサーCTB555は、神経終末より取りこまれ、細胞体に蓄積することから、どの神経細胞が歯状回に軸索を投射しているかどうかが分かる。 - 7.オーシャンセル
共同研究チームは、大脳嗅内皮質Ⅱ層に位置し海馬歯状回に投射している興奮性神経細胞をオーシャンセルと名付けた。 - 8.オプトジェネティックス
光を意味するOptoと遺伝学を意味するgeneticsを合わせた言葉。神経回路機能を光と遺伝子操作を使って調べる研究分野。ミリ秒単位の時間的精度を特徴とする。2005年に発表され神経科学の革命といわれた。
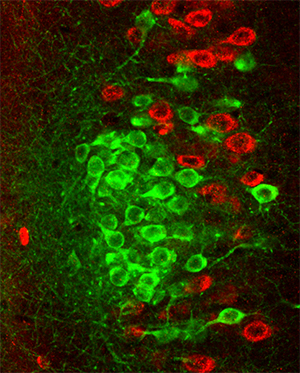
図1 大脳嗅内皮質Ⅱ層におけるアイランドセル(緑色)とオーシャンセル(赤色)
アイランドセルがクラスターを形成していることが分かる。また、アイランドセルの周りにオーシャンセルが位置している。
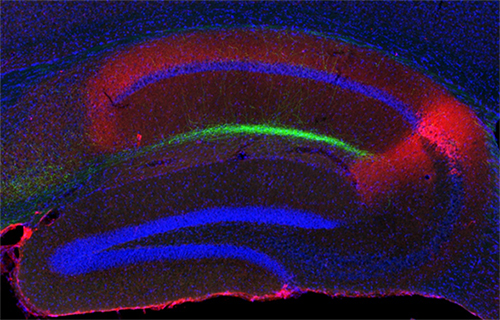
図2 海馬の断面図
アイランドセルの軸索(緑色)が、海馬CA1領域に投射していることが分かる。緑色がアイランドセルの軸索。赤色がCA2領域のマーカー。青が核染色。
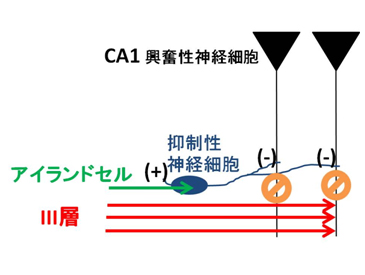
図3 モデル図
アイランドセルの入力(緑)が、CA1の抑制性神経細胞(青)を介して、大脳嗅内皮質Ⅲ層からのCA1興奮性神経細胞(黒)への入力を、遮断する。
