ポイント
要旨
理化学研究所(理研)脳科学総合研究センター神経成長機構研究チームの上口裕之チームリーダーと神経膜機能研究チームの平林義雄チームリーダー、東北大学 大学院薬学研究科の青木淳賢教授、東京大学 大学院総合文化研究科の太田邦史教授らの共同研究グループ※は、異なる種類の感覚を伝える神経突起[1]を分別してその行き先を制御する新たな脂質を発見しました。
身体からの感覚を伝える神経突起は脊髄を経由して脳へとつながっています。痛覚(皮膚で痛みを感じること)と固有感覚(自身の関節の位置や動きを感じること)などのように、異なる種類の感覚を伝える神経突起が、それぞれ脳脊髄の異なる部位へ投射するため、私たちは感覚の種類を識別することができます。脳脊髄の神経回路が作られる段階で、痛覚と固有感覚を担う神経突起は同じ経路を通って脊髄へ到達しますが、脊髄に入った直後にこれらの神経突起は分別され、混線することなくそれぞれの目的地へ誘導されます。しかし、この神経突起を分別するタンパク質はこれまで見つかっておらず、分別の仕組みは明らかにされていませんでした。
共同研究グループは、この神経突起の分別の仕組みは脂質によって制御されていると考えました。その仮説を立証するためには脂質を解析する必要がありますが、現代の医学生物学では脂質を詳細に解析することは非常に困難でした。そこで共同研究グループは、有機合成化学・分析化学・免疫学など異分野の研究者と連携し、脂質分子の合成・精製・定量・抗体作製の技術を神経科学と融合しました。その結果、神経突起の分別を担う新たな脂質「リゾホスファチジルグルコシド」を発見しました。リゾホスファチジルグルコシドは脊髄内の固有感覚の神経突起が通る特定の部位にのみ存在し、痛覚の神経突起を反発[2]することで、両方の神経突起は混ざり合うことなく別の目的地へ投射することが分かりました。また神経突起の表面に存在してリゾホスファチジルグルコシドを感知するGタンパク質共役受容体[3]も特定しました。
本研究は、「脂質が神経回路の構築を制御する」という新原理を明らかにしました。これに伴い、損傷した神経回路の修復技術の開発が進むことが期待できます。また、タンパク質の働きのみでは説明不可能な生命現象に対する研究の成功例であり、脳科学における新たな研究分野の開拓が期待できます。
本研究は、米国の科学雑誌『Science』(8月28日号)に掲載されます。
※共同研究グループ
理化学研究所
脳科学総合研究センター
神経成長機構研究チーム
チームリーダー 上口 裕之(かみぐち ひろゆき)
研究員 アダム・ティー・ガイ(Adam T. Guy)
神経膜機能研究チーム
チームリーダー 平林 義雄(ひらばやし よしお)
伊藤細胞制御化学研究室
主任研究員 伊藤 幸成(いとう ゆきしげ)
小林脂質生物学研究室
専任研究員 ペーター・グライメル(Peter Greimel)
東北大学大学院 薬学研究科 機能解析薬学講座 分子細胞生化学分野
教授 青木 淳賢(あおき じゅんけん)(日本医療研究開発機構 戦略的創造研究推進事業 CREST 研究代表者)
助教 井上 飛鳥(いのうえ あすか)
東京大学大学院 総合文化研究科 広域科学専攻 生命環境科学系
教授 太田 邦史(おおた くにひろ)
背景
私たちが持つ感覚の代表的なものに、皮膚で痛みを感じる「痛覚」と呼ばれるものと、自身の関節の位置や動きを感じることのできる「固有感覚」と呼ばれるものがあります。これらの感覚を伝える神経細胞の突起(神経突起)は、脊髄内の特定の部位を通り、最終的には脳へ投射します。その際に、脊髄までは、それぞれの感覚を伝える神経突起は互いに後根という束を作って到達しますが、脊髄へ入るとそれぞれの神経突起は分別されて、異なる部位を通るようになります(図1)。
私たちがそれぞれの感覚の違いを認識することができるのは、このように異なる感覚を担う神経突起が分別されて、混線することなくそれぞれの目的地へ投射するからです。しかし、これまでの研究で、この神経突起の分別を行うタンパク質などは発見されていませんでした。
私たちの研究チームは、タンパク質の働きだけでは説明不可能な神経突起の分別が脂質によって制御されているという仮説を立てました。ただ、生物学の研究対象として解析手法が定型化しているタンパク質と比較して、脂質は合成・定量・局在解析・抗体作製・機能阻害のすべてが技術的に困難であるため、異分野の研究者からなる共同研究グループ(図2)を立ち上げて本仮説の検証を進めました。
研究手法と成果
共同研究グループは、脊髄を構成する神経細胞以外の細胞(グリア細胞)がホスファチジルグルコシド(PtdGlc)という脂質を産生し、PtdGlcの代謝産物で水溶性の脂質リゾホスファチジルグルコシド(LysoPtdGlc)を細胞外へ放出することを発見しました(図3)。このPtdGlcとLysoPtdGlcは、脊髄の一部のグリア細胞のみが特定の部位(後索[4])で産生、放出します(図4)。
脊髄内の神経突起の走行様式と脂質の存在部位との位置関係から、共同研究グループは、LysoPtdGlcが痛覚神経突起のみを反発して固有感覚神経突起から分離させる役割を担っていると考えました。そこで、カバーガラス上に培養した感覚神経細胞から伸びる神経突起の先端部の片側にLysoPtdGlcの濃度勾配を作製し、LysoPtdGlcによる神経突起の反発を観察しました。LysoPtdGlcは痛覚神経突起を反発しましたが(図5)、固有感覚神経突起の伸長方向には影響を及ぼしませんでした。
生体内でのLysoPtdGlcの働きを検証するため、ADLib法[5]という抗体作製技術でLysoPtdGlcの機能を阻害する抗体を作製し、この抗体をニワトリ胚の脊髄内に注入してLysoPtdGlcが働かないニワトリ胚を作製しました。このニワトリ胚では、痛覚神経突起が固有感覚神経突起とともに脊髄の後索まで進入して混線してしまいました(図6)。したがって、痛覚と固有感覚の神経突起の分別にはLysoPtdGlcの働きが必要であることが分かりました。
次に、LysoPtdGlcが痛覚神経突起を反発する分子メカニズムを調べました。神経突起は細胞表面にLysoPtdGlcを感知する何らかの分子(受容体)を発現しているはずです。この受容体を特定するため、115種類の候補分子を網羅的に解析した結果、Gタンパク質共役受容体であるGPR55がLysoPtdGlcの受容体であることを発見しました。GPR55の遺伝子を欠損したノックアウトマウスから培養した神経細胞を用いて図5と同様の実験を行ったところ、LysoPtdGlcは痛覚神経突起を反発しませんでした。この実験結果から、LysoPtdGlcは神経細胞表面のGPR55を介して神経突起を反発することが分かりました。また、GPR55ノックアウトマウスの脊髄を観察したところ、図6右に示したLysoPtdGlcの働きを抑えた脊髄と同様に、痛覚神経突起が後根進入部[6]を超えて後索へ入り込んでいました。
以上の実験結果から、脊髄の後索でグリア細胞が放出する脂質LysoPtdGlcは、神経細胞表面のGタンパク質共役受容体GPR55を介して痛覚神経突起を反発し、これにより痛覚と固有感覚の神経突起が混線することなく別の目的地へ投射できることが明らかになりました。
今後の期待
神経突起の分別を担う新たな脂質とその受容体の発見により、脳脊髄の発生メカニズムの理解が深まり、損傷した神経回路の修復技術の開発が進むことが期待できます。また、GPR55は痛覚神経細胞だけでなく骨細胞・脂肪細胞・免疫細胞・がん細胞などにも発現していることから、これらの細胞が関与する疼痛・骨疾患・肥満・炎症・がん転移など各種疾患の病態解明と治療法開発に役立つ可能性があります。
さらに、本研究では今まで医学生物学において技術的に困難であった脂質研究を効率的に遂行するための異分野連携体制の構築に成功しており、今後、このような異分野連携を図ることで従来のタンパク質研究では解明が困難であった生命現象の研究を加速することができます。
原論文情報
- Adam T. Guy, Yasuko Nagatsuka, Noriko Ooashi, Mariko Inoue, Asuka Nakata, Peter Greimel, Asuka Inoue, Takuji Nabetani, Akiho Murayama, Kunihiro Ohta, Yukishige Ito, Junken Aoki, Yoshio Hirabayashi and Hiroyuki Kamiguchi, "Glycerophospholipid regulation of modality-specific sensory axon guidance in the spinal cord", Science, doi: science.aab3516
発表者
理化学研究所
脳科学総合研究センター 神経成長機構研究チーム
チームリーダー 上口 裕之(かみぐち ひろゆき)
脳科学総合研究センター 神経膜機能研究チーム
チームリーダー 平林 義雄(ひらばやし よしお)
東北大学大学院 薬学研究科 機能解析薬学講座 分子細胞生化学分野
教授 青木 淳賢(あおき じゅんけん)
(日本医療研究開発機構 戦略的創造研究推進事業 CREST 研究代表者)
東京大学 大学院総合文化研究科 広域科学専攻 生命環境科学系
教授 太田 邦史(おおた くにひろ)
 左上:上口裕之、右上:平林義雄
左上:上口裕之、右上:平林義雄左下:アダム・ティー・ガイ、右下:長塚靖子(論文著者)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
東京大学 大学院総合文化研究科 報道担当
Tel: 03-5454-6306 / Fax: 03-5454-4319
koho-jyoho [at] adm.c.u-tokyo.ac.jp(※[at]は@に置き換えてください。)
補足説明
- 1.神経突起
神経細胞から伸びる細長い突起で、シナプスを介して他の細胞へ情報を伝える。 - 2.反発
神経細胞の周囲に存在する分子が神経突起をはねのけて、その分子から遠ざかる方向へ神経突起を誘導すること。 - 3.Gタンパク質共役受容体
細胞膜を貫通するタンパク質であり、ホルモンや神経伝達物質などさまざまな細胞外因子を受容して細胞内へシグナルを伝える。すべてのタンパク質の中で最大のファミリーを形成し、多くの疾患に関与しているため、創薬の重要な標的となる。 - 4.後索
脊髄の背側にある神経突起の通り道。 - 5.ADLib法
動物を免疫することなく、遺伝子組み換えを促進した細胞を用いて試験管内で抗体を作製する技術。 - 6.後根進入部
脊髄へ向かう感覚神経突起の束(後根)が脊髄へ入った後の狭い領域。
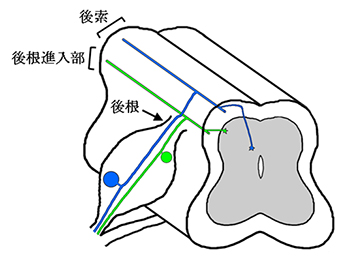
図1 脊髄へ投射する神経突起の走行
切断した脊髄の模式図で、図の上が背側で下が腹側。後根を通る痛覚神経突起(緑色)と固有感覚神経突起(青色)は、脊髄へ入ると分別される。痛覚神経突起は脊髄の外側部(後根進入部)を長軸方向に走行し、固有感覚神経突起は背側部(後索)を長軸方向に走行する。
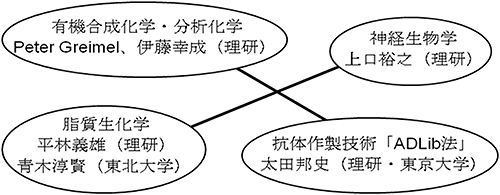
図2 神経回路構築における脂質の働きを検証するための異分野共同研究グループ
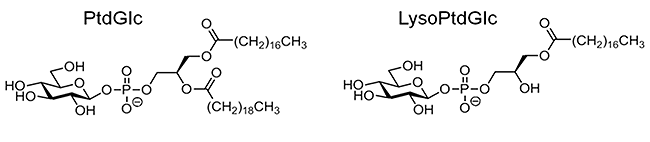
図3 ホスファチジルグルコシド(PtdGlc)とリゾホスファチジルグルコシド(LysoPtdGlc)の分子構造
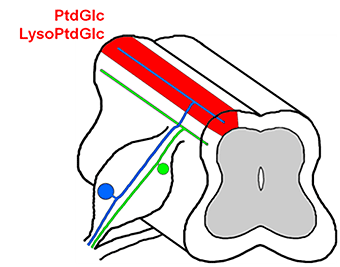
図4 脊髄での脂質の局在
PtdGlcとLysoPtdGlcは後索(赤で塗った領域、図1も参照)に限って存在する。固有感覚神経突起(青色)は脂質が存在する後索を走行するが、痛覚神経突起(緑色)は脂質が存在しない後根進入部を走行する。

図5 LysoPtdGlcによる痛覚神経突起の反発
痛覚神経突起の先端部の左側に、矢印の方向からLysoPtdGlcを投与し青色のような濃度勾配を作製した。LysoPtdGlc投与開始後の経過時間をそれぞれの画像の右下に示した。約40分後には、神経突起はLysoPtdGlcにより反発されて右方向に旋回した。
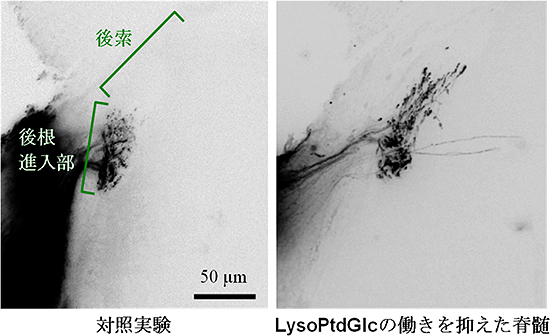
図6 ニワトリ胚内での痛覚神経突起の走行
図4の脊髄切断面の左上に相当する部分の顕微鏡写真。蛍光色素でラベルした痛覚神経突起を黒で示す。正常の脊髄では痛覚神経突起は後根進入部を走行する(左図)。しかし、LysoPtdGlcの機能阻害抗体で処理した脊髄では、痛覚神経突起は後索まで進入する(右図)。
