要旨
理化学研究所(理研)環境資源科学研究センター天然物生合成研究ユニットの高橋俊二ユニットリーダー、ケミカルバイオロジー研究グループの宮澤岳大学院生リサーチ・アソシエイト、長田裕之グループディレクターらの共同研究グループ※は、ポリケチド化合物[1]の骨格形成に重要となる伸長基質[1]が生合成される仕組みを解明しました。
微生物が生産する天然化合物は複雑な化学構造を持ち、それらの中には医薬、農薬などとして利用されるものもあります。ポリケチド化合物はこのような天然化合物の1つであり、特に放線菌[2]Streptomycessp. SN-593は構造の違う4種類のリベロマイシンと呼ばれるポリケチド化合物を作り出すことが知られています。このように、多様な構造を持つリベロマイシンは、他のポリケチド化合物の骨格形成に用いられる伸長基質とは違うユニークな伸長基質(2-アルキルマロニルCoA)を持ちます。共同研究グループは、この2-アルキルマロニルCoAの生合成に関わる遺伝子を絞りこみ、その遺伝子の働きを遺伝子欠損株を利用して調べ、そして各遺伝子に由来する酵素の機能を調べることで、2-アルキルマロニルの生合成される仕組みを明らかにしました。
ポリケチド骨格を形成する伸長基質の種類は限られており、本研究で見出した2-アルキルマロニルCoA生合成システムを活用することによって、創薬の探索源となるポリケチド化合物の構造多様性の拡張が期待できます。
本研究は、科学研究費補助金、農林水産省の農林水産業・食品産業科学技術研究推進事業(研究課題「ケミカルバイオロジーを基盤とした農薬等の探索研究」支援等により実施され、成果は米国の科学雑誌『The Journal of Biological Chemistry』(11月6日)、オンライン版(9月16日付け:日本時間9月17日)に掲載されました。
※共同研究グループ
理化学研究所 環境資源科学研究センター 天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
テクニカルスタッフ I Suresh Panthee(シュレス・パンテー)
ケミカルバイオロジー研究グループ
大学院生リサーチアソシエイト 宮澤 岳(みやざわ たけし)
上級研究員 清水 猛 (しみず たけし)
研究員 野川 俊彦(のがわ としひこ)
グループディレクター 長田 裕之(おさだ ひろゆき)
背景
微生物の作り出す二次代謝産物[3]のなかには、抗生物質や抗がん剤といった私たちにとって有用な生理活性物質も含まれています。こうした微生物が作り出す物質のうち、ポリケチド化合物と呼ばれる有機物の中には、実際に駆虫薬、抗がん剤、免疫抑制剤として利用されているものもあります。特に、放線菌(Streptomyces sp. SN-593)が生産するリベロマイシンA(RM-A)は骨を分解・吸収する破骨細胞を選択的に細胞死(アポトーシス)へと誘導して骨の分解・吸収を防ぐ作用を持ち、骨粗しょう症や骨関連疾患の治療薬としての開発が期待されています。Streptomyces sp. SN-593はRM-Aの他にアルキル側鎖[4]の長さが異なるRM-C、RM-D、RM-Eを作り出します。その4つの構造の多様性は伸長基質である2-アルキルマロニルCoA(ブチルマロニルCoA、イソブチルマロニルCoA、ペンチルマロニルCoA、ヘキシルマロニルCoA)に由来すると考えられます(図1)。ポリケチド化合物の骨格形成に用いられる伸長基質の多くはマロニルCoAまたはメチルマロニルCoAであるため、リベロマイシン生合成で見いだされたユニークな2-アルキルマロニルCoA生合成機構の解明はポリケチド化合物の構造多様化につながります。
研究手法と成果
共同研究グループは、まずリベロマイシン生合成に関わる21遺伝子の中からアミノ酸の相同性をもとに2-アルキルマロニルCoA生合成に関わると予想される遺伝子を3つに絞り込みました。今回見出したrevR、revS、revT遺伝子は一方向に並んで存在しており、脂肪酸代謝やCoAの代謝に関与しうる酵素に相同性を持っていました。各遺伝子の機能を明らかにする為、遺伝子破壊株を作製し、その代謝産物を解析した結果、revR遺伝子破壊株ではRM-Aの生産量が1/3程度に減少し、脂肪酸生合成初期反応に関わることでブチルマロニルCoA生合成に関与することが示唆されました。revS遺伝子破壊株では、すべてのRM類の生産量が半分程度に減少していました。一方、revT遺伝子破壊株ではすべてのRM類が生産されなくなりました。これらの結果から、上記3遺伝子はRM類の生合成に関与していることが示唆されました。次に、revS、revT遺伝子に由来する各酵素の機能を解析したところ、RevSは脂肪酸(炭素鎖長C8からC10)を効率的にアシルCoA[5]へと変換するCoAリガーゼ[6]であること、RevTは(E)-2-エノイルCoAを2-アルキルマロニルCoAに変換する還元カルボキル化酵素[7]であることが分かりました。
以上の結果より、RevSがアシルCoAを生成した後に、RevTが2-アルキルマロニルCoAを合成すると予想できますが、RevSが合成したアシルCoAの炭素鎖長は、RevT基質となる(E)-2-エノイルCoAよりも長いため、アシルCoAは脂肪酸の分解系を経て、(E)-2-エノイルCoAへと切り縮められる必要があると考えられました。この経路を証明する為、13C標識[8]した炭素鎖C8の脂肪酸([1,2,3,4-13C]オクタン酸)を添加して菌体を培養した後にRM-Aを単離し、NMR解析を行いました。その結果、オクタン酸のRM-Aへの取り込みが確認され、RevS、RevT反応には脂肪酸の分解系が関与していることが明らかになりました(図2)。
以上のことから、RevSは、脂肪酸代謝により生成した遊離脂肪酸を基質としてアシルCoAを生成し、RevTは、脂肪酸のβ酸化を経て生じた(E)-2-エノイルCoAを還元カルボキル化することにより2-アルキルマロニルCoAを生成するという生合成機構を明らかにすることができました。
今後の期待
本研究により、様々な脂肪酸がrevSとrevT遺伝子により2-アルキルマロニルCoAへと変換され、伸長基質としてポリケチド骨格に取り込まれることでリベロマイシン構造を多様化していることを突き止めました。今後、さまざまなポリケチドの構造に新規の伸長基質を導入することによって、化合物の多様性拡張や新たな生理活性物質の創出につながると期待できます。
原論文情報
- Takeshi Miyazawa, Shunji Takahashi, Akihiro Kawata, Suresh Panthee, Teruo Hayashi, Takeshi Shimizu, Toshihiko Nogawa, and Hiroyuki Osada, "Identification of middle chain fatty acyl-CoA ligase responsible for the biosynthesis of 2-alkylmalonyl-CoAs for polyketide extender unit", The Journal of Biological Chemistry, doi: 10.1074/jbc.M115.677195
発表者
理化学研究所
環境資源科学研究センター 天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
環境資源科学研究センター ケミカルバイオロジー研究グループ
大学院生リサーチ・アソシエイト 宮澤 岳(みやざわ たけし)
グループディレクター 長田 裕之(おさだ ひろゆき)
 天然物生合成研究ユニット
天然物生合成研究ユニット
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ポリケチド化合物、伸長基質
ポリケチド合成酵素(PKS)により、様々な開始基質にマロニルCoAやメチルマロニルCoAなどの伸長基質が複数回縮合して生合成された化合物である。PKSは複数の機能ドメインを有する巨大酵素であり、ドメイン構成に応じて還元、脱水等の反応が行われ構造が多様化される。 - 2.放線菌
土壌中など自然界に広く存在するグラム陽性の真正細菌で、多様な構造を有する二次代謝産物を生産することで知られる。人類は、それらの中から、医薬、農薬、動物薬などの生理活性を持つ物質を見いだし利用してきた。 - 3.二次代謝産物
生物体を構成、維持する上で重要な物質を一次代謝物、生育に必ずしも必須ではない物質を二次代謝物と呼ぶ。微生物において、二次代謝物の生合成に関わる遺伝子群はゲノム中のある特定の領域に並んで存在している。 - 4.アルキル側鎖
CnH2n+1で表される炭化水素鎖 - 5.脂肪酸アシルCoA
補酵素A(CoA)のチオールが脂肪酸のカルボキシル基とチオエステル結合を形成した化合物。生体内において、脂肪酸代謝、エネルギー生産等に用いられる。 - 6.CoAリガーゼ
高エネルギー化合物であるATP(アデノシン3リン酸)を補酵素として、CoAと基質のカルボキシル基を結合させる酵素。 - 7.還元カルボキル化酵素
還元反応とカルボキシル化反応を同時に触媒する酵素。 - 8.13C標識
安定同位体である13Cを用いて化合物を標識することにより、生体内で化合物の代謝パターンを予測することができる。
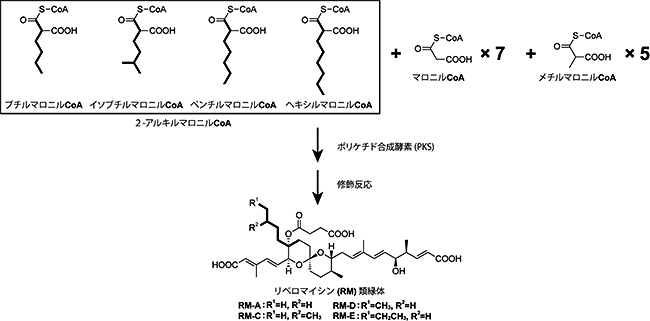
図1 リベロマイシン構造多様化に関わる伸長基質
4種の2-アルキルマロニルCoAはPKSの機能によりリベロマイシン骨格の一部に取り込まれる。
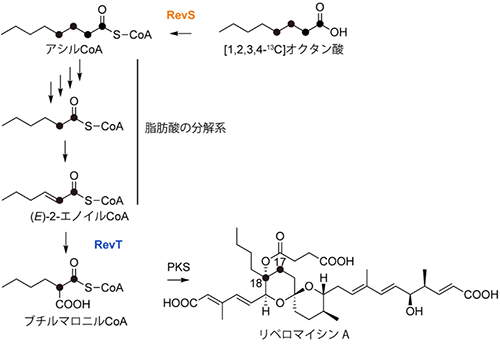
図2 RM-Aのアルキル側鎖の生合成
13C標識したオクタン酸は、RevS、脂肪酸分解系、RevTによりブチルマロニルCoAに変換された後に、リベロマイシンAの構造中に取り込まれる。
