要旨
理化学研究所(理研)ライフサイエンス技術基盤研究センターゲノム情報解析チームのピエロ・カルニンチ チームリーダー、ボグミル・カチコフスキー国際特別研究員と、オーストラリア・ハリー・パーキンス医療研究所のアリスター・フォレスト教授(理研客員主管研究員)らの国際共同研究チームは、多様な臓器のがんで異常な発現を示すRNAを多数発見しました。これらのRNA群は、がん診断の新しいバイオマーカー[1]となる可能性があります。
がん細胞で発現が変化するRNAは、がん診断のバイオマーカーや、抗がん剤の標的分子の候補となる可能性があります。特に、高い治療効果が見込める早期のがんや、治療後の再発などを診断するためのバイオマーカーとしての活用が期待されていますが、実際に臨床応用されているものはまだ少数しかありません。
国際共同研究チームは、理研が主導する「FANTOM5プロジェクト[2]」の一環として、さまざまな臓器・組織のがんに由来する225種の細胞株と、それらに対応する339種の正常細胞を対象に、がん細胞で発現が変化するRNAの解析を行いました。RNAにはタンパク質を作る情報を持ったメッセンジャーRNA(mRNA)と、タンパク質を作る情報を持たないノンコーディングRNA(ncRNA)[3]があります。解析の結果、多くのがん細胞株で発現が上昇、もしくは低下する2,108種のRNA群を発見しました。これらのRNAのうち、mRNAについて米国主導のがんゲノム解析プロジェクト「がんゲノムアトラス計画[4]」の臨床検体解析データと照合したところ、両者で共通して発現が上昇する76種のRNA群と、発現が減少する52種のRNA群を同定しました。さらに、ncRNAを詳細に解析したところ、がん関連遺伝子近傍のロングノンコーディングRNA(lncRNA)[5]や、特定のエンハンサー[6]の活性化を示すエンハンサーRNA(eRNA)[6]、反復配列[7]由来のRNAが多くのがん細胞で発現が上昇しており、ncRNAとがん化との関連を示唆する多くのデータを得ました。
今回同定したmRNAやncRNAは、多様な臓器のがんで汎用的に活用可能なバイオマーカーとしての応用が期待できます。また、これらのRNA群と発がんとの関係を明らかにすることで、抗がん剤の新たな標的となる可能性もあります。
本研究は、米国の科学雑誌『Cancer Research』に掲載されるのに先立ち、オンライン版(11月9日付け:日本時間11月10日)に掲載されました。
背景
がんは進行すればするほど治療が難しくなるため、早期診断が非常に重要です。がんの診断法の1つとして、血中のバイオマーカーの測定があります。バイオマーカーは生体の変化を示す指標で、生体分子や遺伝子発現の変化を捉えてがんを含む疾患の有無や進行度を正確に把握するために用いられます。しかし、血液検査でがんを診断できるバイオマーカーは少なく、診断に十分に役立てられているとはいえないのが現状です。効果的ながん治療を実現するため、信頼性が高く早期発見が可能ながんバイオマーカーの探索が進められています。
がんは、1つの組織で生じた場合であっても構成する細胞が複数存在し、遺伝子変異が細胞ごとに異なることが多いため、不均一で多様な性質を持っています。また、性質の違いは臓器が異なればより大きくなる傾向にありますが、異なる臓器に生じたがんに共通した性質が見つかる場合があります。実際に、米国主導の大規模ながんゲノム解析プロジェクト「がんゲノムアトラス計画」では、12種のがんにおいて高頻度で現れる幾つかの遺伝子変異や発現変化を報告しています。また理研が主導する国際研究コンソーシアムFANTOMの第5期「FANTOM5プロジェクト」は、がん由来の細胞株や正常な初代培養細胞を含む約1,000種類のサンプルからRNAを抽出し、CAGE法[8]による網羅的・定量的な発現解析を行っています。FANTOM5で解析に用いるがん細胞株はがん組織から単離培養されたもので、均質な細胞集団であるものの、長期間培養することで本来のがんの性質が変化する可能性があります。一方、がんゲノムアトラス計画で用いているがん細胞や正常細胞は、患者から直接採取したものですが、血球など複数種の細胞が混在するといった問題があります。今回の研究では双方のデータを照合することでその問題点をカバーし、多様な臓器のがんで発現異常を示すRNAの網羅的な探索を行いました(図1)。
研究手法と成果
国際共同研究チームは、FANTOM5プロジェクトで集めた多様な細胞のうち、さまざまながんに由来する細胞株225種と、それらに対応する正常な組織から得た初代培養細胞339種を用いました。これらの細胞のRNAの発現データを解析し、がん細胞において発現量が大きく上昇もしくは減少、または、発現のオン・オフが切り替わっているRNAを探索しました(図2)。
解析の結果、多様ながん細胞で発現が変化するRNAは2,108種ありました。このうち1,595種類ががん細胞で発現が上昇、または正常細胞で発現せずがん細胞のみで発現しているものでした。一方、がん細胞で発現が減少、または正常細胞では発現が見られるのにがん細胞ではまったく発現していないものが513種類存在しました。RNAには、タンパク質を作る情報を持ったメッセンジャーRNA(mRNA)と、タンパク質を作る情報を持たないノンコーディングRNA(ncRNA)がありますが、2,108種のRNAのうち、約6割がmRNAで、約1割がロングノンコーディングRNA(lncRNA)でした。また、未知のRNAも2割以上含まれていました(図3)。
約6割を占めたmRNAのうち、同じ遺伝子の複数の転写開始点に由来するRNAの重複を除くと、656種の遺伝子ががん細胞と正常細胞で異なる発現をしていることが分かりました。これらの遺伝子をがんゲノムアトラス計画の遺伝子データと照合した結果、両者で共通する128種の遺伝子を得ることができました。このうち、がん細胞で発現がオンになる、もしくは発現が上昇する遺伝子は76種あり、TOP2A遺伝子などの既知のバイオマーカーやがん遺伝子、細胞周期関連因子、DNA代謝酵素、発生関連遺伝子などがありました。一方、発現が減少した遺伝子は52種あり、酸化還元反応[9]関連遺伝子が多く含まれていました。細胞内の代謝反応は主に酸化還元反応であり、がん化によって代謝のリプログラミングが起きていることが示唆されました。
次に、ncRNAを詳しく解析しました。271種類のlncRNAの発現が変化しており、その大半(247種)ががん細胞で発現上昇していました。発現が上昇したlncRNAの多くはがん細胞で活性化するがん関連遺伝子の近傍から転写されており、これらのがん関連遺伝子の発現制御に関与している可能性が示唆されました。また、がん細胞で発現上昇するncRNAには、転写制御領域であるエンハンサーの活性化を示すエンハンサーRNA(eRNA)や、レトロトランスポゾン[10]などの反復配列に由来するRNAが多数存在しました。特に強い発現上昇を示す反復配列には、ゲノム中に散在する反復配列の一種REP522ファミリー[11]が含まれていました。この発現上昇はqRT-PCR法[12]を用いたがん細胞株やがん組織の発現解析でも確認できました。REP522ファミリーはこれまで研究が進んでおらず、がんとの関連を示したのはこれが初めてです。
今後の期待
がん細胞と正常細胞の網羅的な発現解析により、mRNAとともに多数のncRNAが、汎用的ながんバイオマーカーの候補として新たに浮かび上がりました。これらのタンパク質やRNAを検出する技術を開発できれば、さまざまな種類のがんに応用可能な診断法が実現するかもしれません。また、がん治療の新たな標的分子を探索する創薬への貢献も期待できます。
さらに今回の研究では、反復配列に由来するRNAの発現上昇が、がん化の一般的な傾向であることが示唆されました。今後のがん研究では、反復配列の発現とがん化の解明が課題となります。
原論文情報
- Bogumil Kaczkowski, Yuji Tanaka, Hideya Kawaji, Albin Sandelin, Robin Andersson, Masayoshi Itoh, Timo Lassmann, the FANTOM5 consortium, Yoshihide Hayashizaki, Piero Carninci, and Alistair R. Forrest, "Transcriptome analysis of recurrently deregulated genes across multiple cancers identifies new pan-cancer biomarkers.", Cancer Research, doi: 10.1158/0008-5472.CAN-15-0484
発表者
理化学研究所
ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 LSA要素技術研究グループ ゲノム情報解析チーム
チームリーダー ピエロ・カルニンチ(Piero Carninci)
研究員 ボグミル・カチコフスキー(Bogumil Kaczkowski)
ハリー・パーキンス医療研究所 Systems biology and Genomics
教授 アリスター・フォレスト(Alistair Forrest)
(理化学研究所 客員主幹研究員)
 ピエロ・カルニンチ
ピエロ・カルニンチ
 ボグミル・カチコフスキー
ボグミル・カチコフスキー
 アリスター・フォレスト
アリスター・フォレスト
お問い合わせ先
理化学研究所 ライフサイエンス技術基盤研究センター
広報・サイエンスコミュニケーション担当 山岸 敦(やまぎし あつし)
Tel: 078-304-7138 / Fax: 078-304-7112
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.バイオマーカー
生体の変化を示す指標で、特定の状態の細胞を特徴付けることにより、疾患の有無や進行度を正確に把握するために用いられる。特定の疾患に特徴的な分子や遺伝子発現を病気の診断に用いる場合、これらを診断マーカーと呼ぶ。 - 2.FANTOM5プロジェクト
理化学研究所が中心となり結成した国際研究コンソーシアムFANTOMの第5期プロジェクト。FANTOM5には20カ国、100以上の研究機関が参加し、ヒトの主要な組織、初代培養細胞、細胞株を対象にゲノムワイドな解析を行った。185,000個のプロモーターと44,000個のエンハンサーの遺伝子制御活性を測定し、正常な細胞や細胞株の体系的な定義注)を得ることができた。
注)2014年3月27日プレスリリース「 ゲノム上の遺伝子制御部位の活性を測定し正常細胞の状態を定義」 - 3.ノンコーディングRNA(ncRNA)
non-coding RNA。メッセンジャーRNA(mRNA)と異なり、タンパク質の設計図として用いられないRNAの総称。エピジェネティクス(塩基配列に依存しない遺伝子の調節機構)や転写、翻訳といった生物の活動の中枢をなす反応、幹細胞性の維持など、さまざまな働きに関与するncRNAが次々に報告されており、その重要性に注目が集まっている。 - 4.がんゲノムアトラス計画
The Cancer Genome Atlas(TCGA)。米国主導の大規模ながんゲノム解析プロジェクト。ゲノム、トランスクリプトーム、エピジェネティックな修飾など、がんのゲノムについて包括的な理解を目指し解析を進めている。
The Cancer Genome Atlas(TCGA)ホームページ(英語) - 5.ロングノンコーディングRNA(lncRNA)
long non-coding RNA。ノンコーディングRNA(ncRNA)のうち、100~200塩基かそれ以上の塩基からなる長いものを指す。全長にわたる保存性は高くないが、反復配列やウィルス由来の配列などの保存性の高い断片が含まれる。転写、翻訳、エピジェネティクスなど生体内の多様なプロセスに寄与していることが示されている。 - 6.エンハンサー、エンハンサーRNA(eRNA)
エンハンサー(enhancer)領域(配列)は、主に遺伝子の上流や下流に位置し、遺伝子の転写効率を変化させるDNAの特定の配列のうち、転写効率を著しく高める部分。エンハンサーが活性化する際、エンハンサー配列からノンコーディングRNA(ncRNA)が転写されることが近年報告され、エンハンサーRNA(eRNA)と呼ばれている。 - 7.反復配列
ゲノム中に多数見られる、同じ配列の繰り返しからなる保存性の高い配列。ウイルスゲノムが核ゲノム中に組み込まれた際に生じたと考えられる。かつては宿主である細胞にとって意味のないものと考えられていたが、近年、細胞が自らの機能のためにこれらの配列を活用していることを示唆する報告が出てきており、関心が高まっている。 - 8.CAGE法
Cap Analysis Gene Expressionの略。理研が独自に開発した手法で、耐熱性逆転写酵素やmRNAのCap構造を捕捉する技術を組み合わせて転写産物の5'末端の塩基配列を決定する実験手法。この塩基配列を読み取ってゲノム配列と照らし合わせて、どこから転写が始まっているかを調べることができる。遺伝子の転写開始点をゲノムワイドに同定できる。 - 9.酸化還元反応
2つの物質間で電子の移動が生じる反応の総称で、電子を奪う反応(酸化)と電子を与える反応(還元)を対にした言葉。呼吸による生命活動に必要なエネルギーの獲得など、生体内ではさまざまな酸化還元反応が起きている。 - 10.レトロトランスポゾン
HIVなどのレトロウイルスのように、DNA→RNAへの転写と、RNA→DNAへの逆転写によって増殖する性質を持つ遺伝因子。ゲノム上のレトロトランスポゾンが転写されてRNAになり、さらに逆転写酵素によりDNAに戻ることでゲノム中を移動しコピー数を増やす。ヒトゲノムの進化の過程で、ほとんどのレトロトランスポゾンは不活性化されたと考えられている。 - 11.REP522ファミリー
約1.8Kbの長さで、不完全な回文配列と、トランスポゾンに共通の配列を持つ反復配列の一種。テロメア(染色体の末端部にある構造)と関連する配列と考えられていたが、テロメア以外の領域にも存在する。ほとんど研究が進んでいない。 - 12.qRT-PCR法
定量PCR(qPCR、quantitative PCR)とは、DNAを増幅するPCRの手法を用いて、サンプルに含まれているDNA量を測定する手法。本研究で用いたqRT-PCR法では、RNAを逆転写して作ったcDNAをこの手法で測定することでRNA量を測定している。
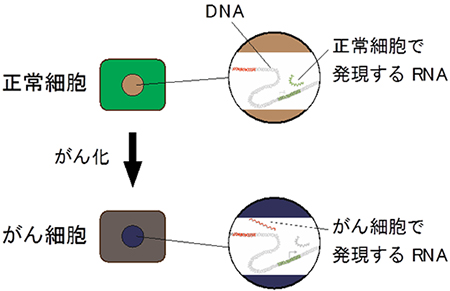
図1 本研究の概要
正常細胞とがん細胞のRNAを解析し、多様な臓器のがん細胞で発現が変化するRNAを網羅的に解析した。
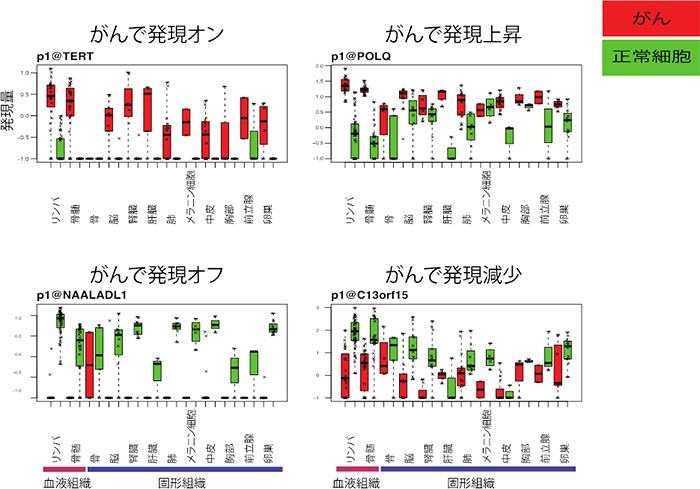
図2 多様な臓器に由来するがん細胞株で発現変化を示すRNA
がん細胞株において、正常な初代培養細胞と異なる発現を示すRNAの例。4つの遺伝子のプロモーター配列(遺伝子を発現させる機能を持つ塩基配列)の発現からの発現量が、それぞれの組織の細胞でどのように変化しているかを示した。
- 左上:正常初代培養細胞では発現せず、がん細胞株で発現がオンになる。
- 左下:正常初代培養細胞で発現し、がん細胞株では発現がオフになる。
- 右上:正常初代培養細胞に比べてがん細胞株での発現が上昇する。
- 右下:正常初代培養細胞に比べてがん細胞株での発現が減少する。
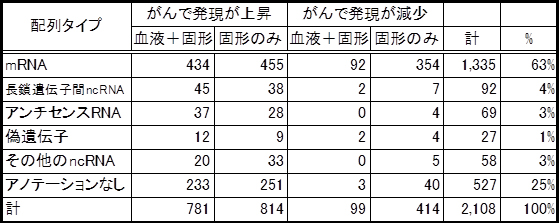
図3 多様ながん細胞で発現が変化するRNA群
FANTOM5プロジェクトで解析した細胞株と、正常初代培養細胞の比較から明らかになった、がん細胞で発現が変化するRNA群の内訳。血液がんと固形がんの両方で共通して発現が変化していたものと、固形がんだけで発現が変化していたRNAの数を示す。既存のデータベースと照合できた配列タイプのうち、mRNA以外の配列タイプはロングノンコーディングRNA(lncRNA)を含む。「アノテーションなし」は、既知の配列との関連性がみられなかったもので、多くのncRNAが含まれる。
