要旨
理化学研究所(理研)脳科学総合研究センター シナプス可塑性・回路制御研究チームの合田裕紀子チームリーダーらの研究チーム※は、ラット及びマウスを使った実験で脳内の「アストロサイト[1]」と呼ばれる細胞が、1つの神経細胞に存在する複数のシナプス[2]間の「シナプス強度[3]」のバランスを調節していることを発見しました。
脳内では数千億個の神経細胞が複雑な神経ネットワークを形成しています。神経細胞同士がつながっている部分はシナプスと呼ばれ、このシナプスを介して1つの神経細胞から次の神経細胞へと情報が伝わります。シナプスが使われる頻度によって、シナプス強度(情報の伝わりやすさ)が変化し、学習や記憶が可能になるとされています。1つの神経細胞には平均数万個ものシナプスがありますが、個々のシナプスはそれぞれの情報の入力に応じて独立に強度変化を示すと考えられてきました。ところが近年、情報の入力があったシナプス(ホモシナプス)の近傍の入力のないシナプス(ヘテロシナプス)でも、シナプス強度の変化が起こる現象が報告され、同一神経細胞内の異なるシナプス間で相互作用が生じる可能性が指摘されていました。しかし、そのような相互作用を支えるメカニズムは分かっていませんでした。
研究チームは、脳内の神経ネットワークの性質を反映しつつ、比較的単純なネットワークを形成する海馬[4]由来の培養神経細胞系[5]をモデルに、ホモシナプスとヘテロシナプスの性質の変化を、電気生理学的手法[6]を用いて調べました。その結果、ホモシナプスへの入力によって起こるシナプス強度の変化に伴い、ヘテロシナプスでもシナプス強度が変化することが分かりました。詳しい解析により、ヘテロシナプスでのシナプス強度の変化は、神経細胞を取り囲むアストロサイトのNMDA型グルタミン酸受容体[7]に依存することが分かりました。また、神経細胞表面のL型電位依存性カルシウムチャネル(L-VGCC)[8]の働きを介してホモシナプスとヘテロシナプスとの間のシナプス強度の差がもたらされることが分かりました。さらにこれらのメカニズムは、より生体に近い海馬のスライス標本[9]でも当てはまることが明らかになりました。
神経細胞における複数のシナプス強度のバランスの崩れが、精神疾患の発症につながる可能性が指摘されています。本研究で明らかになった、複数のシナプス間のシナプス強度のバランスを調節するメカニズムの理解が進めば、精神疾患発症のメカニズムの解明につながると期待できます。
本研究は、米国の科学雑誌『Proceedings of the National Academy of Science』に掲載されるのに先立ち、オンライン版(4月25日付け:日本時間4月26日)に掲載されます。
※研究チーム
理化学研究所 脳科学総合研究センター シナプス可塑性・回路制御研究チーム
チームリーダー 合田 裕紀子(ごうだ ゆきこ)
研究員(研究当時) マチュー・レテリエ (Mathieu Letellier)
研究員 ユンギョン・パク(Yun Kyung Park)
研究員 トーマス・E・チェイター(Thomas E Chater)
訪問研究員 ピーター・H・チップマン(Peter H Chipman)
研究員 スニタ・ギミレ・ゴータム(Sunita Ghimire Gautam)
研究員(研究当時) 大島-鷹合 知子(おおしま-たかごう ともこ)
背景
脳内では神経細胞が数千億個集まり、ほかの神経細胞とつながり合って複雑につながった、巨大な神経ネットワークを形成しています。神経細胞同士がつながっている部分はシナプスと呼ばれ、このシナプスを介して1つの神経細胞から次の神経細胞へと情報が伝わります。シナプスの大半は化学シナプスというもので、神経伝達物質(グルタミン酸やアセチルコリンなど)をはじめとする化学物質が、シナプス前部の神経末端から放出され、それをシナプス後部の神経細胞の樹状突起にある受容体が受け取ることによって、情報伝達が行われます(図1)。シナプスには、使われる頻度によって情報の伝わりやすさ(シナプス強度)が変化する性質があります。一般に、神経活動によるシナプスへの情報の入力の頻度とタイミングによって、そのシナプスは増強されたり、抑圧されたりすることが知られています。このシナプス強度の変化は、シナプス前部から神経伝達物質が放出される確率や、シナプス後部の受容体の量が増減することによって起こるとされ、学習や記憶を支えるメカニズムであると考えられています。
1つの神経細胞には平均数万個ものシナプスがありますが、これまで、個々のシナプスはそれぞれの情報の入力に応じて独立に強度変化を示すと考えられてきました。ところが近年、シナプス強度の変化を起こす入力があったシナプス(ホモシナプス)の近傍に存在する入力のないシナプス(ヘテロシナプス)でも、シナプス強度の変化が起こる現象が報告され、同一神経細胞内の異なるシナプス間で相互作用が生じる可能性が指摘されていました。しかし、そのような相互作用を支えるメカニズムの詳細は不明でした。
研究チームは、脳内の神経ネットワークの性質を反映しながらも、比較的単純なネットワークを形成する、海馬由来のラットの培養神経細胞系をモデルに、ホモシナプスとその近傍のヘテロシナプスの性質の変化を、電気生理学的手法を用いて詳しく調べることで、異なるシナプス間の相互作用の仕組みの解明を試みました。
研究手法と成果
海馬由来の単離神経細胞を培養して神経ネットワークを形成させた後、別々の神経細胞からの入力を受け取り、そこに形成された各シナプスが関与していない神経細胞を選び、それぞれのシナプスの伝達効率(シナプス強度)の変化を電気生理学的手法によって調べました(図2)。神経細胞2へ入力する神経細胞1を特定の強さと頻度で電気刺激により活性化させると、受け手側の神経細胞2との間のホモシナプスの伝達効率が増強されたり、抑圧されたりしました。この現象は過去の知見と一致しています。ところが、この実験条件では、神経細胞2は神経細胞3ともつながっており、神経細胞1からの入力を受けないシナプスでも、シナプス前部における神経伝達物質の放出確率が上がって伝達効率が変化していました(図2)。このことは、入力のあったホモシナプスのシナプス強度の変化に伴い、その近傍の入力のないヘテロシナプス前部で、シナプス強度の変化が起こることを示しています。
このヘテロシナプスでの変化は、NMDA型グルタミン酸受容体(NMDA受容体)の阻害剤AP5(2-アミノ-5-ホスホノ吉草酸)や、アストロサイトの活動を低下させるフルオロアセテートを加えると、起こりませんでした。このことは、入力のないヘテロシナプスでのシナプス強度の変化が、NMDA受容体と神経細胞を取り囲むアストロサイトに依存することを示しています。
また、神経細胞の興奮(活動増加)に伴って細胞内にカルシウムイオン(Ca2+)を選択的に透過させる、L型電位依存性カルシウムチャネル(L-VGCC)の阻害剤ニフィディピンを投与したところ、ホモシナプス強度の変化自体に影響はないものの、ヘテロシナプスの強度が通常とは逆方向に変化して、その結果、ホモシナプスとヘテロシナプスとの間のシナプス強度の差が大きく減少しました。これらのメカニズムは、より生体に近い海馬のスライス標本においても当てはまりました。
さらに、あえてホモシナプスを強く刺激しなくても、ホモシナプスとヘテロシナプスの間ではシナプス強度のばらつきがありました。そこで、光遺伝学的手法[10]を使い、光に応答する抑制的イオンチャネルをアストロサイトに人為的に発現させ、特定の波長の光を照射してそのイオンチャネルを稼働することでアストロサイトの活性化を阻害してみました。その結果、ホモシナプスとヘテロシナプスとの間のシナプス強度の差がなくなりました。また、アストロサイトのNMDA受容体だけ発現を阻害したところ、シナプス強度の差が減少しました。
これらの結果から、異なるシナプス間の相互作用は、神経細胞を取り囲むアストロサイトにおけるNMDA受容体の働きに依存することが明らかになり、同時にホモシナプスとヘテロシナプスの間のシナプス強度の差は、神経細胞表面のL型電位依存性カルシウムチャネルの働きを介して形成されることが分かりました。
今後の期待
本研究で明らかになったホモシナプスの変化により、近傍のヘテロシナプスでのシナプス強度が調節されるようなシナプス間相互作用のメカニズムは、特に学習や記憶のプロセスにおいて、回路の中の特定のルートの情報の伝わりやすさを促進するという点で重要だと考えられます。近年、このような複数のシナプス間におけるシナプス強度のバランスの崩れが、いくつかの精神疾患の発症につながる可能性も指摘されています。シナプス間相互作用のメカニズムをさらに解明することにより、精神疾患の発症メカニズムの理解につながることが期待できます。
またこれまで、電気信号を発しないアストロサイトは、神経細胞にエネルギーを供給したり、神経細胞を構造的に支持したりと、受動的な役割を主に担っていると考えられてきました。しかし、本研究によって、アストロサイトはシナプス間の相互作用にも重要な役割を果たしていることが明らかになりました。
原論文情報
- Mathieu Letellier, Yun Kyung Park, Thomas E Chater, Peter H Chipman, Sunita Ghimire Gautam, Tomoko Oshima-Takago, Yukiko Goda, "Astrocytes regulate heterogeneity of presynaptic strengths in hippocampal networks", Proceedings of the National Academy of Science, doi: 10.1073/pnas.1523717113
発表者
理化学研究所
脳科学総合研究センター シナプス可塑性・回路制御研究チーム
チームリーダー 合田 裕紀子(ごうだ ゆきこ)
 合田 裕紀子
合田 裕紀子
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.アストロサイト
神経系を構築する細胞のうち、神経細胞ではない細胞であるグリア細胞の1種。多数の突起をもち星状にみえることから名付けられた。その表面積は広く、ラットでは約9万個の、ヒトでは200万個以上のシナプスを覆っていると考えられている。 - 2.シナプス
神経細胞の軸索の末端と、次の神経細胞の樹状突起の間の小さな間隙。その多くは化学シナプスと呼ばれ、神経伝達物質のような化学物質がシナプス前部から放出されて、シナプス後部にある受容体に結合することで情報が伝達される。化学シナプスの他に電気的につながっている電気シナプスもある。 - 3.シナプス強度
シナプスにおける情報伝達率。化学シナプスの場合は、シナプスにおける神経伝達物質の放出量や受容体の量などによって、情報伝達率が変化する。 - 4.海馬
脳の側頭葉にある記憶や空間認知などに関わる領域。 - 5.培養神経細胞系
脳組織の一部を切り出し、細胞をばらばらに単離して培養液の中で培養し、簡単な神経回路を再現させる実験系。 - 6.電気生理学的手法
神経細胞の持つ電気的な特徴を計測する方法。 - 7.NMDA型グルタミン酸受容体
神経伝達物質の1つであるグルタミン酸に結合する受容体の1つ。 - 8.L型電位依存性カルシウムチャネル(L-VGCC)
神経細胞膜の脱分極を感知し、細胞外から細胞内へカルシウムイオンを透過させるチャネル。 - 9.スライス標本
脳組織を細胞が生きた状態で薄片にした標本で、主に電気生理学的手法を用いた解析に使用される。 - 10.光遺伝学的手法
光に応答するタンパク質を遺伝子操作の手法で特定の細胞に発現し、光を照射することによってそのタンパク質の機能を操作する技術。
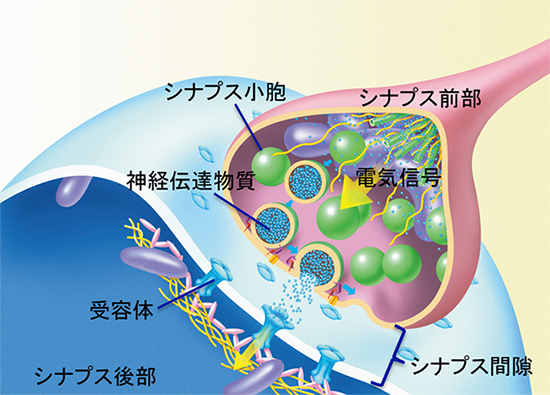
図1 シナプスの模式図
神経細胞の軸索の末端は少し膨らんだ形をしていて、受け手側の神経細胞の樹状突起と小さな隙間(シナプス間隙)を挟んで接続している。軸索の末端側をシナプス前部と呼ぶ。神経細胞の電気信号が末端に到達すると、末端に存在するシナプス小胞内に蓄えられた神経伝達物質がシナプス間隙に放出される。放出された神経伝達物質は受け手側(シナプス後部)の細胞膜上にある受容体に結合し、受け手側の神経細胞へと情報を伝達する。
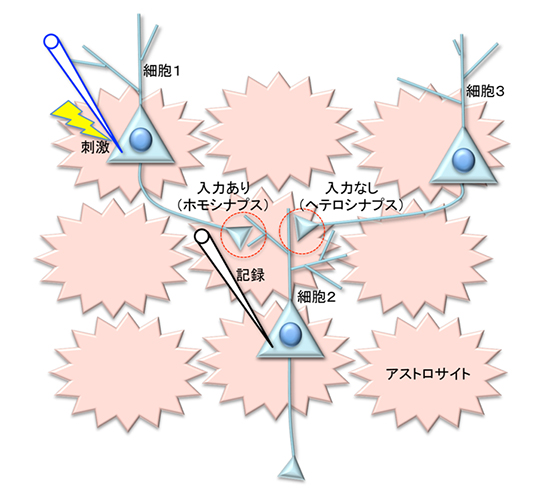
図2 海馬の培養細胞系による実験
神経細胞1と神経細胞3から情報を受け取る神経細胞2を選び、神経細胞2におけるそれぞれのシナプスでの情報の伝わりやすさの変化を記録電極で記録した。神経細胞1を特定の強さと頻度で電気刺激により活性化させると、神経細胞1と神経細胞2の間のシナプス(入力あり:ホモシナプス)の情報の伝わりやすさは変化する。それに伴って入力のない神経細胞3と神経細胞2の間のシナプス(ヘテロシナプス)でも情報の伝わりやすさが変化した。観察したシナプス間の相互作用は、周囲のアストロサイトのNMDA受容体に依存する。
