要旨
理化学研究所(理研)伊藤ナノ医工学研究室の張晨国際プログラム・アソシエイト、宮武秀行専任研究員、創発物性科学研究センター創発生体工学材料研究チームの伊藤嘉浩チームリーダー、佐甲細胞情報研究室の稲葉岳彦研究員、吉林大学薬学部の王 毅教授、中国科学院長春応用化学研究所の王宇助教、章培標教授らの国際共同研究グループ※は、人工臓器の生体材料として使用されるチタンの表面に、ムラサキイガイ[1]由来のバイオ接着成分を固定化することで、チタンに細胞を活性化する機能を付与することに成功しました。
人工臓器の材料は生体材料と呼ばれ、金属やセラミックスなどの無機材料とプラスチックなどの有機材料に分類されます。無機材料は、主に骨などの硬い組織の置換に使われ、例として人工関節、歯科インプラントなどが挙げられます。このような無機材料は強度については十分ですが、人体とは異なった材料であるために移植後の生着に長い時間を要し、その間に感染症を引き起こして生着しない場合もあります。また、代謝機能がないため、患者の高齢化に伴い、劣化や不具合が生じるなどの問題があります。この問題を解決するために、国際共同研究グループは強力な接着性と生体に対する安全性を両立できる生体材料の作製法の開発に取り組みました。
ムラサキイガイなどの貝類は、水中でも岩場に接着することができます。これは、自身が分泌する接着タンパク質による作用です。ムラサキイガイの接着性の源となるのが、ドーパ(DOPA)と呼ばれる化合物です。DOPAは天然アミノ酸のチロシンに水酸基が一つ付加した物質で、チロシンよりも水素結合が強くなるため、さまざまな物質に接着できると考えられています。国際共同研究グループは、遺伝子組換え技術と酵素法によって、成長タンパク質IGF-1のC末端にムラサキイガイ由来の接着性ペプチドをつなげた「IGF-1-X-K-X-K-X(X=DOPA、K=リシン)」を作り出すことに成功しました。この新しいタンパク質の効果を調べたところ、金属材料のチタンに強く結合し、細胞増殖を活性化する効果を持つことが分かりました。
本成果は、今後、再生医療や医療機器開発などの分野での貢献する方法が期待できます。
本研究は、ドイツの化学雑誌『Angewandte Chemie International Edition』オンライン版(7月6日付け)に掲載されました。
※国際共同研究グループ
理化学研究所
伊藤ナノ医工学研究室
国際プログラム・アソシエイト 張 晨(ジャン チェン)(吉林大学薬学部 博士課程)
専任研究員 宮武 秀行(みやたけ ひでゆき)
創発物性科学研究センター 創発生体工学材料研究チーム
チームリーダー 伊藤 嘉浩(いとう よしひろ)(伊藤ナノ医工学研究室 主任研究員)
佐甲細胞情報研究室
研究員 稲葉 岳彦(いなば たけひこ)
吉林大学 薬学部
教授 王 毅(ワン イ)
中国科学院 長春応用化学研究所
助教 王 宇(ワン ユ)
教授 章 培標(ジャン ペイビャオ)
背景
現在、高齢化の進行やスポーツ人口の増加に伴い、日本国民の10~15人に1人は人工臓器の恩恵にあずかっているといわれています。これら人工臓器の材料は生体材料と呼ばれ、古くは一般的な材料から生体になじむものが選ばれるだけでしたが、近年は人工臓器用に材料の設計が行われるようになりました。
生体材料は、金属やセラミックスのような無機材料とプラスチックなどを中心とする有機材料に分類されます。無機材料は、主に骨などの硬い組織の置換に用いられ、例として人工関節、歯科インプラントが挙げられます。これらは数十年前から実用化されているものですが、もともとが素材の硬さなどから選ばれている構造材料です。人体とは異なった素材のため、移植後の生着に長い時間を要し、場合によってはその間に感染症などを引き起こして生着しないこともあります。また、代謝機能もないため、患者の高齢化に伴い劣化や不具合が生じるなどの課題があります。
このような課題を解決する手法として、無機材料の表面にタンパク質を固定化することなどが考えられます。しかし、その方法は限られており、しかも生体親和性が高い方法ではありませんでした。そこで今回、国際共同研究グループは、ムラサキイガイが水中で岩などに接着する性質に注目しました。
研究手法と成果
ムラサキイガイなどの貝類は、水中でも岩場に接着することができます。これは、自身が分泌する粘性物質に含まれる接着タンパク質による作用です。この接着タンパク質は、水中でほとんどすべての物質に強力に接着でき、しかも生体への安全性が高いという、再生医療には理想的な性質を持っています。
国際共同研究グループは、ムラサキイガイの接着性の源であるドーパ(DOPA)と呼ばれる化合物に注目しました。DOPAは、天然のアミノ酸であるチロシン(Y)に水酸基(-OH)が一つ付加した物質で、チロシンよりも水素結合が強くなるため、さまざまな物質に結合できると考えられています。DOPAは、通常の遺伝子組換えによるタンパク質工学だけでは作ることができないため、遺伝子組換え技術と酵素法を組み合わせた新しい方法を取りました。
まず、通常の遺伝子組換え技術により、細胞の成長を活性化させる成長因子タンパク質であるIGF-1のC末端に、DOPAのもとになるチロシンを含むY-K-Y-K-Y配列(K=リシン)の人工ペプチドを導入したIGF-1-Y-K-Y-K-Yを大腸菌で発現させました。次に、酵素チロシナーゼによりチロシンに水酸基を導入してDOPAに変換することで、C末端が接着性ペプチドの成長因子タンパク質「IGF-1-X-K-X-K-X(X=DOPA)」を準備しました(図1)。
続いて、新しく調製したIGF-1-X-K-X-K-Xがチタン表面へどれくらいの強さで結合するか調べるために、 水晶発振子マイクロバランス[2]で計測しました( 図2)。その結果、チロシンからDOPAに変換することで、成長因子タンパク質の結合量が増加することが分かりました。さらに、実際に細胞の増殖が活性化されるか調べるために、チタンプレートにIGF-1-X-K-X-K-Xを固定化して、このプレートの上でNIH3T3(マウス繊維芽細胞[3])の増殖を調べました。IGF-1-X-K-X-K-Xの場合は、チタンプレートに固定化能力のない野生型IGF-1を作用させたときと比べて、約1.8倍の細胞増殖効果が確認されました(図3)。HUVEC(ヒト臍帯静脈内皮細胞)やC2C12(マウス筋芽細胞)などの細胞でも同様に細胞増殖を促進したため、さまざまな細胞の増殖に利用できると考えられます。
また、IGF−1-X-K-X-K-Xは表面に結合しているため、通常の成長因子のように細胞内に取り込まれません。その結果として、細胞伝達系を長期間にわたって活性化し続けることを、細胞情報伝達系の研究から明らかにしました(図4)。
今後の期待
本研究により、活性を保ったまま安全に、成長因子の一種であるIGF-1をチタンに固定化する技術を確立できました。今回は、IGF-1を固定化するタンパク質として用いましたが、人工骨や歯科インプラントには、骨形成タンパク質(Bone Morphogenetic Protein、BMP)などが有効であることが知られています。また、この方法を使えば、チタンの他にも広く一般的な生体材料への固定化も可能です。用途に応じた分子をさまざまな素材に固定化することで、従来よりも優れた生体親和性の人工臓器が生み出されると期待できます。
今後は、本手法の有効性を動物実験などでさらに確認し、最終的にはヒトに対する臨床試験を通して、人工関節や歯科インプラントの生着性の向上を確認します。臨床試験での安全性や効果が確かめられれば、再生医療関連の医薬品としての市販が期待できます。
原論文情報
- Chen Zhang, Hideyuki Miyatake, Yu Wang, Takehiko Inaba,, Yi Wang, Peibiao Zhang and Yoshihiro Ito, "A bioorthogonal approach for the preparation of a titanium-binding insulin-like growth factor-1 derivative using tyrosinase", Angewandte Chemie International Edition
発表者
理化学研究所
主任研究員研究室 伊藤ナノ医工学研究室
国際プログラム・アソシエイト 張 晨(ジャン チェン)
専任研究員 宮武 秀行(みやたけ ひでゆき)
創発物性科学研究センター 超分子機能化学部門 創発生体工学材料研究チーム
チームリーダー 伊藤 嘉浩(いとう よしひろ)
主任研究員研究室 佐甲細胞情報研究室
研究員 稲葉 岳彦(いなば たけひこ)
 伊藤嘉浩、張晨、稲葉岳彦、宮武秀行
伊藤嘉浩、張晨、稲葉岳彦、宮武秀行
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ムラサキイガイ
食用にされる場合にはムール貝とも呼ばれ、足糸(そくし)によって濡れた岩場などに強力に接着できるため、その機構はバイオ接着材としての研究対象にもなっている。 - 2.水晶発振子マイクロバランス
水晶の薄片に物質が吸着した際に、共振周波数が変化することを利用して、吸着量を精密に定量する測定方法。 - 3.繊維芽細胞
結合組織を構成する細胞の一つ。コラーゲン、エラスチン、ヒアルロン酸といった真皮の成分を作り出す。核小体が明瞭な楕円形の核を有し、細胞質は塩基好性を示す。
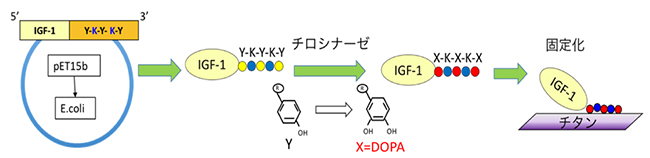
図1 IGF-1への人工ペプチドの導入と接着性ペプチドへの変換
成長因子タンパク質IGF-1のC末端に、遺伝子組換え技術によりY-K-Y-K-Y人工配列(Yはチロシン、Kはリシン)を導入し、IGF-1-Y-K-Y-K-Yを大腸菌で発現させた。次に酵素チロシナーゼ処理により、人工ペプチドを接着性ペプチド(X-K-X-K-X:X=DOPA)に変換し、IGF-1-X-K-X-K-Xをチタンプレートに接着させる。
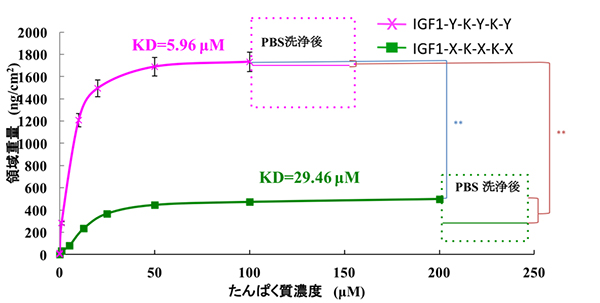
図2 成長因子タンパク質のチタンに対する結合の強さ
使用した成長因子タンパク質濃度と結合量の関係を調べた。緑線はDOPA変換前のIGF-1-Y-K-Y-K-Y、ピンク線はDOPA変換後のIGF-1-X-K-X-K-Xを示す。領域重量(ng/cm2)が増加していることから、DOPA変換によって成長因子タンパク質のチタン表面への結合量が増加したことが分かる。
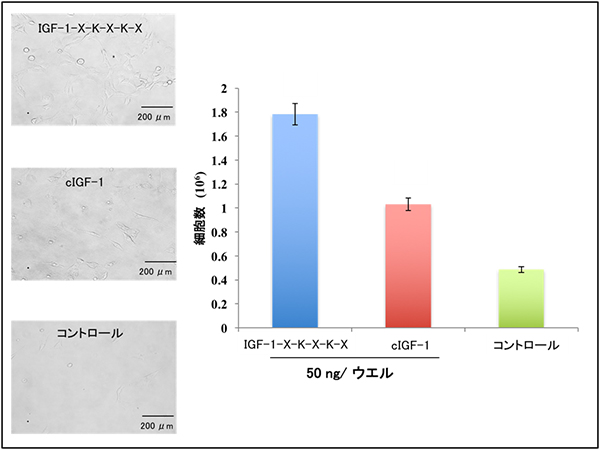
図3 チタンプレートに固定化されたIGF-1の細胞増殖促進活性
50ナノグラム(ng、1ngは10億分の1グラム)のIGF-1-X-K-X-K-Xおよび野生型IGF-1(cIGF-1)をチタンプレートに滴下後、同量のNIH3T3細胞(マウス繊維芽細胞)に暴露させ、24時間培養した。コントロールには、同量のNIH3T3細胞のみを用いた。左は24時間後の培養の様子。右は24時間後の細胞数のグラフ。チタンプレートに固定化されたIGF-1-X-K-X-K-Xの場合は、固定化能力のない野生型IGF-1の場合と比較して、約1.8倍の細胞増殖効果が確認された。
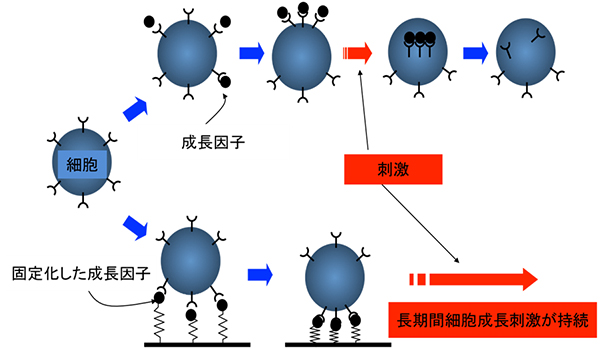
図4 細胞の活性化の長期化
通常、成長因子が細胞に結合すると、成長因子が細胞内に取り込まれるために、細胞成長刺激は短期間にとどまる。これに対して本手法では、成長因子の表面固定化により、細胞内への取り込みが抑制される結果、長期間わたり細胞成長刺激を与えることができる。
