理化学研究所(理研)環境資源科学研究センター天然物生合成研究ユニットの加藤直樹研究員、高橋俊二ユニットリーダーらの研究グループ※は、天然物の生合成経路において、鏡像異性体[1]を作り分ける役割を担っている酵素を発見しました。
本研究成果は、天然物の立体選択性をつかさどる酵素を入れ替えることで、非天然型の環構造を持った天然物誘導体を創出できることを示しており、複雑な骨格を持つ有用天然物の合理的創製に新たな指針を与えると期待できます。
[4+2]環化付加反応[2]を触媒する天然由来の酵素が近年、相次いで発見され、注目を集めています。糸状菌が生産する生物活性物質エキセチン[3]の生合成経路において、立体選択的なデカリン[4](二環性の炭化水素構造)の形成を担う「Fsa2[5]」もその一つです。今回、共同研究グループは、エキセチンと鏡像異性体の関係にある類縁化合物フォマセチン[3]を対象に、その生合成遺伝子を同定し、Fsa2のホモログ[6]である「Phm7」の生合成における役割を明らかにしました。さらに、phm7遺伝子をfsa2遺伝子に置換した遺伝子改変糸状菌を作製することで、非天然型の立体配置[7]を持つフォマセチン誘導体の創製に成功しました。今回の成果は、[4+2]環化付加反応を担う遺伝子の改変によって、非天然型環構造を持つ天然物誘導体の創出に成功した最初の例になります。
本研究は、ドイツの科学雑誌『Angewandte Chemie International Edition』の掲載に先立ち、オンライン版(7月4日付け:日本時間7月5日)に掲載されます。
![[4+2]環化付加反応を触媒する酵素Fsa2とPhm7の図](/medialibrary/riken/pr/press/2018/20180705_1/fig.jpg)
図 [4+2]環化付加反応を触媒する酵素Fsa2とPhm7
※研究グループ
理化学研究所 環境資源科学研究センター
天然物生合成研究ユニット
研究員 加藤 直樹(かとう なおき)
テクニカルスタッフⅠ 衣笠 清美(きぬがさ きよみ)
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
ケミカルバイオロジー研究グループ
研究員 野川 俊彦(のがわ としひこ)
グループディレクター 長田 裕之(おさだ ひろゆき)
先進機能元素化学研究チーム(研究当時)
副チームリーダー 滝田 良(たきた りょう)
(現 東京大学大学院 薬学研究科 准教授)
特別研究員 金井 美紗衣(かない みさえ)
チームリーダー 内山 真伸(うちやま まさのぶ)
(現 開拓研究本部内 山元素化学研究室 主任研究員、東京大学大学院 薬学研究科 教授)
※研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金 新学術領域研究「生物合成系の再設計による複雑骨格機能分子の革新的創成科学(生合成リデザイン)(領域代表:阿部郁朗)」および同基盤研究A「微生物二次代謝遺伝子の改変、覚醒による新規生物活性物質の創出(研究代表者:長田裕之)」による支援を受けて行われました。
背景
[4+2]環化付加反応(ディールス・アルダー反応)は、有機合成化学において最も重要な反応の一つです。近年、天然物の生合成経路において、この反応を触媒する酵素の発見が相次いでいます。2015年に加藤研究員らが発見した、糸状菌が生産するエキセチンの生合成経路において、立体選択的にデカリン(二環性の炭化水素構造)の形成を担う「Fsa2」もその一つです注1)。しかし、これまでに発見された酵素の進化的起源は異なっており、それぞれの生合成経路に特化していることから、酵素機能の全容は明らかになっていません。
Fsa2が関与する直鎖状ポリエンの分子内環化付加反応では、理論的にはデカリンの立体配置が異なる4種類の立体異性体[1]が生成されます(図1A)。天然で見つかっているエキセチン類縁化合物に含まれるデカリンの立体配置は、4種類のうちのどれかと一致します(図1B)。1種類の糸状菌(の生合成経路)からは1種類の立体配置のデカリンを持つエキセチン類縁化合物のみが生産されることから、このグループの天然物の生合成経路には、環化付加反応の立体化学を厳密に制御するメカニズムの存在が予想されました。
研究グループは、Fsa2とそのホモログがその鍵となる役割を担っていると仮定し、Fsa2とそのホモログの構造と機能を比較することで、これらの酵素が複雑な立体配置を持つ天然物の骨格をどのように構築しているのか解明することを目指しました。
注1)2015年4月28日プレスリリース「微生物が特定の形の代謝物を作るために必要な酵素遺伝子を発見」
研究手法と成果
研究グループは、エキセチン類縁化合物の中から、分子内の全ての不斉炭素原子[7]がエキセチンと反対であり、鏡像異性体の関係にあるフォマセチン(図1B)に着目しました。フォマセチンの生合成に関わる遺伝子(phm)クラスターを同定し、そこに含まれるfsa2遺伝子のホモログであるphm7遺伝子の機能を調べました。
まず、フォマセチンを生産する糸状菌(Pyrenochaetopsis sp. RK10-F058株)のゲノムを解読し、生合成に関わる遺伝子(phm遺伝子クラスター)を見いだしました。それらが生合成にどのように関与しているのか調べるために、遺伝子ノックアウト実験[8]を行いました。phm7遺伝子をノックアウト(欠失)したところ、フォマセチンの生産が大幅に低下し、加えて、新たな化合物(図2、右下のcis-デカリン誘導体)の生産が認められました。その化合物の化学構造を調べることで、「Phm7」もまたFsa2と同様に、デカリンの3位、6位の立体制御に関与していることが分かりました。
次に、Phm7が関与する[4+2]環化付加反応について、その反応経路と立体選択性に関するさらなる知見を得るため、密度汎関数計算[9]による解析を行いました。得られた計算結果は、実験で観察された非酵素条件(phm7遺伝子欠失株)での代謝物生産のパターンとよく一致しました。すなわち、理論的に生じる4種類のデカリンの立体配置のうち、2位と11位の立体配置がそれぞれSR表示[7]でのS・Rよりも、R・Sの方が遷移状態[9]の活性化エネルギー[9]が低いため、phm7遺伝子欠失株において検出されたことが分かりました。
また、もしPhm7とFsa2が2位、11位の立体制御にも関与しているのなら、Phm7をFsa2に入れ替えた場合、エネルギー的に不利な立体配置を持つ誘導体を作ることができると考え、これを検証するため、遺伝子置換実験[8]を行いました。フォマセチン生産菌のphm7遺伝子をfsa2遺伝子に置換した遺伝子改変株を作製したところ、phm7遺伝子欠失株で検出された化合物とは異なる立体異性体が生産されました。各種スペクトル分析により、この化合物の化学構造を決定したところ、予想した通り、[4+2]環化付加反応によって生じる4カ所の不斉炭素原子の配置がエキセチン型に反転した異性体(図2、左下のエキセチン型trans-デカリン誘導体)であることが分かりました。
このように、エネルギー的には不利なために非酵素条件ではほとんど検出できない化合物が、Fsa2の導入によって生産されたことから、[4+2]環化付加反応において生じる4カ所全ての不斉炭素原子の立体配置が酵素によって制御されていることが明らかとなりました。
以上のように、[4+2]環化付加反応に関与するFsa2とPhm7を比較することで、これらの酵素がどのように、エキセチンとその類縁化合物のような複雑な立体配置を持つ天然物を生合成しているのか、その一端が明らかになりました。
今後の期待
本研究成果は、複雑な構造を持つ天然物の生合成経路において、[4+2]環化付加反応を担う酵素遺伝子を改変することで、非天然型の誘導体の創出に成功した最初の例になります。
今後は、本酵素がどのように立体選択的な環化付加反応を触媒しているのかを解き明かすことで、複雑な骨格を持つ有用天然物の合理的創製に貢献すると期待できます。
原論文情報
- Naoki Kato, Toshihiko Nogawa, Ryo Takita, Kiyomi Kinugasa, Misae Kanai, Masanobu Uchiyama, Hiroyuki Osada, Shunji Takahashi, "Control of the stereochemical course of [4+2] cycloaddition during trans-decalin formation by Fsa2-family enzymes", Angewandte Chemie International Edition, 10.1002/anie.201805050
発表者
理化学研究所
環境資源科学研究センター 天然物生合成研究ユニット
研究員 加藤 直樹(かとう なおき)
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
産業利用に関するお問い合わせ
補足説明
- 1.鏡像異性体、立体異性体
同じ分子式で表されるが、構造が異なる物質のことを異性体と呼び、原子の並び順が異なる「位置異性体」と、原子の並びは同じでも3次元空間での配置の異なる「立体異性体」に分けられる。右手と左手のように互いに鏡像である立体異性体のことを「鏡像異性体(エナンチオマー)」と呼ぶ。 - 2.[4+2]環化付加反応
共役ジエンにアルケン(ジエノファイル)が付加して6員環構造が生じる反応で、ディールス・アルダー反応とも呼ばれる。天然物の生合成経路において、鎖状構造の中間体から環状構造への変換に、本反応が関与していることが以前より指摘されており、近年、この反応を触媒する酵素が次々に発見されている。 - 3.エキセチン、フォマセチン
エキセチン(分子量373)は、フザリウム属糸状菌より単離された二次代謝物。グラム陽性細菌に対する抗菌活性、およびHIV-1インテグラーゼに対する阻害活性を示すことが知られている。フォマセチン(分子量413)は、エキセチンと鏡像異性体の関係にあるものの、同様の生物活性(HIV-1インテグラーゼ阻害活性など)を示すことが報告されている。 - 4.デカリン
二環性の炭化水素化合物。別名デカヒドロナフタレン。その構造から trans-デカリンと cis-デカリンに大別できる。 - 5.Fsa2
エキセチンの生合成経路において、特定の立体配置のデカリン構造を形成する反応([4+2]環化付加反応)を触媒する酵素。これまでの研究により、Fsa2は[4+2]環化付加反応において、3位と6位の立体配置を制御することで、特定のデカリン環形成を触媒することが明らかにされている。 - 6.ホモログ
共通の祖先を持つ遺伝子(あるいはタンパク質)。遺伝子(アミノ酸)配列が似ていることから、同様の機能を担っていることが推定できる。 - 7.立体配置、不斉炭素原子、 RS表示
異なる四つの置換基が共有結合している炭素原子のことを「不斉炭素原子」と呼び、その四つの置換基の空間的配列を「立体配置」と呼ぶ。不斉炭素原子を含む分子には、鏡像異性体が存在する。鏡像異性体の立体配置の違いを表記する方法の一つが「 RS表示法」であり、四つの置換基の命名法における優先順位に基づいて R、または Sと表記する。分子の中に複数の不斉炭素原子がある場合は、その一つ一つに、 Rまたは Sを表示する。 - 8.遺伝子ノックアウト実験、遺伝子置換実験
「遺伝子ノックアウト」実験は、遺伝子の機能を失わせることで、その遺伝子の生体内での機能や役割を調べる遺伝子組換え実験手法。今回の研究では、生物が本来持っている機能である「相同組み換え」(ゲノム中のDNA配列がよく似た部分同士で入れ換えを起こすシステム)を利用することで、調べたい遺伝子を外来の遺伝子と入れ換え、ゲノムから完全に削除した遺伝子欠失株を作製した。通常、外来遺伝子として抗生物質耐性遺伝子を用いることで、その抗生物質を含む培地で培養すると、ノックアウトが起きている細胞を選別することができる。「遺伝子置換」実験では、抗生物質耐性遺伝子に加え、機能を知りたい遺伝子を一緒に組み込むことで、削除した遺伝子の代わりに導入した遺伝子の機能を知ることができる。 - 9.密度汎関数計算、遷移状態、活性化エネルギー
「密度汎関数計算」は、原子や分子などの物性を明らかにする量子化学計算手法の一つ。例えば、今回の研究では分子の構造変化のエネルギーを明らかにし、各反応経路の検証に用いられている。また、反応が進行する際に最もエネルギーが高い状態を「遷移状態」と呼び、基底状態とのエネルギー差が「活性化エネルギー」である。遷移状態は、エネルギーが高く不安定なため実験的には観測は困難であるが、量子化学計算によりその構造を見ることができる。密度汎関数法は、正確なエネルギーが電子密度の汎関数(関数の関数)として一意的に定められているというHohenberg-Kohn定理に基づいている。計算コストに対して、比較的良い計算精度が得られることから、近年化学分野で広く活用されている。
![[4+2]環化付加反応で生じる四つの立体異性体とエキセチンとその類縁化合物の図](/medialibrary/riken/pr/press/2018/20180705_1/fig1.jpg)
図1 [4+2]環化付加反応で生じる四つの立体異性体とエキセチンとその類縁化合物
- A) 直鎖状のポリエンから、[4+2]環化付加反応によってデカリン構造ができる反応を模式的に表したもの。反応によって生じる環構造を赤色で示した。理論的に生じる4種類の立体異性体の構造の違いは、4カ所の不斉炭素原子(2, 3, 6, 11位)の配置(S体、またはR体)で表すことができる。大きく6位と11位の置換基の水素が、トランス型のtrans-デカリンとシス型のcis-デカリンに分けられる。
- B) 天然で見つかっているエキセチンとその類縁化合物の化学構造。これらの化合物のデカリンの立体配置は上記の4種類のいずれかに一致する。今回の研究では、trans-デカリンを持つエキセチンとフォマセチンを対象とした。
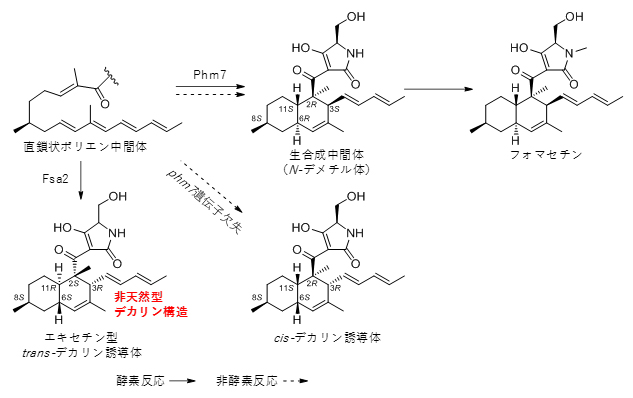
図2 酵素Phm7、Fsa2の作用によって生じたデカリンの構造
上段が本来の生合成で、Phm7の作用により直鎖状ポリエン中間体から(2R,3S,6R,11S)の立体配置のデカリン(生合成中間体)が形成される。phm7遺伝子欠失株、すなわち非酵素条件では、酵素条件で生成された生合成中間体と、3位と6位の立体配置が反転したcis-デリカン誘導体(2R,3R,6S,11S:右下)が検出された。phm7遺伝子をfsa2遺伝子に置換した遺伝子改変株では、4カ所の立体配置がすべて反転したエキセチン型transデリカン誘導体(2S,3R,6S,11R:左下)が検出された。これは、8位の置換基のメチル基がS体であり、天然には存在しない非天然型のデカリン構造をしている。
