要旨
理化学研究所(理研)環境資源科学研究センター触媒・融合研究グループの袖岡幹子グループディレクター、河村伸太郎特別研究員の研究チームは、安価で入手容易なペルフルオロ酸無水物[1]をペルフルオロアルキル源に用いて、アルケン[2]類からペルフルオロアルキル化合物[3]を合成する反応の開発に成功しました。
CnH2n+1からなるアルキル基の水素(H)がすべてフッ素(F)に置き換わったペルフルオロアルキル基[3]を分子内に持つ有機化合物(ペルフルオロアルキル化合物)は、高い脂溶性を持ち、代謝に対する安定性を示すことが知られており、医薬品候補群、農薬として注目されています。このため、研究チームを含む国内外の多数の研究グループによって、ペルフルオロアルキル基を有機化合物に導入する合成反応の開発が盛んに行われています。しかし、現在報告されている手法のほとんどが、高価なペルフルオロアルキル源を必要とするため、コストや安全面で実用性に課題がありました。
今回、研究チームは、トリフルオロ酢酸無水物などのペルフルオロ酸無水物を用いて、トリフルオロメチル化合物などのペルフルオロアルキル化合物を効率良く簡便に合成する新しいアルケン類のペルフルオロアルキル化反応を開発しました。本手法は安価で入手容易なペルフルオロ酸無水物を用いることができるため、実用性に優れています。さらに、得られた生成物はペルフルオロ基を持つ「ビルディングブロック[4]」として有用であり、今後、医薬品や農薬の開発が促進されると期待できます。
本研究の内容は、ドイツの科学雑誌『Angewandte Chemie International Edition』オンライン版(6月2日付け)に掲載されます。
背景
トリフルオロメチル基を主としたペルフルオロアルキル基を持つ化合物は、多くの医薬品候補群や農薬にみられます。これは、最も高い電気陰性度をもち、安定な炭素-フッ素結合を形成するというフッ素原子のユニークな性質によって化合物の物性や代謝安定性が向上し、生体内における吸収や排泄といった薬物動態を改善できるためです。ペルフルオロアルキル基を有機化合物の炭素骨格に導入することは、少量の投与で効能の高い医薬品、農薬を開発するために有効な方法であるといえます。このため、近年ペルフルオロアルキル基を有機化合物に直接導入する化学反応の開発が盛んに行われており、研究チームもこれまでにペルフルオロアルキル化反応の1つであるトリフルオロメチル化反応の開発に関する論文を発表しています注1)。
しかし、新しいペルフルオロアルキル化反応が続々と開発されている一方、医薬品、農薬の開発のような実際の場面での同反応の応用は限られていました。これは、ペルフルオロアルキル源が、高価であったり安全な取り扱いに注意を要することが原因の1つであると考えられます。
今回、研究チームは、安価かつ工業的に大量生産されており、入手が容易で安定なトリフルオロ酢酸無水物などのペルフルオロ酸無水物を用いて、アルケン類からトリフルオロメチル化合物などのぺルフルオロアルキル化合物を合成する反応の開発を試みました(図1)
注1)
総説:
(a) H. Egami, M. Sodeoka, Angew. Chem. Int. Ed.2015, 53, 8294.
原著論文:
(b) R. Shimizu, H. Egami, Y. Hamashima,M. Sodeoka, Angew. Chem. Int. Ed.2012, 51,4577.
(c) H. Egami, R. Shimizu, S. Kawamura, M. Sodeoka, Angew. Chem. Int. Ed.2013, 125, 4092.
(d) H. Egami, S. Kakawamura, A. Miyazaki, M. Sodeoka, Angew. Chem. Int. Ed.2013, 52, 7841.
(e) S. Kawamura,H. Egami, M.Sodeoka, J. Am. Chem. Soc.2015, 137, 4865.など
研究手法と成果
研究チームは、はじめにペルフルオロ酸無水物と尿酸—過酸化水素から活性の高い(ジアシル)ペルオキシド[5]を発生させた後、同一フラスコにアルケンを加えて加熱することで反応させました。しかし、反応は非常に遅く、複雑な混合物が生成されることが分かりました。そこで、研究チームは銅を触媒として添加したところ、二重結合の移動を伴うペルフルオロアルキル化であるアリルペルフルオロアルキル化反応が選択的に進行し、高収率で生成物が得られることを発見しました(図2上)。
また、炭素鎖の適切な位置(二重結合の端の炭素からみて、4または5番目の炭素)にベンゼン環などの芳香環を持つアルケンを用いて反応を行った場合、銅触媒がなくてもペルフルオロアルキル基の導入と炭素環の形成が同時に進行する反応であるカルボペルフルオロアルキル化反応が進行することも見出しました。カルボペルフルオロアルキル化反応では、アルケンの二重結合から4番目に芳香環がある場合は5員環の炭素環が、5番目に芳香環がある場合は6員環の炭素環が形成されました(図2下)。
これらの生成物は銅触媒の有無によって作り分けることができます。研究チームが開発した方法は、さまざまなアルケンを用いることができ、高い効率で目的の生成物を得ることができるためペルフルオロアルキル化合物の製造方法として非常に有用です。
今後の期待
研究チームは、ペルフルオロ酸無水物を活用したアルケン類のペルフルオロアルキル化反応の開発に成功しました。従来のアルケン類のペルフルオロアルキル化手法では高価なペルフルオロアルキル源を必要としていましたが、本研究では安価で入手容易な酸無水物を用いることでき、実用性に優れます。さらに、得られた生成物はペルフルオロ基を持つ「ビルディングブロック」として有用であり、今後ペルフルオロアルキル基を持つ医薬品や農薬の開発を促進すると期待できます。
原論文情報
- Shintaro Kawamura, Mikiko Sodeoka, "Perfluoroalkylation of Unactivated Alkenes with Acid Anhydrides as the Perfluoroalkyl Source", Angewandte Chemie International Edition, doi: 10.1002/anie.201604127
発表者
理化学研究所
環境資源科学研究センター 触媒・融合研究グループ
グループディレクター 袖岡 幹子(そでおか みきこ)
(袖岡有機合成化学研究室 主任研究員)
特別研究員 河村 伸太郎(かわむら しんたろう)
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.ペルフルオロ酸無水物
ペルフルオロアルキル基を持つカルボン酸が脱水縮合して形成したもの。特に、研究チームが用いたトリフルオロ酢酸無水物(TFAA)は工業的に大量生産されており非常に安価で手に入りやすい。 - 2.アルケン
C=C二重結合を持つ炭化水素化合物の総称。 - 3.ペルフルオロアルキル化合物、ペルフルオロアルキル基
CnH2n+1からなるアルキル基の水素(H)がすべてフッ素(F)に置き換わったものをペルフルオロアルキル基、これを分子内にもつ化合物をペルフルオロアルキル化合物と呼ぶ。 - 4.ビルディングブロック
医薬や農薬の多くは複雑な化学構造をした有機化合物であり、通常はプラモデルや積み木のように複数の部品を組み立てて目的の分子をつくる必要がある。このとき部品に相当する小さく化学変換しやすい分子をビルディングブロックと呼ぶ。 - 5.ペルオキシド
O-O結合を持つ分子の総称。
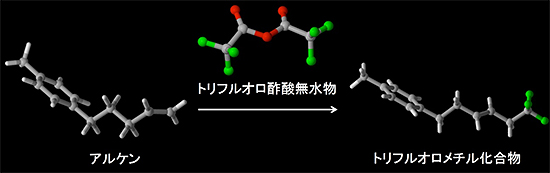
図1 トリフルオロ酢酸無水物を用いるアルケンのトリフルオロメチル化反応
安価で入手容易なトリフルオロ酢酸無水物を用いて、アルケン類からトリフルオロメチル化合物を合成する反応の開発を試みた。上図で、緑、灰、赤、白の球は、それぞれフッ素(F)、炭素(C)、酸素(O)、水素(H)を表している。
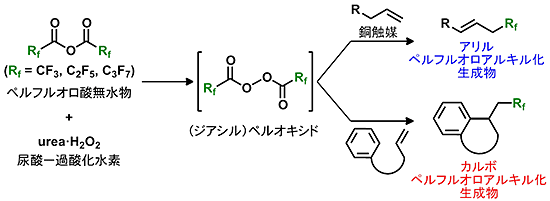
図2 銅触媒アリルペルフルオロアルキル化反応とカルボペルフルオロアルキル化反応
銅を触媒とした場合、二重結合の移動を伴うペルフルオロアルキル化反応が進行する(上)。炭素鎖の適切な位置(二重結合の端の炭素からみて、4または5番目の炭素)に芳香環を持つアルケンを用いた場合は無触媒で炭素環(5員環または6員環)の構築を伴うペルフルオロアルキル化反応が進行する(下)。
