要旨
理化学研究所(理研)統合生命医科学研究センター循環器疾患研究グループの田中敏博グループディレクター、医科学数理研究グループの角田達彦グループディレクター、重水大智研究員および国立循環器病研究センターの相庭武司医長、日本医科大学の清水渉教授らによる共同研究グループは、全エクソームシークエンス解析[1]によってカルモジュリン結合遺伝子がQT延長症候群[2]の発症に関与している可能性があることを発見しました。
QT延長症候群は、突然死を引き起こす可能性がある難治性の遺伝性不整脈疾患で、約2,000人に1人の頻度で発症することが知られています。これまでに少なくとも15種類の原因遺伝子が報告されていますが、約2割の患者は既知の原因遺伝子に変異が認められず、新たな原因遺伝子の解明が急務となっていました。
そこで共同研究グループは、既知の原因遺伝子に変異が認められなかった発端者[3]とその血縁者120例と、その血縁に属さない発症者138例の計258例に対して、次世代シークエンサー[4]とスーパーコンピュータを用いて全エクソームシークエンス解析を行い、新たな原因遺伝子の同定を試みました。解析の結果、原因遺伝子の候補となった遺伝子と、既知の原因遺伝子との関連性を調べ、発症者と非発症者との関連解析[5]を行った結果、11種の原因遺伝子の候補を同定しました。また、同定した遺伝子について変異の有無を確認したところ、見つかった変異のほとんどはカルモジュリン結合遺伝子で確認されました。
本研究により、カルモジュリン結合遺伝子がQT延長症候群の発症に関与している可能性があることが分かりました。原因遺伝子の候補となった11種の遺伝子は今後、詳しい機能解析によりQT延長症候群の新規原因遺伝子として同定されることが期待できます。また、今回の発見がQT延長症候群の機序の理解に貢献し、今後の発症メカニズム解明の手がかりになることが期待できます。
本研究は、米国のオンライン科学雑誌『PLOS ONE』(7月1日付け:日本時間7月2日)に掲載されます。
背景
QT延長症候群は、突然死を引き起こす可能性がある難治性の遺伝性不整脈疾患で、約2,000人に1人の頻度で発症することが知られています。これまでに少なくとも15種類の原因遺伝子が報告されており、そのほとんどが、カリウム、カルシウム、ナトリウムチャネルといった膜貫通タンパク質の一種であるイオンチャネルと、それらと関連のある遺伝子群であることが分かっています。しかし、約2割のQT延長症候群患者は既知の原因遺伝子に変異が認められません。QT延長症候群の全容を解明するためには、新たな原因遺伝子の解明が急務となっています。一方、近年のDNA解読技術の目覚ましい発展に伴い、次世代シークエンサーとスーパーコンピュータを駆使することで、疾患の原因となる変異を包括的に解析することが可能になりました。特に、対象を遺伝子コード領域(エクソーム)に絞ることでより高精度なDNA解読を可能にした全エクソームシークエンス解析は、すでにさまざまな疾患の原因となる変異を解明しています。
そこで、共同研究グループは、全エクソームシークエンス解析を用いてQT延長症候群の新規原因遺伝子の探索を進めました。
研究手法と成果
共同研究グループは、QT延長症候群の既知の原因遺伝子に変異が認められなかった35例の発端者とその血縁者からなる計120例(59例の発症者と61例の非発症者)の血液からDNAを抽出し、全エクソームシークエンス解析を行いました。QT延長症候群の発症に関与していると思われる変異を選定するため、まず、疾患と関連がない一塩基多型(SNP)[6]を除外しました。次に、家系図から推定される遺伝形式[7]に従うアミノ酸置換を伴った変異[8]に着目しました。その結果、88種の遺伝子から92個の変異を同定しました。同定した変異について、既知の原因遺伝子との関連性から10種(図1)、発症者と非発症者との関連解析から1種、合計11種の遺伝子をQT延長症候群の原因遺伝子の候補として同定しました。また、この11種のうち5種はカルモジュリンと相互作用する遺伝子でした。この割合は、全遺伝子のうちカルモジュリンと相互作用する遺伝子の割合と比べて統計学的に有意に多く、QT延長症候群とカルモジュリンに相互作用する遺伝子には、強い関連があることが分かりました。
さらに、同定した11種の遺伝子について既知の原因遺伝子に変異が認められなかった発端者とその血縁に属さない発症者138例を用いて変異を確認したところ、QT延長症候群の発症に関与していると思われる変異を新たに16個同定しました。そのうちの14個がカルモジュリン結合遺伝子で確認され、QT延長症候群の発症においてカルモジュリン結合遺伝子が重要な役割を担っている可能性があることが示唆されました。また、リアノジン受容体(RYR2)遺伝子では9ヵ所で変異が同定され、RYR2遺伝子に変異を持つ9症例は全て若年発症かつその家族は非発症者であるという特徴が確認されました。また、RYR2遺伝子に変異を持つ発症者の多くは運動時に失神や心室細動が出現し、その他のQT延長症候群発症者と比べて重篤な不整脈を発症する傾向があることが分かりました。
今後の期待
共同研究グループは、全エクソームシークエンス解析によってカルモジュリン結合遺伝子がQT延長症候群の発症に関与している可能性があることを発見しました。原因遺伝子の候補となった11種の遺伝子は今後、詳しい機能解析によりQT延長症候群の新規原因遺伝子として同定されることが期待できます。また、今回の発見がQT延長症候群の機序の理解に貢献し、今後の発症メカニズム解明の手がかりになることが期待できます。
原論文情報
- Daichi Shigemizu, Takeshi Aiba, Hidewaki Nakagawa, Kouichi Ozaki, Fuyuki Miya, Wataru Satake, Tatsushi Toda, Yoshihiro Miyamoto, Akihiro Fujimoto, Yutaka Suzuki, Michiaki Kubo, Tatsuhiko Tsunoda, Wataru Shimizu and Toshihiro Tanaka, "Exome analyses of long QT syndrome reveal candidate pathogenic mutations in calmodulin-interacting genes", PLOS ONE, doi: 10.1371/journal.pone.0130329
発表者
理化学研究所
統合生命医科学研究センター 循環器疾患研究グループ
グループディレクター 田中 敏博(たなか としひろ)
統合生命医科学研究センター 医科学数理研究グループ
グループディレクター 角田 達彦(つのだ たつひこ)
研究員 重水 大智(しげみず だいち)
国立循環器病研究センター 心臓血管内科部門 不整脈科
医長 相庭 武司(あいば たけし)
日本医科大学大学院医学研究科 循環器内科学分野
教授 清水 渉(しみず わたる)
(国立循環器病研究センター 心臓血管内科 客員部長)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
国立循環器病研究センター広報担当
Tel: 06-6833-5012 / Fax: 06-6833-9865
kouhou [at] ml.ncvc.go.jp(※[at]は@に置き換えてください。)
補足説明
- 1.全エクソームシークエンス解析
全染色体(ゲノム)のうち、1~2%のタンパク質をコードする領域について、次世代シークエンサーを用いて個人レベルの変異を検出する解析手法。 - 2.QT延長症候群
致死性不整脈を発症して心臓突然死の原因となる疾患。心電図検査時のQT波形が正常に比べて長いという特徴がある。詳細は、国立循環器病研究センター「 遺伝性不整脈疾患の遺伝子診断」 - 3.発端者
ある家系で、ある遺伝性疾患に初めて注意が向けられるきっかけとなった、臨床的に罹患した個人のこと。 - 4.次世代シークエンサー
現在使用されている次世代シークエンサーの基本原理は、解析対象のDNAを細かく断片化し、それらを超並列に解読することである。(超)並列シークエンサーとも呼ばれる。断片化したものの端から配列決定したものをリードという。このリードは一般的に短い(本研究では100塩基のリードが多い)。断片化したDNAの両端から読んだリードの対をペアエンドリードという。ヒトゲノムの全配列約30億塩基対を1,000ドル以下のコストで解読すべく、欧米の政府や企業の技術開発が日々進んでいる。 - 5.関連解析
ある疾患の患者(ケース)と、罹患していない被験者(コントロール群)の間で、頻度に差があるかどうかを統計的に検定し、疾患と関連する遺伝子を見つける方法の1つ。本研究ではアミノ酸置換を伴う変異を用いて遺伝子単位でこの解析を使用した。 - 6.一塩基多型(SNP)
ヒトゲノムの全配列約30億塩基対は、1人ひとりを比較するとその塩基配列に違いが見られる。このうち、集団内での頻度が1%以上のものは遺伝子多型と呼ばれる。その代表的なものとして一塩基多型(SNP; Single Nucleotide Polymorphism)がある。 - 7.遺伝形式
遺伝性疾患の遺伝形式には、常染色体優性遺伝、常染色体劣性遺伝、X連鎖優性遺伝、X連鎖劣性遺伝、 de novo変異があげられる。家系内の発症者と非発症者の関係からこの遺伝形式は推定される。家系解析で遺伝形式を推定する場合、変異を持っている場合に実際に発症する率(浸透率)を100%と仮定する場合が多い。 - 8.アミノ酸置換を伴った変異
DNA配列が置換されることによって、対応するアミノ酸が変化する非同義置換とアミノ酸が変化しない同義置換の2種類がある。非同義置換は、タンパク質機能の低下や機能欠如、異常タンパク質の出現などにつながる場合もある。
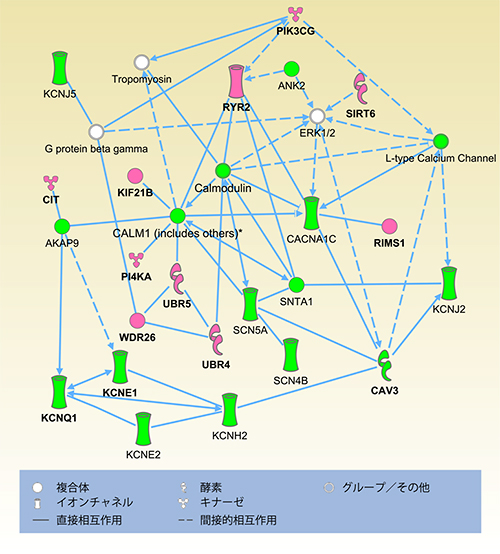
図1 既知原因遺伝子と候補原因遺伝子との相互作用ネットワーク
緑はQT延長症候群における既知の原因遺伝子、ピンクが今回同定した原因遺伝子の候補となる遺伝子を表している。原因遺伝子の候補となる遺伝子の多くが既知の原因遺伝子と相互作用している。
