ポイント
- 生きたまま体細胞クローン胚の染色体を60時間連続観察することに成功
- 体細胞クローン作製成功率が低い主な原因は卵割時の染色体分配異常であると判明
- 正常な体細胞クローン胚を移植することで成功率が大幅に向上する可能性を示唆
要旨
独立行政法人理化学研究所(野依良治理事長)は、マウスを用いて体細胞クローン胚※1の発生開始から着床期直前まで生きたまま連続観察する技術を開発し、クローン作製成功率の低い決定的な要因の1つが、初期卵割※2過程における染色体分配異常(ACS:Abnormal chromosome Segregation)であることを実験で突き止めました。これは理研発生・再生科学総合研究センター(竹市雅俊センター長)ゲノム・リプログラミング研究チーム(若山照彦チームリーダー)の山縣 一夫研究員(現大阪大学・微生物病研究所特任准教授)、水谷 英二研究員(現理研BRC遺伝工学基盤技術室協力研究員)らによる研究成果です。
体細胞クローンは、1997年のクローン羊「ドリー」誕生の報告以来、畜産分野をはじめ多くの分野への応用が期待されています。しかし、その成功率は著しく低いのが現状です。これまで、その原因を調べるために、胚の遺伝子発現解析※3や各種分子の局在解析など多くの研究が行われてきました。しかし、これらの方法は胚を固定・破壊しなければならず、見つかった異常が最終的な個体発生にどのように影響するのかは分かりませんでした。
そこで研究チームは、胚を傷つけずに長時間観察できる新しい「ライブセルイメージング技術※4」を開発し、産仔へ発育した体細胞クローン胚の卵割過程を初めて連続画像(動画)で確認することに成功しました。この映像を基に産仔が産まれる条件を遡って解析したところ、体細胞クローン胚は、少なくとも8細胞期までの卵割において染色体分配が正常に保たれる必要があることが分かりました。逆に、全体の80%近くは8細胞期までに少なくとも1度は分配異常を起こしており、産仔は全く産まれないことを確認しました。以上から、体細胞クローン作製の成功率が低い決定的な要因の1つは、初期胚発生に起こる染色体分配異常にあることが明らかになりました。
本成果により、初期胚の段階で正常に産まれるクローン胚を見分けることが可能になりました。これによってクローン作製の成功率を大幅に向上させる可能性があるだけでなく、染色体分配異常がある胚とない胚を比較した研究を進めることで、初期化異常※5の原因解明が期待できます。
本研究成果は、米国の科学雑誌『Developmental Biology』に最終版が近日掲載予定です。
背景
体細胞クローン技術とは、体細胞から個体を作りだす技術であり、絶滅動物、絶滅危惧種の復活や保存、畜産・医療分野における有用家畜の効率的な生産、さらには基礎生物学における核の初期化メカニズムの研究への応用が期待されています。しかし、1997年に世界で初めて哺乳類の体細胞クローンとなるクローン羊「ドリー」の作製が報告されてから15年以上たちますが、その成功率はいまだに低いままです。その原因を探り、作製の成功率を改善するため、多くの研究が行われてきました。これまでに研究チームは、体細胞クローン胚のゲノムの状態を正常化することで、作製効率の向上に成功しています。しかし、正常胚レベルにまで改善したとはいえず、そのほかにも大きな原因があると考えられています。
これまで原因が特定できなかった主な理由に、実験手法の難しさがあります。まず、クローンに用いる体細胞核移植自体、熟練した技術が必要です。卵子は培養細胞とは異なり増えないので、物質を抽出して解析するような生化学的・分子生物学的手法を用いるのは大変困難です。また、染色法のような細胞を固定・破壊してしまう解析方法では、ある時点での体細胞クローン胚が異常を示しても、その後の発生過程を追えないのでそれがどのように個体発生に影響するのかは分かりません。さらに、同一の体細胞クローン胚であっても個々の性質が少しずつ異なっており、そのうち個体にまで発生できるものはごく一部です。従って、複数の胚を混ぜてしまう解析では意味がありません。そこで、作製成功率が低い主な原因を探るためには、体細胞クローン胚を1つずつ識別し、胚発生開始から産仔まで追跡し続ける必要がありました。
研究チームは、ライブセルイメージング技術を用いて、1つ1つの体細胞クローン胚を発生開始から着床期直前まで連続的に観察し、その後、その胚を個別に移植することで、観察した現象と作製率を直接結びつけた解析ができると考えました。解析対象として、近年、生殖医療分野において不妊の主な原因と指摘されている胚の染色体の異常性に着目しました。しかし、サンプルに対して繰り返し紫外線などの光を照射する従来のイメージング技術では、観察後の細胞が死んでしまいます。そこで、できる限り体細胞クローン胚を傷つけないイメージング技術の構築に挑みました。
研究手法と成果
雌マウスから採取した未受精卵に、核・染色体は赤色に、紡錘体※6は緑色にそれぞれ染める蛍光プローブを注入しました。その後卵子の核を除き、代わりに卵丘細胞※7由来の細胞核を注入しました(体細胞核移植)。発生開始後に研究チームが開発したライブセルイメージング技術を使って桑実胚※8・胚盤胞期※8までの3日間、連続的かつ3次元的に染色体の動きを観察し続けました。得られた画像情報を基に1つ1つの胚についてその特徴を把握し、個別に偽妊娠マウス※9に移植して体細胞クローンマウスが産まれるか調べました(図1)。
このライブセルイメージング技術では、ダメージの要因である過剰な蛍光タンパク質を減らすため、胚での発現量を可能な限り少なくするとともに、励起光(レーザー)の照射を最小限にしても蛍光を最大限検出するような光学機器群を採用しました。レーザー強度、露光時間、照射間隔などについても最適条件を設定しました。また、顕微鏡上という環境であっても温度やガス濃度などを長時間にわたって安定的に保持できるようにしました。こうした改良を加え「胚発生にやさしい」イメージング技術を開発し、体細胞クローン胚の発生を60時間近く連続観察することに成功しました(図2)。また、解析後の胚からでもクローンマウスが産まれることも確認しました。
撮影した動画を詳細に解析したところ、8細胞期までの卵割過程において80%近くのクローン胚が、少なくとも1度は染色体分配の異常を起こしていることが明らかとなりました。16細胞期までに1度も異常を起こさない胚は、8.9%しかありませんでした(図3)。
次に、このような染色体分配異常を起こした胚について、異常が起きたステージごとに区別し、それらを個別に偽妊娠マウスに移植することで、染色体分配異常が体細胞クローン作製に与える影響を検討しました(図4)。その結果、8細胞期までの卵割過程の間に1回でも染色体分配異常を起こした胚からは、クローンマウスは得られませんでした。また、8細胞期から16細胞期の間に染色体分配異常を起こした胚からは2.5%、16細胞期までの間に1度も分配異常を起こさなかった胚からは7.1%の確率で産まれていることから、8細胞期までに起きる染色体分配異常が、体細胞クローンを作製できない決定的な要因の1つであると分かりました。
この結果を確認するため、実験に用いた体細胞クローン胚から72個を無作為に選び、それぞれ1匹ずつの偽妊娠マウスに移植しました。最終的に3匹のクローンマウスが得られ、それらのもとになった体細胞クローン胚の卵割過程を遡って解析した結果、いずれのクローン胚も8細胞期まで染色体分配異常は見られませんでした(図5)。
今後の期待
今回、開発した「胚発生にやさしいライブセルイメージング技術」により、生きた体細胞クローン胚の発生過程の解析とその作製率を直接的な相関性を持って調べることに成功し、体細胞クローン作製成功率の低い決定的な要因の1つは、染色体分配異常に起因することを証明しました。これまで不可能であった解析を可能にしたという意味で、この技術開発自体が科学的に重要な成果です。また、これにより初期胚の段階で将来個体になる可能性があるクローン胚と致死の胚を見分けることが可能になり、体細胞クローン作製の成功率が大幅に向上する可能性があります。
染色体分配異常という核や遺伝子構造レベルの大きな異常が主な原因であったという知見は、これまでの常識をくつがえす非常に重要な結果です。今後、その原因を詳細に調べ、染色体の正常性を維持できるような機構の創出に結びつけていくことができれば、さらに効率的な体細胞クローンの作製につながります。また、近年の生殖医療研究の進展により、不妊の原因の多くは、初期胚の染色体安定性維持能力の低下である可能性が指摘されています。「胚発生にやさしいライブセルイメージング技術」は、生きたままの胚の染色体を評価することが可能であり、不妊の原因究明などにも応用できるため、生殖医療分野への貢献も期待できます。
原論文情報
- Eiji Mizutani, Kazuo Yamagata*, Tetsuo Ono, Satoshi Akagi, Masaya Geshi and Teruhiko Wakayama. “Abnormal chromosome segregation at early cleavage is a major cause of the full-term developmental failure of mouse clones.” Developmental Biology.2012 doi: 10.1016/j.ydbio.2012.01.001
発表者
理化学研究所
バイオリソースセンター 遺伝工学基盤技術室
協力研究員 水谷 英二(みずたに えいじ)
Tel: 029-836-9167 / Fax: 029-836-9172
大阪大学微生物病研究所
生体応答遺伝子解析センター
特任准教授 山縣 一夫(やまがた かずお)
Tel: 06-6879-8375 / Fax: 06-6879-8376
お問い合わせ先
神戸研究推進部広報・国際化室
Tel: 078-306-3092 / Fax: 078-306-3090
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.体細胞クローン胚
あらかじめ核を取り除いた卵子に、ドナーとなる体細胞の核を入れ替えて作った胚。この胚が発生すればドナー細胞と同じ遺伝子を持つ子ども(クローン)が産まれる。 - 2.卵割
受精や人工的な刺激により発生を開始した胚が起こす体細胞分裂。初めは1つの細胞である胚が2つに分割し、さらにその2つが分割され細胞の数が倍に増えてゆく。卵割により生じた1つ1つの細胞を割球という。 - 3.遺伝子発現解析
細胞内でどのような遺伝子が働いているのかを調べる方法。マイクロアレイ法やRT-PCR法などが知られている。この方法により正常胚とクローン胚を比べることで、両者の性質の違いを見ることができる。 - 4.ライブセルイメージング技術
細胞内の分子や構造の時間変化を生きたまま観察する技術。オワンクラゲ由来の蛍光タンパク質(下村脩博士が発見し、2008年にノーベル化学賞受賞)を目的とするタンパク質と結合させた蛍光プローブを作製し、それを細胞内に導入する。その細胞を顕微鏡下で培養しながら継時的に蛍光観察する。 - 5.初期化異常
体細胞クローン技術では、分化した細胞である体細胞核の情報が卵子の中でリセットされ、通常の受精卵のようなまっさらな状態にもどると考えられている。このリセットを初期化というが、その実態はいまだ不明な部分が多い。この過程で起きている何らかの失敗、すなわち初期化異常が体細胞クローン作製の成功率が低い原因と考えられている。 - 6.紡錘体
細胞分裂の際に染色体の周りに形成され、染色体分配を行う細胞内構造。 - 7.卵丘細胞
卵子を取り囲んでいる顆粒層細胞。卵子とはゆるく結合しており、卵子の成熟、生存に重要な役割を果たしている。採卵時に卵子とともに採取できる体細胞であるため、ドナー細胞としてクローン研究によく用いられる。 - 8.桑実胚、胚盤胞期
胚が卵割を繰り返していく過程でみられる発生ステージ。マウスの場合桑実胚は、発生開始から3日目ほど進んだ状態で、おおむね16細胞期に相当する。見た目が桑の実のような見ためこういわれる。胚盤胞期は、さらに分裂がすすんだ4日目から5日目の状態で、卵割腔と呼ばれる空洞ができ、将来体をつくる内部細胞塊と胎盤をつくる栄養膜細胞とに分かれる。 - 9.偽妊娠マウス
精管結紮したオスマウスとの交配や電気刺激などにより、実際は妊娠していないが、妊娠したような状態になったメスマウスのこと。このマウスの卵管や子宮に体外培養した胚を移植することで産仔を得る。仮腹ともいわれる。
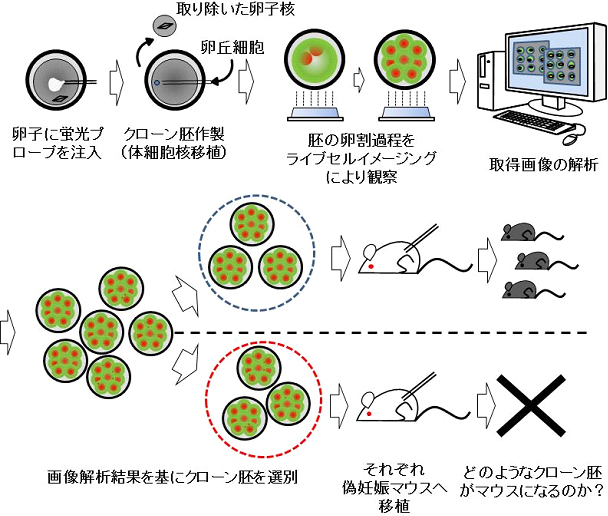
図1 ライブセルイメージング技術を使ったクローン胚の解析
細胞分裂を可視化する蛍光プローブを未受精卵に注入し、その卵子を使って卵丘細胞由来のクローン胚を作る。このクローン胚が卵割する際の染色体の動きを、独自に開発した「胚発生にやさしいライブセルイメージング技術」を用いて1細胞期から桑実胚・胚盤胞期胚まで3次元的に連続観察する。次に、取得した連続画像(動画)を基にクローン胚を選別し、個別に偽妊婦メスへ移植する。それぞれの体細胞クローン胚がマウスになるのか調べることで、体細胞クローン胚で起きている現象と個体発生の相関性を直接的に解析できる。
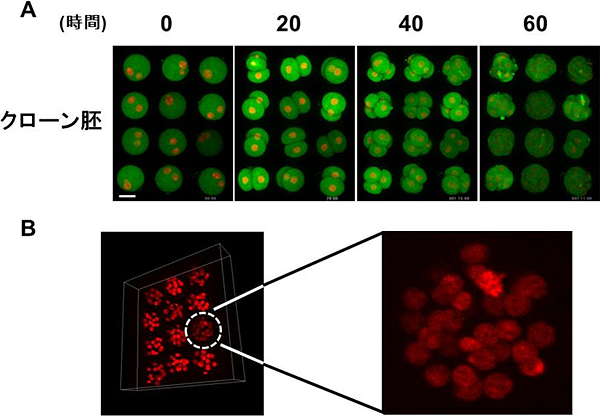
図2 ライブセルイメージングによって得られた画像例
- A: 体細胞クローン胚発生における卵割過程の長時間連続蛍光画像。計60時間撮影の一例。実際は15分間隔で撮影しているが、ここでは20時間ごとの画像を示した。緑色の1個1個が胚で12個示している。赤色は核・染色体、緑色は紡錘体。白線は50マイクロメーター。
- B: 共焦点レーザー顕微鏡を用いて観察しているため、3次元で胚を表示することも可能。
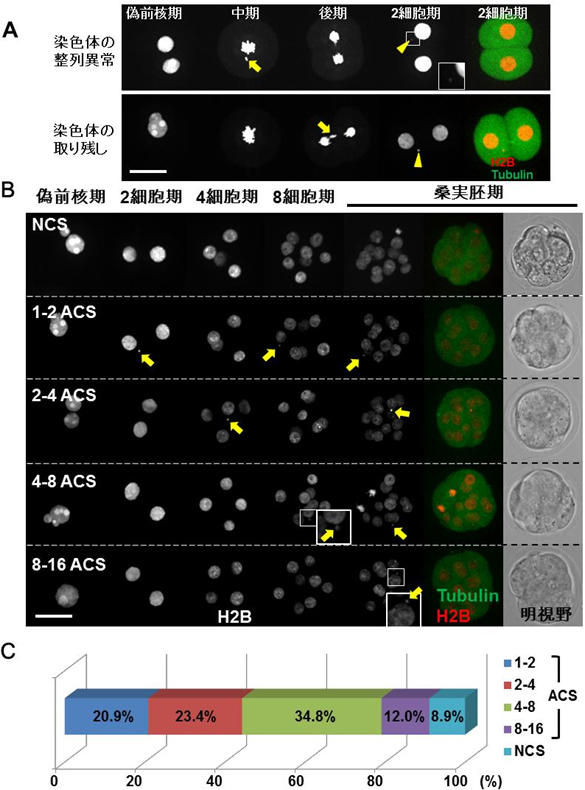
図3 クローン胚で見つかった染色体分配異常とその頻度
- A: 体細胞クローン胚で観察し染色体分配異常(ACS:Abnormal chromosome Segregation)の例。通常ならば卵割時に1カ所に整列するはずの染色体が、一部外に飛び出たり(上、黄色矢印)、染色体が2つに分かれる際に間に取り残されたりする様子(下、黄色矢印)が見られた。また、これらの異常の後、次のステージにおいて微小な核(上下、黄色矢頭)を形成するものが多かった。白線は50マイクロメーター。
- B:
各卵割ステージでの染色体分配異常。ACSは1細胞期から桑実胚期までの各卵割段階で起きていた。明視野で見た桑実胚の外見は、正常な染色体分配(NCS:Normal chromosome Segregation)の体細胞クローン胚もACSを起こした体細胞クローン胚も見分けがつかない。黄色矢印は分裂時に取り残された染色体あるいは微小核。白線は50マイクロメーター。
- NCS:16細胞期まで正常に染色体分配をした胚
- 1-2ACS:1から2細胞期にACSを起こした体細胞クローン胚
- 2-4ACS:2から4細胞期にACSを起こした体細胞クローン胚
- 4-8ACS:4から8細胞期にACSを起こした体細胞クローン胚
- 8-16ACS:8から16細胞期にACSを起こした体細胞クローン胚
- C: 各卵割段階でのACSの頻度。80%近くのクローン胚が8細胞期までにACSを起こした。
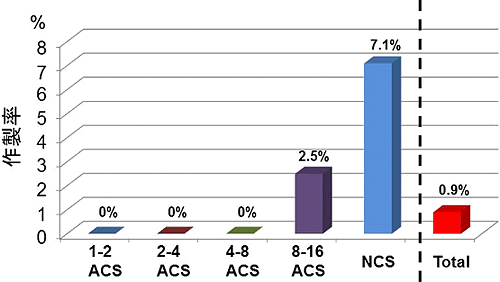
図4 各卵割段階で起きたACSと作製率の関係
クローン胚をACSの発生段階でグループ分けして、偽妊婦マウスに移植した結果の産仔作製率を示している。8細胞期までにACSを起こしたクローン胚は産仔になれないことが分かった。一方で、NCSや8細胞期以降にACSを起こしたクローン胚からは産仔が産まれた。Totalは全てのクローン胚を分けずに移植した場合を示しており、そのクローン作製の成功率は0.9%だった。この結果はNCSのクローン胚を見分けたことでクローン成功率が約8倍に改善したことを示している。
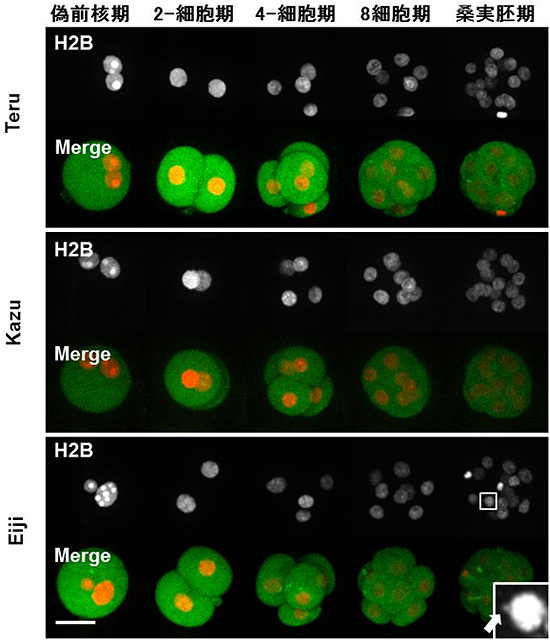
図5 産仔に至ったクローン胚の発生過程の連続画像
クローン胚の単一移植実験で産まれた3匹のクローンマウスに、出生順にTeru, Kazu, Eijiと名付け、それぞれのクローン胚の発生の様子を遡って解析した。Teru、KazuはNCS、Eijiは8-16ACSの胚だった。この結果からも、クローン胚が個体に発生するためには少なくとも8細胞期まで正常な染色体を持つことが必要であることが確認できた。白線は50マイクロメーター。
- H2B:核・染色体のみの連続画像
- Merge:核・染色体と紡錘体の連続画像
