2012年5月8日
独立行政法人 理化学研究所
水にしか溶けなかった核酸が有機溶媒に溶けて触媒機能を発揮
-有機溶媒中の核酸を触媒として利用し、新たな有機合成反応を可能に-
ポイント
- 水にも有機溶媒にも溶ける、ポリエチレングリコール(PEG)結合をした核酸を開発
- 有機溶媒中でも水中と同様に核酸の立体構造は保持され、触媒機能を発揮
- 核酸の触媒機能は、有機溶媒中の方が水中よりも熱的に安定
要旨
理化学研究所(野依良治理事長)は、これまで水にしか溶けなかった核酸を有機溶媒に溶かすことに成功しました。また、有機溶媒中の核酸は水中と同じ立体構造を保持し、熱的にも安定した触媒として機能することを見いだしました。これは理研基幹研究所(玉尾皓平所長)伊藤ナノ医工学研究室の阿部洋専任研究員(JSTさきがけ兼任)、阿部奈保子(元協力技術員)、伊藤嘉浩主任研究員らによる研究成果です。
核酸は生命現象を担う重要な生体分子ですが、リボザイム(ribozyme)※1などのように、その配列によっては生体反応の触媒(酵素)の役割も持っています。2000年以降になると、六員環を形成するディールズアルダー反応など、水中で有機合成反応を触媒するリボザイムが報告されています。しかし核酸は水にしか溶けません。有機合成反応をさまざまな環境で利用して、新たな機能性分子を創出するには、核酸を有機溶媒に溶かして触媒機能を発揮させる必要がありました。
化粧品などの材料で知られるポリエチレングリコール(PEG)は、タンパク質に結合させると、水にも有機溶媒にも溶かすことができるようになります。そこで研究チームは、ヒトテロメア配列※2と同じ配列のオリゴ核酸※3の末端に、PEGを結合したPEG-DNAを作製して可溶性を調べたところ、クロロホルム、ベンゼン、塩化メチレン、アセトニトリル、エタノールなど、ほとんどの有機溶媒に溶けることを発見しました。また、有機溶媒中でも水溶液中と同じ立体構造を保持し、触媒機能も同様に発揮することを確認しました。具体的には、水中で酸化反応を触媒するDNAザイム(DNAzyme)※1にPEGを結合して有機溶媒に溶かしたところ、発光試薬として広く利用されるルミノール※4を酸化させることが分かりました。
今回、生体分子に簡単な化合物を結合するだけで、有機溶媒中でも触媒機能を発揮させることに成功しました。この可溶化技術により、核酸の利用範囲は大きく広がります。今後、新たな有機合成反応の開発に貢献するなど、広範な化学の研究分野を形成すると期待できます。
本研究成果は、ドイツの化学会誌『Angewandte Chemie International Edition』に近くオンライン掲載されます。
背景
核酸は生命現象を担う重要な生体分子で、その配列は遺伝情報の記憶、個体の独自性の識別、生体反応の触媒(酵素)など多くの役割を持っています。1995年頃には、これらの性質を利用した情報記録手段として、メモリ、分子認識、バーコードタグなどに核酸を応用する研究が報告されています。さらに2000年以降には、核酸の情報を利用して、一度に複数の反応を進行させたり、生物活性分子の創出に利用したりできることが示されました。また、リボザイムなどの人工核酸が有機合成反応を触媒することも明らかになりました。しかし、核酸は水にしか溶けないため、こうした機能は水中だけに限られ、有機溶媒中では利用できませんでした。核酸が有機溶媒に溶けて機能すると、有機合成反応の利用範囲は大きく広がります。そのため、機能を損なうことなく核酸を有機溶媒に溶かす方法の開発が望まれていました。
研究手法と成果
研究チームは、核酸を構成する4個の塩基(A:アデニン、T:チミン、G:グアニン、C:シトシン)を21個つなげて、ヒトテロメア配列として知られる分子量約3,000のオリゴ核酸(5'-GGG TTA GGG TTA GGG TTA GGG- 3')を合成し、その末端に分子量約5,000のPEGを1個結合したPEG-DNAを作製しました(図1)。このPEG-DNAは、クロロホルム、ベンゼン、塩化メチレン、アセトニトリル、エタノールなどの有機溶媒に、少なくとも0.2mM(ミリモル/リットル)の濃度まで溶解しました(図2)。
次に、溶解したPEG-DNAの立体構造が、有機溶媒中と水中でどう異なるかについて調べました。カリウムイオンを含んだ水中でGカルテット構造※5をとるPEG-DNAを有機溶媒(ジクロロエタン)に溶かし、円偏光二色性分光法(CD)※6で立体構造を解析しました。その結果、有機溶媒中にカリウムイオンが存在すると、水中と全く同じGカルテット構造をとることが分かりました(図3)。これまで、PEGを結合して、オリゴ核酸の立体構造を保持したまま有機溶媒に溶かした報告例はありません。また、水中では50~59℃になると立体構造が崩れるのに対し、有機溶媒中では10~80℃の範囲で立体構造が変化せず、非常に安定であることが分かりました。このことは、広い温度範囲で触媒機能が利用できることを示します。さらに、酸化反応を触媒するDNAzyme(5'-TTA GGG-3')にPEGを結合してメタノールに溶かしたところ、やはりその構造は保持されました。そこで、過酸化水素(H2O2)と反応して酸化されると青紫色を発光するルミノールと混ぜたところ、水中とほぼ同じ速度で反応が進行し、青紫色の発光を確認しました(図4)。
今後の期待
PEGを核酸の末端に結合するだけ、という「簡単な」手法により、核酸がさまざまな有機溶媒に溶けるようになりました。これまで、水中での核酸の構造・機能に関する研究は盛んに行われてきましたが、今後は有機溶媒中でのオリゴ核酸の性質と比較することができます。具体的には、「有機溶媒中の塩基の水素結合は水中より強くなるのか?」、「核酸の立体構造は、有機溶媒の種類によってどのように影響を受けるのか?」といった核酸の相互作用に関する謎の解明に貢献します。また、PEGを結合した核酸は、ほとんどの有機溶媒(アセトニトリル、ベンゼン、アルコール系、ハロゲン系)に溶けます。そのため、機能性核酸分子の利用範囲を、水からさまざまな有機溶媒へと広げることができます。それによって、有機溶媒に溶かした核酸を触媒に用いた新たな有機合成反応の開発など、多くの利用法を生み出すことが期待できます。
発表者
理化学研究所
基幹研究所 伊藤ナノ医工学研究室
専任研究員 阿部 洋(あべ ひろし)
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.リボザイム(ribozyme)、DNAザイム(DNAzyme)
タンパク質酵素のように触媒能を有するデオキシリボ核酸(DNA)がDNAzyme、リボ核酸(RNA)がリボザイムと呼ばれる。 - 2.テロメア配列
真核生物の染色体の末端部分にある構造で、その末端部分を保護する役目を持つ。通常は複製の度に短くなっていく。 - 3.オリゴ核酸
2個以上の核酸塩基で構成されるデオキシリボ核酸(DNA)あるいはリボ核酸(RNA)。 - 4.ルミノール
含窒素化合物で、酸化されると発光する。血液検査のルミノール発光に用いられる。 - 5.Gカルテット構造
ヒトテロメア配列として知られ、G(グアニン)が繰り返し並ぶグアニン四量体。 - 6.円偏光二色性分光法(CD)
右円偏光と左円偏光のどちらを吸収しやすいかを測定する手法。右巻きのバネと左巻きのバネのようなキラルな分子は、円偏光のどちらか一方を選択的に吸収する。円偏光二色性は、Circular Dichroismの頭文字からCDと略される。
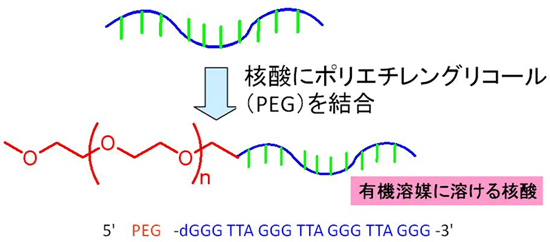
図1 オリゴ核酸にポリエチレングリコール(PEG)を結合したPEG-DNA
21個の塩基をつなげたヒトテロメア配列由来の核酸(分子量約3,000)の末端に、分子量が約5,000のポリエチレングリコール(PEG)を化学結合させた。
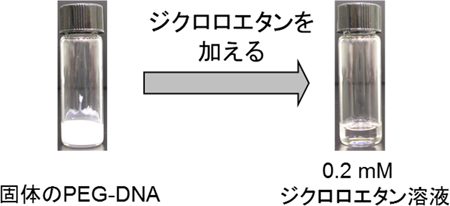
図2 ジクロロエタン溶液に溶けるPEG-DNA
PEG-DNAを非極性有機溶媒であるジクロロエタンに溶かした。少なくとも0.2mM(ミリモル/リットル)の濃度まで溶けることを確認した。
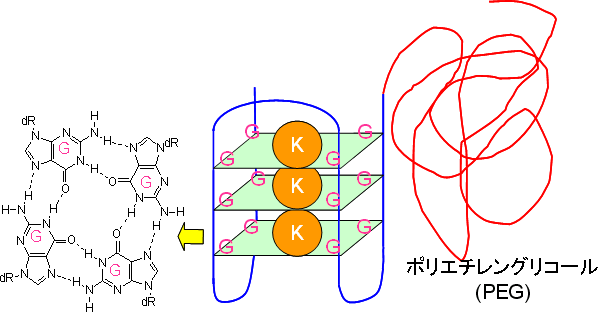
図3 有機溶媒中におけるPEG‐DNAによるGカルテット構造
G:グアニン、K:カリウムイオン
ヒトテロメア配列を有するPEG-DNAは、カリウムイオンが存在すると、水中でも有機溶媒中でもGカルテット構造を形成する。
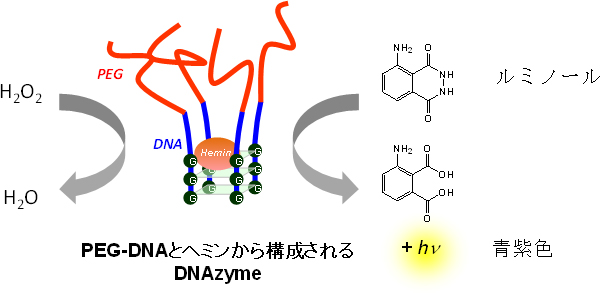
図4 有機溶媒中におけるPEG-DNAzymeによる酸化反応
G-カルテット構造を有するPEG-DNAzymeの構造。中心にヘミンという鉄イオン含有ポルフィリン誘導体を結合している。
PEG-DNAzymeはメタノール中でルミノールを効率よく酸化し、青紫色を発光する。
